Повышение эффективности использования гидроидов при биотестировании: выбор вида, сезона, температурного режима
Повышение эффективности использования гидроидов при
биотестировании: выбор вида, сезона, температурного режима
Карлсен А. Г., Марфенин Н. Н.
Среди
различных видов гидроидов чувствительность к повышенному содержанию в морской
воде ионов цинка во много раз различается. С помощью регистрации доли
рассосавшихся за 1—2 сут гидрантов у ObeUa loveni можно без применения дорогостоящего
оборудования даже в полевых условиях установить наличие в воде токсических
примесей (ионов цинка в концентрации 0,5 мг/л и выше). Чувствительность метода
может быть повышена, если использовать материал в период начала активного роста
колоний после зимней диапаузы.
В
последнее время была экспериментально доказана высокая чувствительность
гидроидов к различным токсическим веществам, добавляемым к морской воде (Karbe,
1972; Stebbing, 1980a, 1981), что ставит их в ряд перспективных объектов для
биотестирования (Stebbing, 1980b). Поэтому возникла необходимость выявить среди
гидроидов виды, наиболее чувствительные к токсикантам, и условия, при которых
указанная чувствительность проявляется в наибольшей мере.
Работа
в этом направлении уже была начата нами ранее (Карлсен, Марфенин, 1987). На
трех видах гидроидов рода Obelia—О. loveni (Allm., 1859) О. flexuosa (Hincks,
1861), 0. geniculata (L., 1758), взятых из моря в августе, было испытано в
лабораторных условиях действие различных концентраций ионов цинка и меди в
морской воде. Эффект токсического воздействия регистрировали по доле
дедифференцировавшихся гидрантов через 1—2 сут, сопоставляя их в
экспериментальных и контрольных колониях. Тогда было установлено, что,
вопервых, среди обелий наиболее чувствительный к тосикантам вид О. loveni. а
вовторых, чувствительность его к токсическому воздействию повышается при
возрастании температуры (от 14 к 18°).
В
настоящем исследовании мы продолжили изучение сравнительной чувствительности
различных видов гидроидов к ионам цинка, испытав его воздействие на более
примитивных гидроидах Clava multicornis (Forskal, 1775) и Coryne tubulosa (M.
Sars, 1835), относящихся к подотряду Athecata.
Кроме
того, мы проверили реакцию на длительное воздействие (до 22 сут) различных
концентраций ионов цинка трех видов обелий: О. longissima (Pallas, 1766), 0.
loveni, 0. flexuosa, а также более высокоорганизованного гидроида Dynamena
pumila (L., 1758) из семейства Sertulariidae того же подотряда Thecaphora.
Наконец,
для О. loveni проведено сравнение реакции гидроида на стандартные испытываемые
нами концентрации ионов цинка в разное время вегетационного сезона—в его начале
(апрель) и в конце (август).
Полученные
результаты позволяют сделать предварительные выводы о характере вариаций в
чувствительности гидроидов к токсикантам, что поможет, как мы надеемся,
избежать необоснованных экстраполяции и уточнить подход к выбору объектов для
биотестирования.
Материал и методы
Основные
методы описаны в предыдущих публикациях. Культивирование гидроидов в лабораторных
условиях осуществляли по специально разработанному методу (Бурыкин с соавт.,
1984). Рост гидроидов учитывали периодически, подсчитывая число имеющихся в
колонии гидрантов. Метод определения действия ионов цинка на процесс
дедифференцировки гидрантов сводился к сравнению относительного количества
дедифференцировавшихся гидрантов в опыте и контроле (Карлсен, Аристархов, 1986;
Карлсен, Марфенин, 1987). Относительное количество дедифференцировавшихся
гидрантов определяли как отношение их числа к общему числу гидрантов в колонии
к моменту наблюдения (в процентах). Общее количество гидрантов в каждом опыте
было не менее 30 и, как правило, превышало 100. Самые большие выборки (200— 400
гидрантов) были в опытах, в которых определяли действие минимальных концентраций
токсиканта. В этих же статьях описан способ приготовления рабочих растворов,
содержавших ионы цинка в повышенной концентрации. При кратковременных
наблюдениях (около 2 сут) растворы не меняли, гидроиды находились в чашках
Петри в термостате. При хронических экспериментах растворы меняли 1 раз в 2
сут. Срок выбран на основании данных, показывающих, что через 2 сут 20%, а
через 6 сут 80% ионов ртути “исчезает” из раствора (Baier et al., 1975).
Специальные исследования поведения ионов цинка в растворе не проводили.
Статистическую
обработку результатов проводили по критерию Стыодента (Лакин, 1980).
Материал
собирали в разные месяцы: в марте, апреле, мае и августе в течение 1984 и 1985
гг. На Еремеевском пороге Великой Салмы Белого моря. Работу проводили на
Беломорской биостанции МГУ (пос. Приморский).
Результаты
1.
Действие ионов цинка на гидроидов Clava multicornis (Forskal, 1776) и Coryne
tubulosa (M. Sars, 1835) (подотряд Athecata). Представители подотряда Athecata
оказались менее чувствительными к действию ионов цинка, чем исследованные нами
обелии из подотряда Thecaphora. Так, гидроид Clava multicornis, принесенный с
моря в августе после полового размножения, сохранял жизнеспособность в
растворах, содержавших ионы цинка в концентрациях 10,0, 5,0 и 2,5 мг/л в
течение 39 ч (до конца эксперимента).
Колонии
Coryne tubulosa, принесенные с моря в марте и постепенно адаптированные к
теплой (18°) воде, наблюдали в течение 20 сут. Колонии в контрольных условиях
быстро росли, увеличивалось число гидрантов. Практически так же хорошо рос
гидроид в растворе с концентрацией ионов цинка 1,0 мг/л. При 2,5 мг/л колонии
не погибали, но их рост не сопровождался заметным увеличением числа гидрантов,
т. е. количество образовавшихся новых и дедифференцировавшихся старых гидрантов
было приблизительно одинаковым (рисунок. А). При 3,0 мг/л все колонии погибали
не позднее, чем через 2 сут.
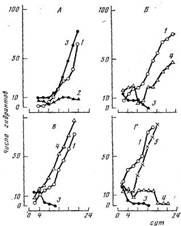
Количество
гидрантов в колониях, которые росли в условиях повышенных концентраций ионов
цинка; А — Coryne tubulosa, Б—Obelia flexuosa, В—Obelia geniculata Г—Obelia
loveni, /—контроль; концентрация ионов цинка 2,5 мг/л (2), 1,0 (3), 0,5 (4),
0,25 мг/л (5)
2.
Долговременный рост гидроидов рода ObeUa (подотряд Thecaphora) в присутствии
повышенных концентраций ионов цинка. Если колонии, извлеченные из моря в начале
марта, когда они находятся в состоянии гипобиоза, предварительно адаптировать к
теплой (18°) воде в течение 6 сут, то все они начинают бурно расти. В
контрольных условиях этот рост сохраняется на протяжении всего эксперимента
(15—22 сут).
В
присутствии ионов цинка в концентрации 1,0 мг/л все три вида гидроидов растут
хуже, чем в контрольных условиях, и через 10—12 сут погибают (рисунок, б—г).
При концентрации 2 мг/л гидроиды погибают через 2 сут. При концентрации 0,5
мг/л Obelia flexuosa и Obelia longissimа растут практически так же, как в
контроле (рисунок, Б, 5), а О. loveni растет хуже (рисунок, Г), хотя в течение
всего эксперимента не гибнет. При концентрации 0,25 мг/л и О. loveni растет так
же, как в контроле.
3.
Действие повышенных концентраций ионов цинка на гидроид Dynamena pumila
(подотряд Thecaphora). Рост колоний D. pumila в эксперименте был неустойчив,
поэтому удалось установить только летальные концентрации ионов цинка, которые
оказались выше, чем у обелий.
Длительные
наблюдения за состоянием гидроида показали, что если его в марте сразу
поместить в раствор с ионами цинка в период адаптации к теплой воде, то он
погибает в течение 2—3 дней в растворе 3,0 и 2,5 мг/л и через 20 дней при
концентрации 1 мг/л. Если же гидроид предварительно в течение 6 сут
адаптировать к теплой воде и только после это го поместить в экспериментальные
условия, то он, по крайней мере в течение 18 сут, сохраняет жизнеспособность
при концентрации ионов цинка 2,5 мг/л.
Таблица
1
Доля
дедифференцировавшнхся гидрантов (%) у Obelia loveni при 18° в разные периоды
вегетации в материале из моря (*) и в лабораторной культуре (**) после
увеличения концентрации ионов цинка
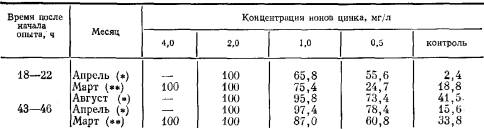
Примечание.
Различие в 19% и более достоверно с вероятностью 95—99,9%. Меньшие различия
кедосто верны,
4.
Особенности регистрации токсического эффекта на гидроидах в зависимости от
периода их вегетации. На наиболее чувствительном к воздействию ионов цинка
гидроиде О. loveni мы сопоставили реакцию его гидрантов на повышенные
концентрации ионов цинка ранней весной (апрель) и в конце лета (август), а
также в марте (лабораторная культура). Мы рассчитывали выяснить, одинаковы ли
вызывающие токсический эффект пороговые концентрации ионов цинка в начале и в
конце сезона вегетации.
Как
уже отмечалось выше, ранней весной колонии О. loveni в море еще не растут и
бывают без гидрантов. Перенос их в аквариум с более теплой водой (в данном
случае 17—18°) стимулирует образование гидрантов и начало роста побегов и
столонов. На этом фоне перехода из одного морфофункционального состояния в
другое (Марфенин, 1980) было проведено испытание токсического воздействия цинка
в одной серии опытов (табл. 1, апрель). В другой серии опыты были осуществлены
не сразу после переноса материала из моря в значительно отличающиеся по
температуре аквариумные условия, а лишь по прошествии 1—2 нед, т. с. после
того, как прошла адаптация гидроидов и культура стала лабораторной (табл. 1,
март).
В
августе материал для опытов брали иа моря. Различие по температуре при переносе
гидроидов в лабораторию было всего в несколько градусов (от 14 до
18°).Результаты опытов, проведенных по единой методике учета доли рассосавшихся
гидрантов во взятых для эксперимента побегах О. loveni, показали, что при
концентрации цинка, равной 2,0 мг/л, и температуре 18° через 18—22 ч все
гидранты у подопытных побегов дедифференцируются во всех случаях.При концентрации
ионов цинка, равной 1,0 мг/л, доля дедифференцировавшихся гидрантов через 18—22
ч была выше в августе, а весной была выше в лабораторной культуре (табл. 1).
Однако через 43—46 ч в весенних опытах доля рассосавшихся гидрантов стала выше
в материале, взятом непосредственно из моря. Это означает, что через 2 сут при
данной температуре и при данной концентрации ионов цинка реакция гидроидов во
всех случаях приблизительно одинакова.
При
меньшей концентрации ионов цинка (0,5 мг/л) токсический эффект через 18—22 ч
проявился в весеннем материале, взятом из моря (апрель), и в августовском
материале. В лабораторной культуре весной доля дедифференцировавшихся гидрантов
в это время от контроля достоверно не отличалась. Однако через 2 сут
токсическое действие ионов цинка проявилось и в лабораторной культуре, хотя
доля рассосавшихся гидрантов оставалась все же более низкой, чем в материале из
моря.
Таблица
2
Зависимость
доли дедифференцировавшихся гидрантов (%) у гидроида Obelia loveni, взятом из
моря от температуры, концентрации ионов цинка в морской воде и
продолжительности опыта

*
Отличия ог контроля с вероятностью 95%. ** То же, Р=99,0%.
Примечание.
Опыты при температуре 18 и 22° были поставлены в мае. а при 14,5° в августе.
Данные
по дедифференцировке гидрантов в эксперименте могут иметь значение для оценки
токсического эффекта лишь при сопоставлении с контрольными значениями, которые
сильно различались в перечисленных трех сериях опытов.Менее всего
дедифференцировка гидрантов в контроле была выражена в материале, взятом весной
из моря, накануне перед опытом, сильнее в лабораторной культуре и еще больше
доля дедифференцировавшихся гидрантов в контроле была в августовском
материале.Чем интенсивнее идет дедифференцировка гидрантов в контроле, тем
сложнее использовать материал для биотестирования. Так, например, по абсолютным
значениям дедифференцировавшихся гидрантов в опытах с действием ионов цинка
было больше всего в августе, но и дедифференцировка в контроле была в это время
самой большой. Поэтому нельзя утверждать, что в августе гидроиды более
чувствительны к токсическому воздействию ионов цинка. Скорее мы приходим к
обратному заключению, что именно весной, вскоре после перехода колоний в период
активного роста благодаря относительно слабой дедифференцировке в контроле
возможна более чуткая индикация пороговых значений токсических примесей.
5.
Роль температурного режима в повышении чувствительности метода. Повышение
температуры до некоторых пределов приводит к ускорению ряда физиологических
процессов, в том числе у гидроидов: к ускорению роста колонии (Kinne,
Paffenhofer, 1966; Tusov, Davis, 1971; Бурыкин, 1980), интенсивности
дедифференцировки (Crowell, 1953) и формирования (Crowell, 1957) гидрантов,
уменьшению периода ростовых пульсаций (Wyttenbach, 1974) и т. д. Поэтому мы
попытались повысить чувствительность метода с помощью регистрации токсического
эффекта при наиболее высокой температуре, близкой к верхней температурной
границе существования этих гидроидов (табл. 2).
В
мае колонии О. loveni, находящиеся в состоянии перехода из зимнего гипобиоза к
активному росту, мы переносили в лабораторию и содержали при температуре 22,0°.
Порог чувствительности к цинку оказался в этом случае не выше 0,25 мг/л. При
18° (параллельный эксперимент) и при 14,5° (август) пороги чувствительности
гидроидов к ионам цинка оказались около 0,5 и 1,0 мг/л соответственно (табл.
2). Поэтому увеличение температуры можно рассматривать как один из путей
повышения чувствительности метода.
Обсуждение результатов
Впервые
достаточно высокая чувствительность гидроидов к цинку была обнаружена Карбе
(Karbe, 1972). Он провел экспериментальные исследования гидроида Eirene
viridula Eschscholtz, 1829, относящегося к сем. Campanulinidae, подотряд
Thecaphora, и установил, что полипы чувствительны к ионам цинка при
концентрации 1,5—3,0 мг/л.Вслед за Карбе английский исследователь Стеббинг
(Stebbing, 1976, 1979, 1980b; Stebbing, Santiago—Fandino, 1983) подробно
занялся возможностью использования гидроидов в качестве тестобъектов. Используя
гидроид Obelia flexuosa (Hincks, 1861) из сем. Campanulariidae, подотряд
Thecaphora, он показал, что колонии этого гидроида погибают при содержании в
морской воде меди в концентрации около 0,05 мг/л, а кадмия—0,5 мг/л. Пытаясь
обнаружить токсическое действие тяжелых металлов на организм гидроидов задолго
до их гибели, Стеббинг стал использовать различные морфологические и
физиологические показатели, например частоту образования гонозооидов
(специализированных половых зооидов), скорость роста тела колонии, число
зооидов в экспериментальных колониях по отношению к контролю. Таким способом
Стеббингу удалось достоверно зарегистрировать эффект стимуляции роста колонии и
частоты образования гонозооидов при очень малых концентрациях токсикантов (0,1
мкг/л меди и 0,05 мг/л кадмия) (Stebbing, 1980a, 1981). Этот эффект, известный
ранее под названием закона АрндтаШульца, а затем “хормезиса”, был описан
неоднократно для разных объектов (Stebbing, 1982). Для нас важно, что Стеббинг
подробно изучил его проявление и по возможности механизм у гидроидов с целью
практического использования этого эффекта для биотестирования (Stebbing et al.,
1983).
Метод
основан на регистрации дедифференцировки гидрантов в эксперименте и контроле.
Рассасывание гидрантов и частей колонии—характерное явление у гидроидов. Оно
было обнаружено в начале нашего века (Thatcher, 1903; Huxley, DeBeer, 1923) и
первоначально считалось результатом реакции колонии на неблагоприятные условия
существования, в частности воздействия ядов.Хаксли и Де Вир на гистологических
препаратах подробно исследовали весь процесс рассасывания гидрантов у О.
geniculata и сравнили его с дифференцировкой в обратной
последовательности—укорачиваются щупальца, смыкается гипостом, утоньшается и
делается короче тело гидранта, становясь похожим на зачаток в момент начала
дифференцировки гидранта. Исходя из этих особенностей процесса, они назвали его
“дедифференцировкой”. Они же установили, что материал дедифференцировавшихся
гидрантов поступает внутрь колонии и используется ею.
После
того как колонии гидроидов научились содержать в лабораторных условиях (Fulton,
1960), выращивая их на стеклах, Кровеллом (Crowell, 1953) было обнаружено, что
у кампануляриид дедифференцировка гидрантов—регулярный процесс, связанный с их
(гидрантов) коротким жизненным циклом. На месте дедифференцировавшихся
гидрантов через короткое время при благоприятных условиях образуются новые
гидранты, которые, так же как и предшествовавшие им, примерно через неделю
“старятся” и рассасываются.
Все
это помогает лучше представить возможности повышения эффективности
использования нашего метода для биотестирования. Пытаясь увеличить “разрешающую
способность” предлагаемого метода, мы должны действовать одновременно в двух
направлениях—искать способы повышения чувствительности гидрантов к токсикантам
и в то же время пытаться уменьшить скорость рассасывания их в контроле.Что
касается чувствительности объекта к токсикантам, то преждевсего следует выявить
наиболее восприимчивые к ним виды гидроидов.. Ранее (Карлсен, Марфенин, 1987)
мы уже установили, что из трех видов рода Obelia наиболее удачный для
биотсстирования — О. lovеni.Испытание еще четырех видов гидроидов из разных
семейств, результаты которого приведены в данной статье, показало, что они
менее чувствительны к токсическому действию ионов цинка по сравнению с О.
loveni. Следовательно, подтвержден сам факт различной восприимчивости гидроидов
к токсикаптам, и дальнейший поиск наиболее чувствительных видов имеет смысл и
должен быть продолжен.Можно ожидать, что степень влияния токсикантов на колонии
различается на разных этапах их жизненного цикла. Действительно, в жизни
колонии есть периоды, в течение которых токсический эффект, вероятно, трудно
было бы установить. Это, например, гипобиотическое состояние во время зимней
диапаузы или же период депрессии после размножения (Марфенин, 1980). С другой
стороны, были основания предполагать, что переход из гипобиотического состояния
к активному росту колонии или же период подготовки колонии к зимней диапаузе
более восприимчивы к токсическим воздействиям.
Мы
не проводили систематического изучения этого вопроса, а ограничились сравнением
действия цинка на двух этапах жизненного цикла колонии, первый из которых
соответствует переходу из гипобиотического к активному состоянию ранней весной,
а второй—росту после размножения в конце лета. Можно считать, что различие в
степени проявления токсического эффекта подтвердилось, однако это произошло на
фоне еще более значительных различий в контроле. Это служит хорошим примером
того, что уменьшение дедифференцировки гидрантов в контроле—не менее важный
путь увеличения разрешающей способности методики. Эффективность метода можно
также повысить, работая при более высоких температурах.
Если
же подойти к проблеме повышения эффективности использования гидроидов для
биотестировапия со стороны совершенствования контроля, то и в этом случае, судя
по полученным нами результатам, можно надеяться на весомый успех. Почти в 20
раз различалась доля дедифференцировавшихся гидрантов в контроле через 20 ч
после начала эксперимента у колоний при переходе из гипобиотического состояния,
с одной стороны, и летнем материале—с другой. При переходе колоний к активному
росту после зимней диапаузы все гидранты начинают расти одновременно и,
следовательно, должны дедифференцироваться также одновременно—приблизительно
через 1 нед. Этим объясняется столь низкое значение доли дедифференцировавшихся
гидрантов в контроле у апрельской серии через 20 ч. Достаточно было провести
эксперимент на материале, уже адаптированном к комнатной температуре, т. е.
через 1—2 нед после начала роста колоний, как доля дедифференцировавшихся
гидрантов в тех же условиях стала существенно выше.
Через
2 сут после начала эксперимента дедифференцировка гидрантов в контроле всегда
возрастала. Это связано с тем, что по условиям предлагаемой методики побеги с
гидрантами не получали пищи. Голодание ускоряло рассасывание и одновременно
делало более редкой дифференцировку новых гидрантов.
Таким
образом, в результате проведенных исследований стало ясно, что для
биотестирования лучше всего использовать колонии в период .перехода их из
состояния покоя в состояние активного роста. По дедифференцировке гидрантов в
течение 1 сут можно достоверно зарегистрировать токсический эффект малых
концентраций ионов цинка в воде, .которые, как показали долгосрочные
эксперименты, являются сублетальными даже для испытываемых видов гидроидов, а
тем более для других организмов.
Список литературы
Бурыкин
Ю. Б. Регулирующая роль некоторых экологических факторов в процессах роста и
интеграции колониальных гидроидов//Теоретическое и практическое значение
кишечнополостных. Л.: ЗИН АН СССР, 1980. С. 16.
Бурыкин
Ю. Б., Марфенин Н. Н„ Карлсен. А. Г. Опыт содержания мирского колониального
гидроида Dynamena pumiia (L.) и лабораторных условиях//Научн. докл, высш.
школы. Биол. науки. 1984. № 1. С. 102.
Карлсен.
А. Г., Аристархов В, М. Изменение постоянным магнитным полем токсического
действия растворов хлорида цинка на колониальных гидроидов Obelia loveni и
Obelia flехиоsа//Изв. АН СССР. Сер. биол. 1986. № 2. С. 230—237.
К.арлсен
А. Г., Марфенин 11. Н. Действие повышенных концентраций ионов цинка на
некоторых гидроидов//Научн. докл. высш. школы. Биологические науки, 1987,№ 1,
с. 71—73
Лакин
Г. Ф. Биометрия. М.: Высш. школа, 1980. С. 104, 271. Марфенин Н. Н. Основные
морфофункциональные состояния колонии у гидроида Dynamena pumiia (L.) в
естественных условиях//Докл. АН СССР. 1980. Т. 255. № 1.С. 253.
Патин,
С. А. Особенности распространения и биологического действия загрязняющих
веществ в Мировом оксане//Человек и биосфера. М.: Издво
МГУ, 1982. Вып. 7.С. 62.
Baier R. W. Wojnowich G., Petrie L. Mercury loss from culture
media//Analyt. Chem. 1975. V. 45. P. 2464.
Crowell S. The regressionreplacement cycle of hydranths of Obelia
and Campanularia//Physiol. Zool. 1953. V. 26. № 4. Р.
319.
Baier R. W., Wojnowich G., Petrie L. Mercury loss from culture
media//Analyt. Chem. 1975. V. 45. P. 2464.
Crowell S. The regressionreplacement cycle of hydranths of Obelia
and Campanularia//Physiol. Zool. 1953. V. 26. № 4. Р.
319.
Crowell S. Differential responses of growth zones to nutritive
level, age, and temperature in the colonial hydroid Campanularia//J. Expti
Zool. 1957. V. 134. P. 63.
Fulton С. Culture of a colonial hydroid
under controlled conditions//Scicnce. 1960,V. 132. P. 473.
K.arhe L. Marine Hydroiden als Testorganismen zur Prufung der
Toxizitat von Abwasserstoffen. Die wirkung von Schwermetallen auf Kolonien von
Eirene viridula//Marine Biol. 1972. В, 12. № 4. S. 316.
Kinne 0., Paffenhoger G. A. Growth and reproduction as a function of
temperature and salinity in Clava multicornis (Cnidaria, Hydro2oa)//Helgolander
wiss. Meeres. 1966.В. 13. № 1—2. S. 62. Stebbing A, R.
D. The effect of low metal levels on a clonal hydroid//J. mar. biol. Ass.U. K.
1976. V. 56. P. 977.
Stebbing A. R. D. As experimental approach to the determinants of
biological water quality//Phi!os. Trans. Roy. Soc. London. 1979. V. 286. P.
465.
Stebbing A. R. D. Increase in gonozooid frequency and adaptive
response to stress in Campanularia flexuosa.— In: Developmental and cellular
biology of coelenterates/' Eds Tardent P., Tardent R Amsterdam: Elsevier,
1980a. P. 27.
Stebbing A. R. D. The biological measurement of water quality
//Rapp. P.—v. ReunCons. int. Exolor. Mer. 1980b. V. 179. P. 310.
Sfebbing A. R. D. Hormesis—stimulation of colony growth in
Campanularia flexuosa' (Hydrozoa) by copper, cadmium and other
toxicants//Aquatic Toxicol. 1981. V 1. P. 227.
Stebbing A. R. D. Hormesis—the stimulation oi growth by low levels
of inhibitors//Scitotal environment. 1982. V. 22. P. 213.
Stebbing A. R. D., Cleary J. S Brinsley M„ Goodchild C., Santiago —
Fandino V. Responses of a hydroid to surface water samples from the river Tamar
and Plymouth sound in relation to metal concentration s/'/J. mar. biol. Ass. U.
K. 1983. V. 63. № 4. Р. 695.
Sfebbing A. R. D„ Santiago—Fandino V. G. R. The combined and separate
effect of copper and cadmium on the growth of Campanularia flexuosa (Hydrozoa)
colonies// Aquatic Toxicol. 1983. V. 3. P. 183.
Thuicher H. F. Absorption of the hydranth in hydroid polyps//Biol.
Bull. 1903. V. 5. №2. Р. 295.
Tusov J; Davis L. V. Influence of environmental factors on the
growth of Bougainvillia. sp.//Exptl Coelenterate Biol./Eds Lenhoff H. M.,
Muscatine L., Davis L. V. Honolulu. 1971. P. 54.
Wyttenbach C. R. Cell movements associated with terminal growth in
colonial hydroids//Amer. Zool. 1974, V. 14. № 2. Р. 699.
Для
подготовки данной работы были использованы материалы с сайта http://soil.msu.ru/