Расчет каскада пачуков для кислотного выщелачивания урана
Содержание
Введение
1. Цель
расчета
. Данные для
расчета
3.
Материальный расчет
4. Тепловой
расчет
5.
Конструктивный расчет
Заключение
Литература
Приложение А
Приложение В
Введение
Выщелачивание - это гетерогенный процесс, скорость которого определяется
либо скоростью химической реакции, либо диффузионным массопереносом.
Процесс кислотного выщелачивания применяют для извлечения урана из
урановых руд. Разбавленные после измельчения пульпы, сгущают до 50-60 % по
твердому веществу и направляют на выщелачивание. Большинство урановых руд
являются высококремнистыми, поэтому в качестве выщелачивающего агента
используют раствор серной кислоты.
Процессы выщелачивания ведут в агитаторах (аппараты с механическим
перемешиванием), пачуках (аппараты с пневматическим перемешиванием), в
пульсационных перемешивающих устройствах и пульсационных колоннах.
В результате выщелачивания получаются пульпы, урансодержащие растворы с
избытком выщелачивающего агента и твердой фазы из пустой породы. Для отделения
твердых частиц и получения чистого раствора применяют декантацию (отстаивание)
и классификацию.
В данной работе будет произведен расчет каскада пачуков для кислотного
выщелачивания урана.
1. Цель расчета
Целью расчета является закрепление теоретических выводов и расчетно-практических
рекомендаций по курсу «Технология и оборудование спец. производств» и их
приложение к конкретному материальному, тепловому, конструктивному расчету
каскада пачуков для кислотного выщелачивания урана.
2. Данные для расчета
Исходные данные приведены в таблице 1.
Таблица 1
Исходные данные
|
Состав руды:
|
Содержание, %
|
Степень выщелачивания
|
|
- UO3 - UO2 - V2O5 - FeO - CaCO3 - Инертные
|
0,07 0,03 1,0 1,0 2,0 остальное
|
90% 90% 100% 50% 100% 0%
|
|
1. Производительность по урану, кг/час
|
10,0
|
|
2. Температура, 0С
|
60
|
|
3. Концентрация H2SO4, г/л
|
20
|
|
4. Избыток H2SO4, %
|
20
|
|
5. Время выщелачивания, час
|
12
|
|
6. Окислитель
|
MnO2
|
|
7. Избыток MnO2, %
|
50%
|
Примечание: 1) нагрев осуществляется острым паром; 2) каскад из трех
пачуков
Основные химические реакции, протекающие в процессе кислотного
выщелачивания:
1) UO3 + H2SO4 =UO2SO4
+ H2O;
2) UO2 + MnO2 + 2H2SO4
= UO2SO4 + MnSO4 + 2H2O;
) V2O5 + H2SO4
= (VO2)2SO4 + H2O;
) FeO + H2SO4 = FeSO4
+ H2O;
) CaCO3 + H2SO4 =
CaSO4 + H2O + CO2.
3. Материальный расчет
Материальный расчет процесса выщелачивания будет сводиться к составлению
материального баланса для каждой реакции отдельно, а, затем, к составлению
материального баланса для всех реакций совместно. Для удобства, материальный
расчет произведем на тонну руды.
а) первая реакция
0,7кг3 + H2SO4
=UO2SO4 + H2O (U=90%).
238+48 2+32+64 238+32+32+64 2+16
ММ 286 98 366 18
По реакции определим массы всех компонентов:
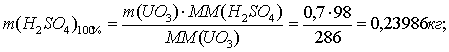

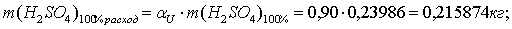
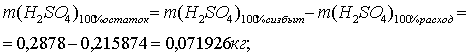
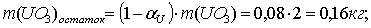
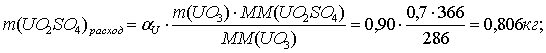
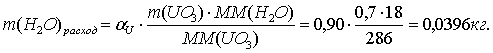
Составим таблицу материального баланса для первой реакции.
Таблица 2
Материальный баланс для первой реакции
|
Приход
|
Расход
|
|
Статьи прихода
|
Статьи расхода
|
кг
|
|
1. UO3 2. H2SO4 с избытком
|
0,7 0,2878
|
1. UO3 остаток 2. UO2SO4 3.
H2O 4. H2SO4 остаток
|
0,07 0,806 0,0396 0,071926
|
|
Итого:
|
0,9878
|
Итого:
|
0,9875
|
Поскольку материальный баланс сошелся, значит, расчеты по первой реакции
были произведены верно.
б) вторая реакция
,3кг
UO2 + 2H2SO4 + MnO2 =UO2SO4 + MnSO4 + 2H2O (U=90%).
+32 2+32+64 54,9+32 238+32+32+64 54,9+32+64 2+16
ММ 270 196 86,9 366 150,9 36
По реакции определим массы всех компонентов:
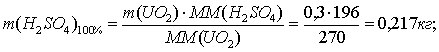
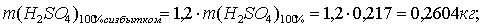
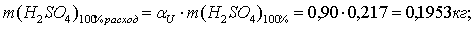
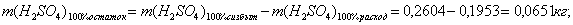
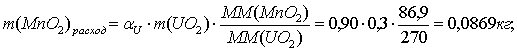
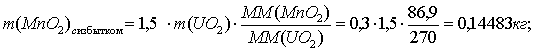
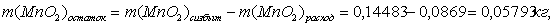


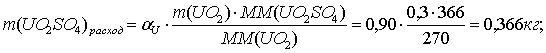
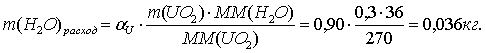
Составим таблицу материального баланса для второй реакции
Таблица 3
Материальный баланс для второй реакции
|
Приход
|
Расход
|
|
Статьи прихода
|
кг
|
Статьи расхода
|
кг
|
|
1. UO2 2. H2SO4 с избытком 3. MnO2 c избытком
|
0,3 0,2604 0,14483
|
1. UO2 остаток 2. UO2SO4 3.
H2O 4. H2SO4 остаток 5. MnSO4 6. MnO2 остаток
|
0,03 0,366 0,036 0,0651 0,1509 0,05793
|
|
Итого:
|
0,70523
|
Итого:
|
0,70593
|
Поскольку материальный баланс сошелся, значит, расчеты по второй реакции
были произведены верно.
в) третья реакция
кг
V2O5 + H2SO4 = (VO2)2SO4 + H2O (=100%).
+80 2+32+64 102+64+32+64 2+16
ММ 182 98 262 18
По реакции определим массы всех компонентов:
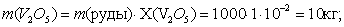
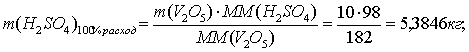
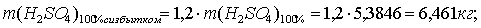
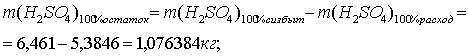
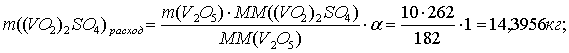
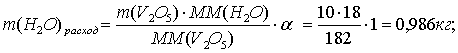
Составим таблицу материального баланса для третьей реакции.
Таблица 4
Материальный баланс для третьей реакции
|
Приход
|
Расход
|
|
Статьи прихода
|
кг
|
Статьи расхода
|
кг
|
|
1. V2O5 2. H2SO4 с избытком
|
10 6,461
|
1. (VO2)2SO4
2. H2O 3. H2SO4 остаток
|
|
Итого:
|
16,461
|
Итого:
|
16,457
|
Поскольку материальный баланс сошелся, значит, расчеты по третьей реакции
были произведены верно.
г) четвертая реакция
кг
FeO + H2SO4 = FeSO4 + H2O (=50%).
+16 2+32+64 56+32+64 2+16
ММ 72 98 152 18
По реакции определим массы всех компонентов:
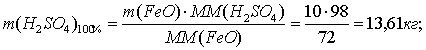
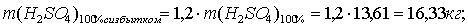
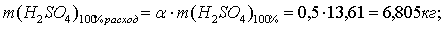
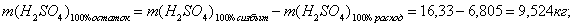
Определим
остаток FeO:
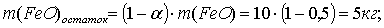
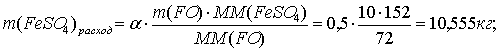
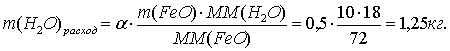
Составим таблицу материального баланса для четвертой реакции.
урановый руда выщелачивание пачук
Таблица 5
Материальный баланс для четвертой реакции
|
Приход
|
Расход
|
|
Статьи прихода
|
кг
|
Статьи расхода
|
кг
|
|
1. FeO
2. H2SO4 с избытком
|
10 16,33
|
1. FeO остаток 2.
FeSO4 3. H2O 4. H2SO4 остаток
|
5 10,555 1,25 9,524
|
|
Итого:
|
26,33
|
Итого:
|
26,329
|
Поскольку материальный баланс сошелся, значит, расчеты по четвертой
реакции были произведены верно.
д) пятая реакция
кг3 + H2SO4
= CaSO4 + H2O + CO2 (=100%).
40+12+48 2+32+64 40+32+64 2+16 12+32
ММ 100 98 136 18 44
По реакции определим массы всех компонентов:
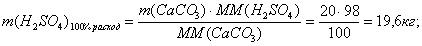

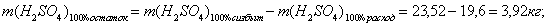
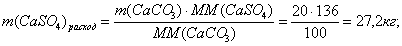
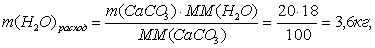
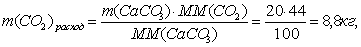
Составим таблицу материального баланса для пятой реакции.
Таблица 6
Материальный баланс для пятой реакции
|
Приход
|
Расход
|
|
Статьи прихода
|
кг
|
Статьи расхода
|
кг
|
|
1. CaCO3 2. H2SO4 с избытком
|
20 23,52
|
1. CaSO4 2. H2O
3. H2SO4 остаток 4. CO2
|
27,2 3,6 3,92 8,8
|
|
Итого:
|
43,52
|
Итого:
|
43,58
|
Поскольку материальный баланс сошелся, значит, расчеты по пятой реакции
были произведены верно.
По результатам материальных расчетов для каждой реакции составим общую
таблицу материального баланса для всего процесса в целом
Таблица 7
Общий материальный баланс
Расход
|
|
Статьи прихода
|
кг
|
%
|
Статьи расхода
|
кг
|
%
|
|
1. Руда UO3 UO2 V2O5 FeO CaCO3 Инертные (SiO2) 2. Окислитель MnO2 c избытком 3. Р-р H2SO4
H2SO4 H2O 4. Конденсат (из теплового баланса)
|
0,7 0,3 10 10 20 959 0,14483 46,8592 2296,1 195,76
|
|
1. Газ (СO2) 2. Пульпа 2.1 Твердая часть: UO3 остаток UO2
остаток MnO2 остаток FeO остаток CaSO4 Инертные (SiO2) 2.2 Растворы6 UO2SO4
MnSO4 (VO2)2SO4
FeSO4 H2SO4 остаток H2O Конденсат
|
8,8 0,07 0,03 0,05793 5 27,2 959 1,172 0,1509 14,3956
10,555 14,6574 2296,1 195,76
|
|
|
Итого:
|
3534,86
|
|
Итого:
|
3532,9
|
|
Для определения массы конденсата необходимо составить тепловой баланс.
После чего продолжить заполнение таблицы материального баланса для всего
процесса.
Так как материальный баланс сошелся, то расчеты были произведены верно.
. Тепловой баланс
Тепловой расчет сводится к составлению теплового баланса процесса
выщелачивания, расхода острого пара.
Расчет теплового баланса произведем на тонну руды. Принимаем давление
острого пара равным 3 атм.
Уравнение теплового баланса процесса выщелачивания записывается в виде:
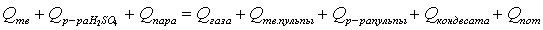 ,
,
где
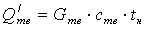 - количество тепла, поступающего в аппарат с рудой и
окислителем, Дж;
- количество тепла, поступающего в аппарат с рудой и
окислителем, Дж;
с =800 [1] -удельная теплоемкость руды, Дж/кг.К;
tн =20 - начальная температура при
входе в аппарат, 0С;
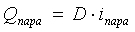 -
количество тепла, поступающего в аппарат с острым паром, Дж;
-
количество тепла, поступающего в аппарат с острым паром, Дж;
D - расход
острого пара, кг/с;
i.пара =2730 [1, с. 591]- удельная энтальпия острого пара,
кДж/кг;
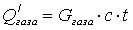 -
количество тепла, уходящего из аппарата с газом, Дж;
-
количество тепла, уходящего из аппарата с газом, Дж;
с
=838 [1]- теплоемкость газа CO2 , Дж/кг.К;
t=60-
температура процесса 0С;
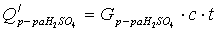 -
количество тепла, поступающего в аппарат с раствором серной кислоты, Дж;
-
количество тепла, поступающего в аппарат с раствором серной кислоты, Дж;
с =4186 [1] -теплоемкость раствора, Дж/кг.К;
t =20
- начальная температура при входе в аппарат, 0С;
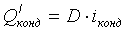 -
количество тепла, уходящего из аппарата с конденсатом острого пара, Дж;
-
количество тепла, уходящего из аппарата с конденсатом острого пара, Дж;
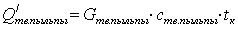 -
количество тепла, уходящего из аппарата с твердой частью пульпы, Дж;
-
количество тепла, уходящего из аппарата с твердой частью пульпы, Дж;
с
=800 [1]- теплоемкость твердой части пульпы, Дж/кг.К;
t=60-
температура процесса 0С;
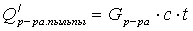 -
количество тепла, уходящего из аппарата с жидкой частью пульпы, Дж;
-
количество тепла, уходящего из аппарата с жидкой частью пульпы, Дж;
с
=4186 [1] -теплоемкость жидкой части пульпы, Дж/кг.К;
t =60 - конечная
температура при выходе из аппарата, 0С;
 - потери
тепла в аппарате, Дж.
- потери
тепла в аппарате, Дж.
Определим
составляющие уравнения теплового баланса.
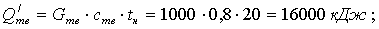
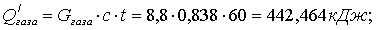


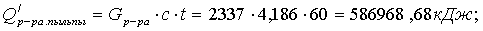
Определим
расход острого пара из уравнения теплового баланса:
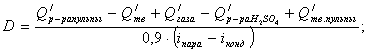
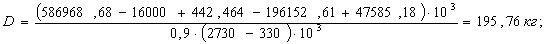
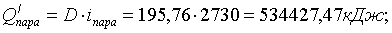
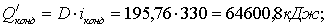
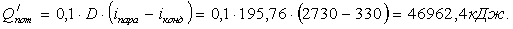
Результаты
теплового баланса сведены в таблице 8
Таблица 8
Тепловой баланс
|
Статьи прихода
|
Статьи расхода
|
|
1. С рудой и окисл. 16000 2. Р-ром серной к-ты 196152,6 3.
С остр. паром 534427,4
|
1. С пульпой жидкая 586968,68 твердая 47585,18 2. С газом
442,464 3. С конденсатом 64600,8 4. Потери 46962,4
|
|
Итого: 746580,08кДж/с
|
Итого: 746559,52кДж
|
Таким образом, видно, что тепловой баланс сошелся. Значит расчеты были
произведены верно.
5. Конструктивный расчет
В конструктивном расчете каскада пачуков определяется объем каждого из
трех аппаратов и их основные геометрические размеры.
Суммарный объем каскада пачуков определяется по формуле:
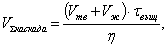
где
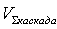 - суммарный объем каскада пачуков, м3;
- суммарный объем каскада пачуков, м3;
 - сумма
производительностей руды и окислителя, м3/с;
- сумма
производительностей руды и окислителя, м3/с;
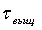 - время
выщелачивания, с;
- время
выщелачивания, с;
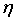 -
коэффициент заполнения аппаратов, 0,85;
-
коэффициент заполнения аппаратов, 0,85;
Определим
количество урана в 1000 кг руды:
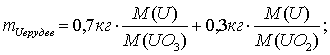
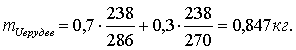
Тогда
производительность по руде определится следующим образом:
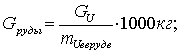

По
аналогии:
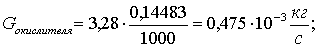
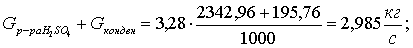
Далее,
рассчитаем объемные производительности по твердой и жидкой фазе:

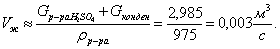
Тогда суммарный объем каскада пачуков определится:
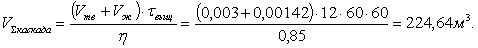
Определим
объем одного из трех одинаковых пачук:

По справочным данным выбираем ближайший стандартный пачук, характеристики
которого представлены в таблице 9.
Таблица 9
Характеристики стандартного пачука
|
D, мм
|
H, мм
|
V, м3
|
Расход воздуха, м3/(мин м3 пульпы)
|
Давление воздуха, МПа
|
|
4600
|
11300
|
120
|
0,02
|
0,3
|
Далее рассчитываем диметры патрубков, а именно:
диаметр для подачи руды и окислителя
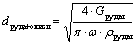

диаметр
для подачи раствора H2SO4
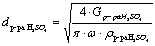
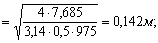
- диаметр для подачи сжатого воздуха
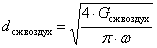
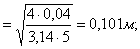
диаметр
для подачи греющего пара
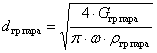
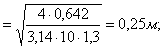
диаметр
сдувки
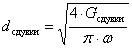
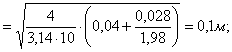
диаметр
для выхода пульпы

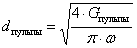
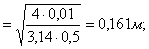
диаметр сдувки для второго и третьего аппаратов
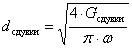

По
результатам конструктивного расчета вычерчиваем эскиз аппарата (рисунок 1А) и
каскад пачуков (рисунок 2А).
Заключение
В
ходе работы были составлен материальный и тепловой балансы, в результате
которых были определены массовые расходы всех компонентов, а также установлен
расход острого пара.
В
результате конструктивного расчета были подобраны стандартные пачуки и
определены основные характеристики аппаратов. А также выполнен эскиз одного из
каскада трех пачук и сам каскад пачуков.
Литература
1. Павлов
К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и
аппаратов химической технологии. - Л.: Химия, 1969. - 624с.
2. Плановский
А.Н., Рамм В.М., Каган С.З. Процессы и аппараты химической технологии. - Л.:
Химия, 1968. - 848 с.
Приложение А (справочное)

Рисунок 1 - Эскиз пачука с пневматическим перемешиванием
Приложение Б (справочное)
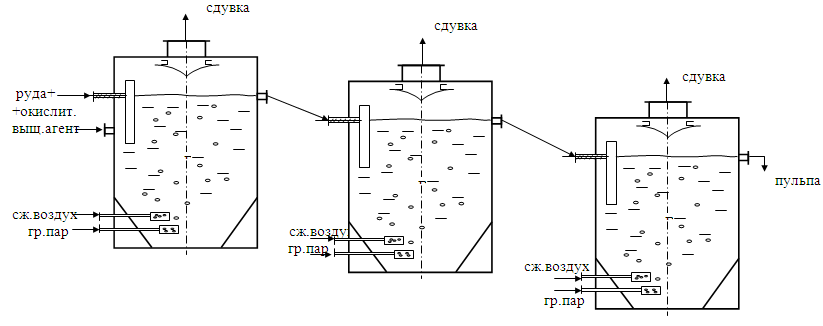
Рисунок 2 - Каскад пачуков с пневматическим перемешиванием