Основы термодинамики
Задача 1
В закрытом сосуде емкостью V=1,4
м³
содержится
воздух при давлении
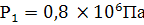 и
температуре
и
температуре 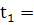 25°С(
25°С( )
В результате охлаждения сосуда, воздух, содержащийся в нем, теряет теплоту Q=130кДж.
Принимая теплоёмкость воздуха постоянной, определить давление
)
В результате охлаждения сосуда, воздух, содержащийся в нем, теряет теплоту Q=130кДж.
Принимая теплоёмкость воздуха постоянной, определить давление 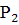 и
температуру
и
температуру , которые
установятся в сосуде после охлаждения.
, которые
установятся в сосуде после охлаждения.
Справка: К= 1,4; μ= 28,96;
 =20,93
КДж/кмоль×К;
=20,93
КДж/кмоль×К;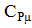 =29,31
КДж/кмоль×К
=29,31
КДж/кмоль×К
|
№
варианта
|
V,м³
|
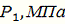
|
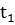  °СQ,
кДж °СQ,
кДж
|
|
|
29
|
1,8
|
0,8
|
25
|
130
|
Сосуд закрытый, значит V
- const (процесс
изохорный)
Газовая постоянная
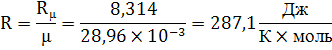
Масса газа в ёмкости из уравнения состояния газа
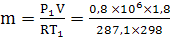 =16,8кг
=16,8кг
удельная теплоёмкост

в изохорном процессе количество теплоты
подведенной к рабочему телу равно изменению внутренней энергии: dU=Q
, отсюда:
= m(
m(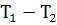 )
)
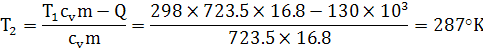
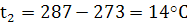
Согласно закона Шарля в изохорном процессе
отношение абсолютных давлений прямо пропорционально отношению абсолютных
температур:
 отсюда
отсюда
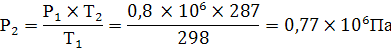
Задача 2
Какое количество теплоты необходимо
затратить, чтобы нагреть объем V=1,4 м³ воздуха при
постоянном избыточном давлении 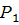
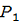 =0,8МПа(0,8×
=0,8МПа(0,8×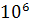 Па) от
температуры
Па) от
температуры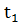
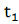 =25°С(298°К) до температуры
=25°С(298°К) до температуры 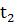
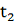 =600°С(873°К)? Какую работу при этом
совершит воздух, если барометрическое давление равно 101325 Па ?
=600°С(873°К)? Какую работу при этом
совершит воздух, если барометрическое давление равно 101325 Па ?
Справка : К= 1,4 ; μ= 28,96; 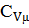
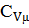 =20,93 КДж/кмоль×К ;
=20,93 КДж/кмоль×К ;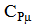
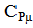 =29,31 КДж/кмоль×К
=29,31 КДж/кмоль×К
|
№
варианта
|
V,м³
|

|
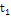 °С °С
|
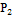 , ,
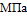
|
|
29
|
1,8
|
0,8
|
25
|
1,7
|
P=const,
процесс изобарный
Газовая постоянная
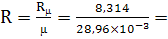 287,1
287,1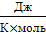
Абсолютное давление P=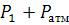 =800000+101325=901325Па
=800000+101325=901325Па
Масса газа в ёмкости из уравнения состояния
газа:
 =18,9кг
=18,9кг
удельная теплоёмкость
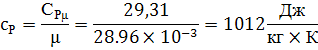
находим количество теплоты согласно выражения
для определения количества теплоты для произвольной массы газа в изобарном
процессе:
=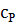 m(
m(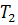 -
-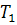 )=1012×18,9(873-298)=10,99×
)=1012×18,9(873-298)=10,99×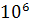 Дж
Дж
Работа в изобарном процессе:
А=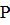 (
(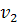 -
-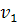 )
)
Удельный объем находим из уравнения
Менделеева-Клайперона:
=RT
Где Р - абсолютное давление
= =800000+101325=901325Па
=800000+101325=901325Па
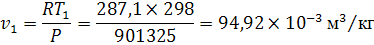

А=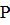 (
(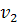 -
-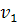 )=
)=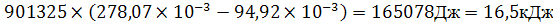
Задача 3
Воздух массой М=1,4кг с температурой 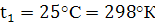 и
давлением
и
давлением  сжимается,
изотермически до конечного давления
сжимается,
изотермически до конечного давления 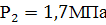 .
Определить конечный объем, затраченную работу и количество теплоты, отводимой
от воздуха.
.
Определить конечный объем, затраченную работу и количество теплоты, отводимой
от воздуха.
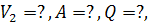
Справка: К= 1,4; μ= 28,96;
 =20,93
КДж/кмоль×К;
=20,93
КДж/кмоль×К;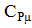 =29,31
КДж/кмоль×К
=29,31
КДж/кмоль×К
|
.№
варианта
|
М,кг
|

|
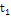 °С °С
|

|
|
29
|
1,8
|
0,8
|
1,7
|
Процесс изотермический Т=const
Газовая постоянная
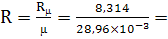 287,1
287,1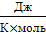
Объём найдем из уравнения состояния идеального
газа для произвольной массы
=mRT
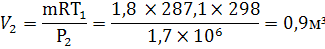
Удельный объем находим из уравнения
Менделеева-Клайперона
=RT
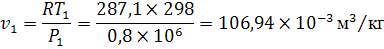
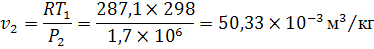
Работа в изотермическом процессе
 =
=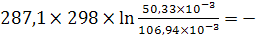 64480,55Дж
64480,55Дж
Физический смысл отрицательного значения работы
состоит в том, что не газ, а внешние силы, приложенные к газу, совершают
работу, т.е. поршень в цилиндре перемещается за счет внешнего усилия,
действующего на него.
Так как в изотермичесом процессе  ,
соответственно
,
соответственно
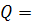 64480,55Дж
64480,55Дж
изотермический теплота работа идеальный газ
Задача 4
Воздух массой М=1,4кг при начальной температуре 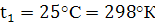 и
давлении
и
давлении  сжимается
адиабатно до конечного давления
сжимается
адиабатно до конечного давления 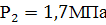 Определить
конечный объем, конечную температуру и затрачиваемую работу.
Определить
конечный объем, конечную температуру и затрачиваемую работу.
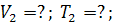 A=?
A=?
Справка: К= 1,4 ; μ= 28,96;  =20,93
КДж/кмоль×К ;
=20,93
КДж/кмоль×К ;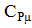 =29,31
КДж/кмоль×К
=29,31
КДж/кмоль×К
|
.№
варианта
|
М,кг
|

|
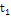 °С °С
|

|
|
29
|
1,8
|
0,8
|
25
|
1,7
|
Процесс адиабатный S=const
Газовая постоянная
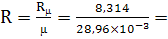 287,1
287,1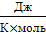
первоначальный объём находим из уравнения
состояния идеального газа для произвольной массы:
=mRT
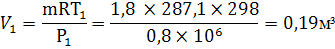
Конечный объём вычисляем из уравнения состояния
газа для адиабатного процесса


Конечную температуру вычислим из уравнения
состояния идеального газа для произвольной массы
=mRT
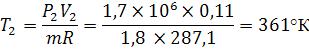
Работа в адиабатном процессе
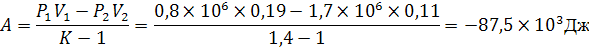
Физический смысл отрицательного значения работы
состоит в том, что не газ, а внешние силы, приложенные к газу, совершают
работу, т.е. поршень в цилиндре перемещается за счет внешнего усилия,
действующего на него.
Задача 5
Воздух массой М=1,4кг при начальной температуре 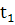 =25°С=298°К
и давлении
=25°С=298°К
и давлении 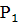 =0,8
=0,8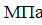 сжимается политропно при показателе политропы п=1,2 до конечного давления
сжимается политропно при показателе политропы п=1,2 до конечного давления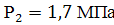 Определить конечный объем, конечную температуру и затрачиваемую работу.
Определить конечный объем, конечную температуру и затрачиваемую работу.
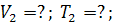 A=?
A=?
Справка: К= 1,4 ; μ= 28,96;  =20,93
КДж/кмоль×К;
=20,93
КДж/кмоль×К;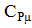 =29,31
КДж/кмоль×К
=29,31
КДж/кмоль×К
|
.№
варианта
|
М,кг
|

|
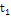
|

|
|
29
|
1,8
|
0,8
|
25
|
1,7
|
Газовая постоянная
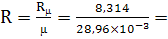 287,1
287,1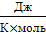
первоначальный объём находим из уравнения
состояния идеального газа для произвольной массы
=mRT
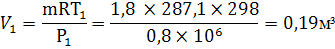
Конечный объём вычисляем из уравнения состояния
газа политропного процесса


Конечную температуру вычислим из уравнения
состояния идеального газа для произвольной массы
=mRT
Работа в адиабатном процессе