Биоорганическая химия
Задание № 1
Глобулярные и фибриллярные белки. Определение и примеры. Ответить на
вопросы: необходимо из смеси белков сконцентрировать (не нарушая нативности)
один из белков с известным значением ИЭТ. Как действовать, располагая набором
кислот, оснований и этанолом?
белок фермент витамин
гипергликемия
Глобулярные белки - белки, в молекулах которых полипептидные цепи плотно
свёрнуты в компактные шарообразные структуры - глобулы (третичные структуры
белка)
Глобулярная структура белков обусловлена гидрофобно-гидрофильными
взаимодействиями.
К глобулярным белкам относятся ферменты, иммуноглобулины, некоторые
гормоны белковой природы (например, инсулин) а также другие белки, выполняющие
транспортные, регуляторные и вспомогательные функции.
Фибриллярные белки - белки, имеющие вытянутую нитевидную структуру, в
которой соотношение продольной и поперечной осей более 1:10. Полипептидные цепи
многих фибриллярных белков расположены параллельно друг другу вдоль одной оси и
образуют длинные волокна (фибриллы) или слои.
Большинство фибриллярных белков не растворяются в воде. К фибриллярным
белкам относят например, α-кератины (на их долю приходится почти весь сухой вес
волос, белки шерсти, рогов, копыт, ногтей, чешуи, перьев), коллаген - белок
сухожилий и хрящей, фиброин - белок шёлка).
Большинство фибриллярных белков обладают особым свойством - в
формировании их пространственной структуры участвуют, кроме слабых связей,
ковалентные непептидные связи, тогда как в глобулярных белках основной вклад в
стабилизацию конформации молекулы вносят слабые нековалентные взаимодействия.
В изоэлектрической точке суммарный заряд белков, обладающих амфотерными
свойствами, равен нулю и белки не перемещаются в электрическом поле. Зная
аминокислотный состав белка, можно приближенно определить изоэлектрическую
точку (pI); pI является характерной константой белков. Изоэлектрическая точка
большинства белков животных тканей лежит в пределах от 5,5 до 7,0, что
свидетельствует о частичном преобладании кислых аминокислот. Однако в природе
имеются белки, у которых значения изоэлектрических точек лежат в крайних
значениях рН среды. В частности, величина рI пепсина (фермент желудочного сока)
равна 1, а сальмина (основной белок из молоки семги) - почти 12.
В изоэлектрической точке белки наименее устойчивы в растворе и легко
выпадают в осадок. Изоэлектрическая точка белка в сильной степени зависит от
присутствия в растворе ионов солей; в то же время на ее величину не влияет
концентрация белка.
Значение изоэлектрической точки характерно для каждого белка и зависит от
аминокислотного состава. Таким образом, меняя концентрацию водородных ионов,
можно изменить заряд белковых частиц.
Так как количество образующихся положительно и отрицательно заряженных
групп в белке зависит от рН , то имеется такое его значение (pI), названное
изоэлектрической точкой, при котором происходит компенсация разноименных
зарядов и белковая молекула, как целое , становится электронейтральной. При рН
<pI макромолекула обладает положительным суммарным зарядом и будет двигаться
к катоду, при рН>pI - отрицательным и будет двигаться к аноду. В
изоэлектрической точке все белки имеют минимальную растворимость и происходит
осаждение.
Задание № 2
Фактор стабильности белков в растворе. Ответить на вопрос:
изоэлектрическая точка гемоглобина 6,8. В каком направлении перемещаются
частицы белка в электрическом поле при рН-3,4?
Факторы стабильности белков в растворе:
. Состав п.п. цепи белка
. Преимущественное расположение гидрофильных аминокислот на поверхности
белковой глобулы. Большинство белков имеют гидрофильную поверхность.
. Наличие спирализованных участков на поверхности белка.
. Чем ниже относительная гидрофобность белков (т.е. ниже взаимодействие с
липидами, а, следовательно, между глобулами и выше сила отталкивания), тем выше
взаимодействие их с молекулами растворителя, следовательно выше растворимость.
. Растворимость белков зависит от рН среды (в изоэлектрической точке
имеют наименьшую растворимость)
. От концентрации солей: невысокая концентрация (NaCl, Na2SO4, (NH4)2SO4 -
повышает растворимость, т.к. ионы препятствуют ионному (электростатическому)
взаимодействию заряженных боковых радикалов аминокислот; высокие концентрации
солей снижают гидратацию глобулы (снимают гидратную оболочку) и тем саамы
усиливают белок-белковые взаимодействия (белок выпадает в осадок -
коагулирует).
. От размеров и формы молекул: низкомолекулярные, глобулярные белки с
большим количеством гидрофильных групп лучше растворимы в воде и слабо солевых
растворах, а фибриллярные - хуже или не растворяются.
. Денатурированные белки теряют способность к растворению.
Если среда кислая (рН < 7). Высокая концентрация H+ (водородных ионов) подавляет
диссоциацию слабой карбоксильной группы аминокислот и белки в кислой среде
приобретают заряд «+». В поле постоянного электрического поля (при
электрофорезе) белки перемещаются к катоду.
Задание № 3
Ферменты. Химическая природа и общие принципы обнаружения активности
ферментов. Перечислите четыре фактора, обуславливающие каталитическую силу
ферментов. Ответить на вопрос: перенос протона от фермента на субстрат -
нередко ключевой этап катализа.
А. Имеет ли место этот этап при катализе химотрипсином, лизоцимом и
карбоксипептидазой А?
Б. Если да, то определите донор водорода в каждом случае.
Ферменты могут иметь все четыре уровня структурной организации:
первичную, вторичную, третичную и четвертичную. Большинство ферментов имеют
четвертичную структуру.
По химической природе фермент могут быть белками простыми (ферменты
протеины) и сложными (ферменты протеиды).
Каталитическая функция ферментов определяется наличием одного или
нескольких активных центров.
Активный центр - это участок в пространственного структуре фермента, с
которым связывается субстрат и подвергается химическому превращению. Число
активных центров может быть равно числу субъединиц в четвертичной структуре
фермента, т.е. сколько субъединиц (протомеров), столько активных центров.
В активном центре условно выделяют два участка:
контактный (якорный или субстратный), отвечающий за специфичность
связывания субстрата (узнавание);
каталитический, где происходит химическое превращение субстрата после его
связывание (сначала фермент узнает субстрат, притягивает его, затем субстрат
располагается в этом активном центре.
Структурная организация фермента.
. Особенности образования активного центра у ферментов протеинов (простых
белковых ферментов).
Обычно он образован 12-16 аминокислотными остатками полипептидной цепи.
Иногда их число больше. Аминокислоты, формирующие активный центр, находятся в
разных местах полипептидной цепи. При пространственной укладки белка-фермента
(в третичную структуру), они сближаются и образуют активный центра.
Приблизительно 1/2 - 1/3 аминокислот фермента прямо или косвенно
участвуют в работе активного центра.
. Особенности образования активного центра у ферментов-протеидов (сложных
белков-ферментов).
Протеиды состоят из:
Апофермент (белковая часть) + кофактор (небелковая часть) = холофермент
(активный комплекс).
Кофактор (или простетическая группа) чаще всего предствавлен витаминами
или ионами металлов.
Холофермент в диссоциированном состоянии неактивен.
У ферментов-протеидов главную роль в катализе играют кофакторы, а боковые
радикалы аминокислот и их функциональные группы в апоферменте отвечают за
специфичность связывания с субстратом и регуляторами (активаторами и ингибиторами)
Таким образом, якорный участок активного центра и регуляторные центры находятся
в апоферменте.
Кинетика ферментативных реакций - этот раздел энзимологии изучает
зависимость скорости ферментативной реакции от условий взаимодействий субстрата
с ферментом (в том числе от факторов среды). Основы были заложены в работах
Михаэлиса и Ментен.
Скорость ферментативной реакции определяется количеством вещества
(субстрата), которое превращается в единицу времени.
Скорость является мерой способности фермента катализировать реакцию и
обозначается как активность фермента.
Измерить активность фермента можно только косвенно: по концентрации
превращаемого субстрата или нарастанию концентрации продукта в единицу времени.
Скорость ферментативной реакции зависит от:
. концентрации субстрата;
. концентрации фермента;
. реакции характера рН-среды;
. температуры
Зависимость скорости ферментативной реакции от температуры.
В определенном ограниченном интервале температур скорость ферментативной
реакции увеличивается с ростом температуры. Повышение скорости реакции по мере
приближения к оптимальной температуре (от 0 до 40 °С) объясняется увеличением
кинетической энергии реагирующих молекул. При дальнейшем увеличении температуры
кинетическая энергия молекулы фермента становиться достаточной для разрыва
связей, поддерживающих вторичную, третичную и четвертичную структуру фермента в
нативном состоянии. Это приводит к тепловой денатурации фермента.
При низкой температуре происходит обратимая инактивация фермента, т.к.
наблюдаются незначительные изменения конформации активного центра фермента.
Фермент имеет белковую природу, поэтому температура на него, влияет также
как на белок (повышении температуры приводит к денатурации).
Задание № 4
Виды иммобилизации ферментов (не менее трех препаратов), принципы
иммобилизации, практическое применение данных препаратов.
Иммобилизованные ферменты, препараты ферментов, молекулы которых связаны
с матрицей, или носителем (как правило, полимером), сохраняя при этом полностью
или частично свои каталитические свойства. Иммобилизованные ферменты обычно не
растворимы в воде; между двумя фазами возможен обмен молекулами субстрата,
продуктов каталитич. р-ции, ингибиторов и активаторов. Существует неск. осн.
способов иммобилизации ферментов: 1) путем образования ковалентных связей между
ферментом и матрицей; 2) полимеризацией мономера, образующего матрицу, в
присут. фермента, к-рый при этом оказывается включенным в сетку полимера -
обычно геля; 3) благодаря электростатич. взаимод. противоположно заряженных
групп фермента и матрицы; 4) сополимеризацией фермента и мономера, образующего
матрицу; 5) связыванием фермента и матрицы в результате невалентных взаимод. -
гидрофобных, с образованием водородных связей и др.; 6) инкапсулированием -
созданием около молекул фермента полупроницаемой капсулы, напр., включением
фермента в липосомы; 7) сшиванием молекул фермента между собой, напр.,
глутаровым альдегидом, диметиловым эфиром диимида адипиновой к-ты. Особый
случай иммобилизации проведение ферментативных р-ций в двухфазной системе,
когда фермент находится в водной фазе, а субстраты и продукты р-ции
распределяются между орг. и водной фазами, что позволяет в зависимости от коэф.
распределения в-в между фазами сдвигать равновесие р-ции в нужную сторону;
диспергирование фаз увеличивает пов-сть их раздела и тем самым улучшает доступ
субстрата к ферменту. Среди способов иммобилизации наиб. распространение
получили ковалентное связывание фермента с матрицей и включение фермента в
гель. В первом случае в качестве матрицы обычно используют целлюлозу,
декстрановые гели (сефароэу, агарозу), микропористые стекла или кремнеземы, а
также синтетич. полимеры. Матрицу при ковалентной иммобилизации ферментов
обычно предварительно активируют, обрабатывая, напр., бромцианом, азотистой
к-той или цианурхлоридом. Благодаря этому она становится носителем активных
группировок, к-рые способны вступать в р-цию сочетания, взаимод. с группами
NH2, ОН, СООН. Во втором случае в качестве гелеобразующего полимера используют
полиакриламид. На практике иммобилизация часто осуществляется одновременно
неск. способами. Так, при фиксации ферментов ковалентными связями между их
молекулами и матрицей обычно возникают также нековалентные взаимодействия.
Известны способы предварит. хим. модификации молекул фермента низкомол. в-вами
или р-римыми полимерами, имеющими заряженные группировки, что изменяет у таких
модифицир. белков электростатич. заряд молекулы и позволяет достаточно прочно
сорбировать их на ионообменных смолах. При всех типах иммобилизации матрица,
взаимодействуя с ферментом, может инактивировать последний или создавать
пространств. затруднения для доступа субстрата к активному центру. При
ковалентном связывании фермента для предотвращения отрицат. влияния матрицы
между ней и молекулой фермента вводят разобщающую цепь атомов - спейсер (наз.
также «вставкой» или «ножкой»). Кроме того, часто стремятся использовать для
иммобилизации гидрофильные матрицы, создающие вблизи фермента более естеств.
микроокружение. При иммобилизации ферментов необходимо, чтобы активные группы
матрицы не блокировали каталитич. центр фермента, а условия иммобилизации не
приводили к потере его активности. Определенные ограничения на способ
иммобилизации налагают и особенности субстрата. Так, в случае высокомол.
субстратов нельзя использовать методы инкапсулирования или включения фермента в
гель. Если матрица несет на себе заряды, то заряд субстрата влияет на кинетич.
параметры р-ции: разноименные заряды на носителе и субстрате увеличивают
скорость р-ции, катализируемой иммобилизованными ферментами, одноименные заряды
ее снижают и м. б. причиной полной потери активности препарата. Заряды носителя
и субстрата влияют также на величину рН, при к-рой скорость ферментативной
р-ции максимальна. Важную роль играет распределение субстрата между фазами
иммобилизованного фермента и р-ра. Ограниченная доступность субстрата к
активному центру фермента может привести к изменению специфичности последнего.
Особенно это Характерно для высокомол. субстратов, к-рые из-за малого коэф.
диффузии медленно переходят в фазу иммобилизованного фермента, что приводит к
относит. увеличению скоростей др. р-ций с участием субстратов меньших размеров.
В нек-рых случаях возможно также изменение направления р-ции. Так, фермент
эндополигалактуроназа, катализирующий расщепление полигалактуроновой к-ты в
середине молекулы, после иммобилизации отщепляет низкомол. фрагменты от концов
молекулы. Существ. влияние на кинетику р-ций, катализируемых иммобилизованными
ферменами, оказывают два диффузионных барьера - внешний и внутренний. Первый
обусловлен наличием тонкого неперемешиваемого слоя р-рителя вокруг частицы
иммобилизованного фермента (слоя Нернста). Толщина этого слоя зависит от
скорости перемешивания. Поэтому увеличение последней или скорости тока р-ра в
колонке с иммобилизованным ферментом увеличивает скорость ферментативной р-ции.
Внутр. диффузионный барьер возникает вследствие ограничения своб. диффузии
субстрата внутри сетки полимерной матрицы. Иммобилизация ферментов создает ряд
преимуществ. К ним относятся: более высокая стабильность ферментных препаратов,
возможность их удаления из реакц. среды и его повторного использования, а также
возможность создания непрерывных процессов на ферментных колонках. Важное
значение имеет относит. стабильность иммобилизованных ферментов к
денатурирующим воздействиям - нагреванию, действию агрессивных сред, автолизу и
др. Последнему подвержены протеолитич. ферменты. Иммобилизация разобщает
молекулы этих ферментов и полностью исключает такой процесс. Благодаря этому
удалось изучить механизм образования протеолитич. фермента пепсина из его
предшественника пепсиногена (при этом от последнего отщепляется пептид,
состоящий из 42 аминокислотных остатков). Было показано, что эта р-ция
катализируется самим пепсином. Иммобилизованные ферменты применяют в произ-ве
L-аминокислот, 6-аминопенициллановой к-ты, из к-рой получают полусинтетич.
пенициллины, в синтезе преднизолона, для удаления лактозы из продуктов питания,
используемых больными с лактазной недостаточностью, в изготовлении ферментных
электродов для экспресс-определения мочевины, глюкозы и др. в-в, для создания
аппаратов «искусств. почка» и «искусств. печень», для удаления эндотоксинов,
образующихся в процессе заживления ран и ожогов, при лечении нек-рых онкологии,
заболеваний и др. Большое значение приобрели в клинич. и лаб. практике
иммуноферментные методы анализа, в к-рых также используются иммобилизованные
ферменты.
Задание №
5
Витамин В. Общие представления о строении витамина, его коферментные
формы, три примера участия их в биохимических реакциях.
Витамин В1 впервые выделен в кристаллическом виде Функом.
Суточная потребность - 1-3 мг.
Распространение в природе. Хлеб грубого помола, горох, фасоль, мясные
продукты. В кисло среде В1 стоек к нагреванию и кипячению, но легко разрушается
при нагревании в нейтральной и щелочной среде. Вследствие этого, В1, мало
разрушается при обработке пищевых продуктов теплом, например при варке пищи или
выпечке хлеба, но чрезвычайно быстро разрушается при выпечке мучных
кондитерских изделий с использованием щелочных разрыхлителей (сода или
углекислый аммоний).
Структура витамина и кофактора. В пищеварительном тракте на путь
всасывания в кровь, встает свободный тиамин. Всасывание осуществляется простой
диффузией. В печени и других тканях тиамин фосфорилируется с участием
тиаминфосфокиназы до ТМФ, ТДФ, ТГФ. Тиаминдифосфат в клетках связывается с
соответствующим апоферментом:

Ферментативные реакции с участием тиамина
Все известные реакции, зависимые от тиаминдифосфата, могут быть
составлены из пяти полуреакций (а-е на рис. 1), каждая из которых является α-расщеплением, приводящим к
образованию связанного с тиамином «активного альдегида» (центральная часть рис.
1), который идентичен соединению, изображенному в левой части уравнения.
Декарбоксилирование α-кетокислоты до альдегида представлено стадией б с
последующей реакцией в направлении, обратном стадии а. Наиболее изученным
ферментом, катализирующим реакцию этого типа, является пируватдекарбоксилаза
дрожжей.
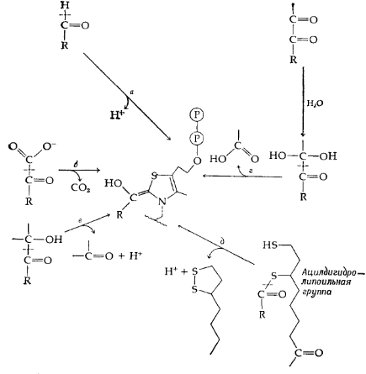
Рис. 1. Полуреакции, составляющие тиаминзависимые реакции α-расщепления и α-конденсации
Образование α-кетолов из α-кетокислот также начинается со стадии
б, за которой следует конденсация с другим карбонильным соединением, осуществляемая
обращением стадии в. Хорошо известным примером такой реакции служит синтез α-ацетолактата

в котором сочетаются декарбоксилирование пирувата и конденсация
образующегося активного ацетальдегида с другой молекулой пирувата. Эта реакция
катализиурется ацетолактатсинтетазой, которую иногда именуют «карбо-лиазой».
Ацетолактат служит предшественником валина и лейцина. Сходная кетольная
конденсация необходима и в биосинтезе изолейцина. Ацетолактат является
Рис. 2. Расщепление α-кетола до альдегида и карбоновой
кислоты; последовательность реакций, сопряжения с фосфорилированием ADP
β-кетокислотой и легко
декарбоксилируется в ацетоин; эта реакция имеет важное значение при некоторых
видах бактериального брожения. Кетольная конденсация двух молекул глиоксилата с
декарбоксилированием катализируется глиоксилат-карболигазой.
Стадия д на рис. 1 представляет собой реакцию расщепления производного
ацилгидролипоата. Реакция обычно протекает в обратном направлении и является
частью процесса окислительного декарбоксилирования α-кетокислоты, который начинается
стадией б.
Важное значение имеет реакция расщепления α-кетолов, в которой используется
стадия в с последующим обращением этой же стадии, но с другим акцептором
альдегида.
Эту реакцию катализирует транскетолаза - фермент, необходимый в
пентозофосфатных путях метаболизма и в фотосинтезе. Родственная реакция (рис.
2), которая имеет более сложный механизм, катализируется ферментом
фосфокетолазой; эта реакция играет важную роль в энергетическом метаболизме
некоторых бактерий. Продуктом реакции, катализиуремой фосфокетолазой, является
ацетилфосфат, расщепление которого может быть сопряжено с синтезом АТР.
Задание № 6
Виды РНК. Транскрипция, характеристика компонентов системы и механизма
синтеза РНК. Ответить на вопрос: специалист по химии белка сказал молекулярному
генетику, что он нашел новый мутантный гемоглобин, в котором аспартат замещает
лизин. Молекулярный генетик удивился и попросил проверить результат.
А. Почему молекулярный генетик удивился и выразил сомнения в возможности
такой аминокислотной замены?
Б. Какая аминокислотная замена показалась бы молекулярному генетику
приемлемой?
Виды РНК
Матричная (информационная) РНК - РНК, которая служит посредником при
передаче информации, закодированной в ДНК к рибосомам, молекулярным машинам,
синтезирующим белки живого организма. Кодирующая последовательность мРНК
определяет последовательность аминокислот полипептидной цепи белка. Однако
подавляющее большинство РНК не кодируют белок. Эти некодирующие РНК могут
транскрибироваться с отдельных генов (например, рибосомальные РНК) или быть
производными интронов. Классические, хорошо изученные типы некодирующих РНК -
это транспортные РНК (тРНК) и рРНК, которые участвуют в процессе трансляции.
Существуют также классы РНК, ответственные за регуляцию генов, процессинг мРНК
и другие роли. Кроме того, есть и молекулы некодирующих РНК, способные
катализировать химические реакции, такие, как разрезание и лигирование молекул
РНК. По аналогии с белками, способными катализировать химические реакции -
энзимами (ферментами), каталитические молекулы РНК называются рибозимами.
Информация о последовательности аминокислот белка содержится в мРНК. Три
последовательных нуклеотида (кодон) соответствуют одной аминокислоте. В
эукариотических клетках транскирибированный предшественник мРНК или пре-мРНК
процессируется с образованием зрелой мРНК. Процессинг включает удаление
некодирующих белок последовательностей (интронов). После этого мРНК
экспортируется из ядра в цитоплазму, где к ней присоединяются рибосомы,
транслирующие мРНК с помощью соединённых с аминокислотами тРНК.
В безъядерных клетках (бактерии и археи) рибосомы могут присоединяться к
мРНК сразу после транскрипции участка РНК. И у эукариот, и у прокариот цикл
жизни мРНК завершается её контролируемым разрушением ферментами рибонуклеазами
[29].
Транспортные (тРНК) - малые, состоящие из приблизительно 80 нуклеотидов,
молекулы с консервативной третичной структурой. Они переносят специфические
аминокислоты в место синтеза пептидной связи в рибосоме. Каждая тРНК содержит
участок для присоединения аминокислоты и антикодон для узнавания и
присоединения к кодонам мРНК. Антикодон образует водородные связи с кодоном,
что помещает тРНК в положение, способствующее образованию пептидной связи между
последней аминокислотой образованного пептида и аминокислотой, присоединённой к
тРНК.
Рибосомальные РНК (рРНК) - каталитическая составляющая рибосом.
Эукариотические рибосомы содержат четыре типа молекул рРНК: 18S, 5.8S, 28S и
5S. Три из четырёх типов рРНК синтезируются в ядрышке. В цитоплазме
рибосомальные РНК соединяются с рибосомальными белками и формируют
нуклеопротеин, называемый рибосомой[29]. Рибосома присоединяется к мРНК и
синтезирует белок. рРНК составляет до 80 % РНК, обнаруживаемой в цитоплазме
эукариотической клетки [33].
Необычный тип РНК, который действует в качестве тРНК и мРНК (тмРНК)
обнаружен во многих бактериях и пластидах. При остановке рибосомы на дефектных
мРНК без стоп-кодонов тмРНК присоединяет небольшой пептид, направляющий белок
на деградацию.
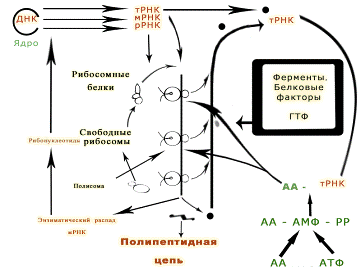
Роль разных типов РНК в синтезе белка (по Уотсону)
Транскри́пция - процесс синтеза РНК с использованием ДНК в качестве
матрицы, происходящий во всех живых клетках. Другими словами, это перенос
генетической информации с ДНК на РНК.
Транскрипция катализируется ферментом ДНК-зависимой РНК-полимеразой.
Процесс синтеза РНК протекает в направлении от 5'- к 3'- концу, то есть по
матричной цепи ДНК РНК-полимераза движется в направлении 3'->5'
Транскрипция состоит из стадий инициации, элонгации и терминации.
Инициация транскрипции
Инициация транскрипции - сложный процесс, зависящий от последовательности
ДНК вблизи транскрибируемой последовательности (а у эукариот также и от более
далеких участков генома - энхансеров и сайленсеров) и от наличия или отсутствия
различных белковых факторов.

Рис. 4. Транскрипция (схема). Бледно розовый - ДНК; темно-розовый - РНК;
зеленый, голубой, сине-зеленый - субъединицы РНК-полимеразы.
Элонгация транскрипции
Момент перехода РНК-полимеразы от инициации транскрипции к элонгации
точно не определен. Три основных биохимических события характеризуют этот
переход в случае РНК-полимеразы кишечной палочки: отделение сигма-фактора,
первая транслокация молекулы фермента вдоль матрицы и сильная стабилизация
транскрипционного комплекса, который кроме РНК-полимеразы включает растущую
цепь РНК и транскрибируемую ДНК. Эти же явления характерны и для РНК-полимераз
эукариот. Переход от инициации к элонгации сопровождается разрывом связей между
ферментом, промотором, факторами инициации транскрипции, а в ряде случаев -
переходом РНК-полимеразы в состояние компетентности в отношении элонгации
(например, фосфорилирование CTD-домена у РНК-полимеразы II). Фаза элонгации
заканчивается после освобождения растущего транскрипта и диссоциации фермента
от матрицы (терминация).
На стадии элонгации в ДНК расплетено примерно 18 пар нуклеотидов.
Примерно 12 нуклеотидов матричной нити ДНК образует гибридную спираль с
растущим концом цепи РНК. По мере движения РНК-полимеразы по матрице впереди
нее происходит расплетание, а позади - восстановление двойной спирали ДНК.
Одновременно освобождается очередное звено растущей цепи РНК из комплекса с
матрицей и РНК-полимеразой. Эти перемещения должны сопровождаться относительным
вращением РНК-полимеразы и ДНК. Трудно себе представить, как это может
происходить в клетке, особенно при транскрипции хроматина. Поэтому не
исключено, что для предотвращения такого вращения двигающуюся по ДНК
РНК-полимеразу сопровождают топоизомеразы.
Элонгация осуществляется с помощью основных элонгирующих факторов ,
необходимых, чтобы процесс не останавливался преждевременно.
Молекулярная патология гемоглобина
При обследовании больных с симпнтомами серповидноклеточной анемии, а
также при проведении электрофоретического анализа гемоглобинов здоровых людей
было обнаружено более 100 аномальных гемоглобинов. В северной Европе
гетерозиготность по варианту гемоглобина А встречается у 1 человека из 300.
Частота любого из мутантных аллелей обычно составляет менее 10-4; это на
несколько порядков ниже, чем частота гена серповидноклеточности в районах,
эндемичных по малярии. Другими словами, большинство аномальных гемоглобинов не
дает организму никаких преимуществ в естественном отборе. Как правило, наличие
аномальных гемоглобинов либо никак не влияет на здоровье человека, либо
оказывается пагубным.
В состав молекулы гемоглобина человека входят две a-цепи (a-цепь
закодирована в 16-ой хромосоме) и две b-цепи (b-цепь закодирована в 11-ой
хромосоме). В состав b-цепи входит 146 аминокислотных остатков, при этом в
нормальной b-цепи шестым аминокислотным остатком является глутаминовая кислота.
С участием нормальной b-цепи образуется нормальный гемоглобин - HbA. В
нетранскрибируемой нити участка ДНК, кодирующего b-цепь, глутаминовая кислота
закодирована триплетом ГАА. Если же в результате мутации в ДНК произойдет
замена триплета ГАА на триплет ГТА, то на месте глутаминовой кислоты в молекуле
гемоглобина в соответствии с генетическим кодом появится валин. В итоге вместо
гемоглобина HbA появится новый гемоглобин - HbS. Такая замена всего лишь одного
нуклеотида и одной аминокислоты приводит к развитию тяжелого заболевания -
серповидноклеточной анемии.
Различают несколько типов аномальных гемоглобинов.
. Изменена наружная часть молекулы. Почти все замены аминокислот на поверхности
молекулы гемоглобина безвредны. Гемоглобин S представляет собой поразительное исключение.
. Изменен активный центр. В этом случае в дефектной субъединице не
происходит связывания кислорода, так как структурные изменения вблизи гемма
непосредственно влияют на связывание кислорода.
. Изменена третичная структура. Замена аминокислот препятствует
возникновению нормальной конформации молекулы. Такие гемоглобины обычно
нестабильны.
. Изменена четвертичная структура. Некоторые мутации, затрагивающие участки
области контактов, приводят к потере аллостерических свойств. В результате
нарушается сродство таких гемоглобинов к О2.
В результате некоторых мутаций гемоглобины утрачивают стабильность из-за
деформаций третичной структуры
Замены аминокислот в отдаленных от гемма участках могут препятствовать
возникновению нормальной конформации гемоглобина и тем самым резко нарушать его
функцию. Большой интерес в этом отношении представляет гемоглобин Riverdale-Bronx, у которого в положении В6 вместо глицина стоит аргинин.
Из-за больших размеров аргинин не умещается в том узком пространстве, в котором
должны пересекаться спирали В и Е (рис. 3). Действительно, во всех нормальных
гемоглобинах и миоглобинах положение В6 всегда занято глицином. Гемоглобин Riverdale-Bronx в результате произошедшей аминокислотной заметы
оказывается нестабильным.
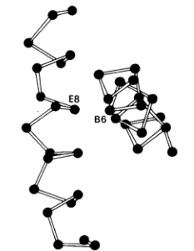
Рис. 3. Молекула гемоглобина принимает нормальную структуру, только если
в положении В6 стоит остаток глицина. Поскольку именно в этом участке перекрещиваются
спирали В и Е, для большей, чем у глицина, боковой цепи нет места.
Клиническая картина талассемии может возникать при аминокислотных заменах
с образованием нестабильных гемоглобинов, при мутациях в терминирующем кодоне,
приводящих к синтезу аномально длинных цепей гемоглобина (например, при
гемоглобинопатий Constant Spring ) или при слиянии генов дельта- и бета-цепей,
приводящих к синтезу аномально коротких цепей гемоглобина (например, при
гемоглобинопатий Lepore ). При гемоглобинопатий E точечная мутация не только
приводит к замене аминокислоты, но и нарушает сплайсинг транскрипта.
Цепи глобина принято обозначать греческими буквами, а мутации - буквами в
верхнем регистре. Например, A в верхнем регистре используется для обозначения
нормального гемоглобина, а относительно широко распространенный гемоглобин S
нередко обозначается как бета с буквой s в верхнем регистре. Чаще, однако,
указывается, какая замена аминокислоты произошла, и тогда гемоглобин S
обозначается как бета(6Глу-Вал), при этом, естественно (6Глу-Вал) находится в
верхнем регистре.
Задание № 7
Репликация ДНК-механизм, основные этапы. Ферменты и механизм репарации
ДНК. Ингибиторы репликации как противоопухолевые и противовирусные препараты,
их механизмы действия (привести не менее 5 примеров). Ответить на вопрос: какой
результат получили бы Мезельсон и Сталь, если бы репликация была бы
консервативной. Укажите предполагаемое распределение молекул ДНК после 1-й и
2-й генераций в случае консервативной репликации (т.е. когда родительская
двойная спираль не расходится)?
Реплика́ция ДНК - это процесс синтеза дочерней молекулы
дезоксирибонуклеиновой кислоты, который происходит в процессе деления клетки на
матрице родительской молекулы ДНК. При этом генетический материал,
зашифрованный в ДНК, удваивается и делится между дочерними клетками. Репликацию
ДНК осуществляет фермент ДНК-полимераза.
Хеликаза, топоизомераза и ДНК-связывающие белки расплетают ДНК,
удерживают матрицу в разведённом состоянии и вращают молекулу ДНК. Правильность
репликации обеспечивается точным соответствием комплементарных пар оснований и
активностью ДНК-полимеразы, способной распознать и исправить ошибку. Репликация
у эукариот осуществляется несколькими разными ДНК-полимеразами. Далее
происходит закручивание синтезированных молекул по принципу суперспирализации и
дальнейшей компактизации ДНК. Синтез энергозатратный.
Цепи молекулы ДНК расходятся, образуют репликационную вилку, и каждая из
них становится матрицей, на которой синтезируется новая комплементарная цепь. В
результате образуются две новые двуспиральные молекулы ДНК, идентичные
родительской молекуле.
Каждая молекула ДНК состоит из одной цепи исходной родительской молекулы
и одной вновь синтезированной цепи. Такой механизм репликации называется
полуконсервативным. В настоящее время этот механизм считается доказанным
благодаря опытам Мэтью Мезельсона и Франклина Сталя (1958 г.). Ранее
существовали и две другие модели: «консервативная» - в результате репликации
одна молекула ДНК состоит только из родительских цепей, а другая - только из
дочерних цепей; «дисперсионная» - все получившиеся в результате репликации
молекулы ДНК состоят из цепей, одни участки которых вновь синтезированы, а
другие взяты из родительской молекулы ДНК).
Процесс редупликации: раскручивание спирали молекулы - отделение одной
цепи от другой на части молекулы ДНК - воздействие фермента ДНК-полимеразы на
молекулу - присоединение к каждой цепи ДНК комплементарных нуклеотидов -
образование двух молекул ДНК из одной.
Ингибиторы репликации - противоопухолевые препараты
Антибиотики, взаимодействующие с ДНК, нарушают её матричную функцию и
вызывают подавление процессов репликации и транскрипции. Их используют для
лечения злокачественных новообразований и называют противоопухолевыми
препаратами (см. раздел 15). Дауномицин, доксорубицин и некоторые другие
взаимодействуют с молекулой ДНК таким образом, что циклическая структура этих
антибиотиков встраивается («интеркалирует») между парами оснований G≡C, а
углеводный компонент занимает малую бороздку ДНК (рис. 4-43). Это ведёт к
локальному изменению структуры ДНК и ингибированию репликации и транскрипции.
К «интеркаляторам» относят также антибиотик актиномицин D, блокирующий
синтез ДНК и РНК у про- и эукариотов. Это соединение слишком токсично, чтобы
использовать его в клинических целях, но его широко используют в
научно-исследовательской работе для изучения процессинга первичных транскриптов
РНК.
Избирательность действия противоопухолевых антибиотиков невелика и
обеспечивается более высокой по сравнению с нормальными клетками скоростью
синтеза ДНК и РНК, а также повышенной проницаемостью клеточных мембран
опухолевых клеток. В то же время эти соединения токсичны для быстроделящихся
нормальных клеток организма, таких как стволовые клетки кроветворной системы,
клетки слизистой оболочки желудка и кишечника, фолликулов волос. В последние
годы проводятся исследования по созданию препаратов, обеспечивающих доставку
ингибитора только в опухолевые клетки. Это достигается связыванием
цитотоксических антибиотиков с белками, рецепторы к которым имеются главным
образом на опухолевых клетках.
К препаратам, останавливающим репликацию, относят алкилирующие агенты и
ингибиторы ДНК-топоизомеразы II (одной из изоформ топоизомераз). Последние
называют ингибиторами гираз, поскольку ДНК-гиразы - ферменты прокариотических
клеток, ответственные за суперспира-лизацию ДНК; у эукариотов аналогичную
функцию выполняют ДНК-топоизомеразы. Известно, что транскрипция некоторых генов
возможна лишь при определённом уровне суперспирализации матрицы. Соединения,
вмешивающиеся в работу ДНК-гираз, могут ингибировать или активировать синтез
РНК. К ингибиторам гираз принадлежат налидиксовая кислота, новобиоцин и
номермицин.
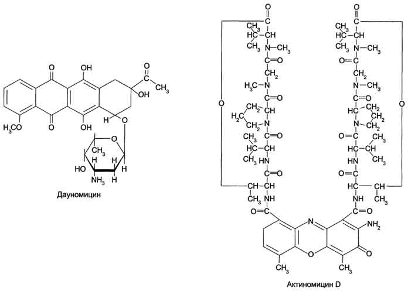
Рис. 5. Строение «интеркаляторов» - дауномицина и актиномицина D
Задание № 8
Дегидрирование субстратов как источник энергии для синтеза АТФ.
Дыхательный контроль. Найдите соответствие.
|
А. Цитохром в
|
а) способен в
восстановленном состоянии связывать молекулярный кислород и ускорять реакции
гидроксилирования ароматических соединений;
|
|
Б. Цитохром с
|
б) имеет максимум
поглощения при длине волны 600 нм и молекулярную массу равну 240000;
|
|
В. Цитохром а
|
в) открывает ансамбль
цитохромов в цепи оксидоредуктах, обеспечивающих сопряжение биологического
окисления с фосфорилированием АДФ;
|
|
Г. Цитохром а3
|
г) представлен белком с
молекулярной массой 13000 и полностью выясненной первичной, вторичной и
третичной структурами
|
|
Д. Цитохром Р450
|
д) завершает
оксидоредуктазный комплекс митохондрий, обеспечивая активирование молекулярного
кислорода
|
|
А. Цитохром в
|
в
|
|
Б. Цитохром с
|
|
В. Цитохром а
|
б
|
|
Г. Цитохром а3
|
д
|
|
Д. Цитохром Р450
|
а
|
Задание № 9
ЦТК-химизм промежуточных реакций, ферменты. Биороль ЦТК. Почему продукт
окисления изоцитрата декарбоксилируется, а сам он - нет? Какое значение для ЦТК
имеет анаплеротическая реакция? Будет ли происходить накопление оксалоацетата,
если к экстракту, содержащему ферменты ЦТК, добавить ацетил-КоА?
Ци́кл трикарбо́новых кисло́т (цикл Кре́бса, цитра́тный цикл) - центральная часть общего
пути катаболизма, циклический биохимический аэробный процесс, в ходе которого
происходит превращение двух- и трёхуглеродных соединений, образующихся как
промежуточные продукты в живых организмах при распаде углеводов, жиров и
белков, до CO2. При этом освобождённый водород направляется в цепь тканевого
дыхания, где в дальнейшем окисляется до воды, принимая непосредственное участие
в синтезе универсального источника энергии - АТФ.
Цикл Кребса - это ключевой этап дыхания всех клеток, использующих
кислород, центр пересечения множества метаболических путей в организме. Кроме
значительной энергетической роли циклу отводится также и существенная
пластическая функция, то есть это важный источник молекул-предшественников, из
которых в ходе других биохимических превращений синтезируются такие важные для
жизнедеятельности клетки соединения как аминокислоты, углеводы, жирные кислоты
и др.
Реакции цикла Кребса:
этап. Конденсация щавелевоуксусной кислоты и ацитил ~ SKoA идет с участием цитратсинтазы на
образование ковалентной связи затрачивается энергия макроэгической связи Ацитил
~ SKoA. Образуется цитрат (цитрил~ SKoA - промежуточный метаболизм 1-го
этапа).
этап. Фермент алонитатгидратаза сначала катализирует реакцию
дегидротации, а затем гидратации. В результате лимонная кислота переходит в
изолимонную.
этап. Окислительно-восстановительная реакция. Изоцетрат подвергается
процессу дегидрирования (окисления) при участии НАD+-зависимой изоцитратдегидрогеназы. Одновременно идет реакция
прямого декарбоксилирования промежуточного продукта оксалосукцината. Таким
образом изоцитрат - это первый субстрат окисления цикла Кребса, который отдает
атом водорода в дыхательную цепь.
В р-ции 3, катализируемой НАД- или НАДФ-зависимой
изоцитратдегидрогеназой, происходит дегидрирование изо-цитрата при атоме С-2 с
одновременным декарбоксили-рованием и образованием 2-оксоглутарата и СО2.
Бактерии содержат НАДФ-зависимую изоцитратдегидрогеназу, активность к-рой
регулируется хим. модификацией - фосфо-рилированием (инактивация) и
дефосфорилированием (активация) при участии бифункцион. фермента
изоцитратдегид-рогеназа-киназа (фосфатаза), играющего существ. роль в
переключении обмена с трикарбоновых кислот цикла на анаплеротич. («возмещающий»
образование промежут.

Эукариоты содержат обе формы изоцитрат-дегидрогеназы. Активность
НАДФ-зависимого фермента, локализованного в митохондриальном матриксе и
цитозоле, контролируется продуктами р-ции. Активность НАД-зави-симой
изоцитратдегидрогеназы, локализованной исключительно в митохондриальном
матриксе, активируется у грибов аденозинмонофосфатом (АМФ) и цитратом, у
животных - аденозиндифосфатом (АДФ), цитратом и ионами Са2+.
этап. Реакция окислительного декарбоксилирования α-кетоглутаровой кислоты. Механизм
реакции идентичен реакции окислительного декарбоксилирования пирувата.
Участвуют в реакции пять кофакторов, α-кетоглуторат (второй субстрат
окисления) ДГ отличается от пируватдегидрогеназы - апоферментом.
этап. Реакция субстратного фосфорилирования. Энергия макроэргической
тиоэфирной связи в молекуле субстрата - сукцинил~ SKoA - разрывается и аккумулируется в макроэргические
фосфатные связи ГТФ, а затем АТФ (фермент сукцинаттиоксидаза). Это единственная
молекула ГТФ (АТФ), которая образуется непосредственно в цикле Кребса, а не в
дыхательной цепи.
Преварщение ГТФ в АТФ идет с помощью фермента нуклеозиддифосфаткиназы ГТФ
+ АДФ «=« АТФ + ГТФ
этап. Окислительно-восстановительная реакция. Сукцинат подвергается
процессу дегидрирования (окислению) при участии ФАД - зависимой сукцинатдегидрогеназы
(СДГ). СДГ - отщепляет атомы водорода в «транс»-положении. Сукцинат - это
третий субстрат окисления.
этап. Реакция гидратации. Фермент фумаратгидратаза обладает
стереохимической субстратной специфичностью (действует на транс-изомер).
этап. Окислительно-восстановительная реакция завершающая стадия. Малат
подвергается дегидрированию (окислению) при участии НАД+ зависимой
малатдегидрогеназы. Малат является четвертым субстратом окисления цикла Кребса,
который отдает атом водорода в дыхательную цепь.
Регуляция цикла
Цикл Кребса регулируется «по механизму отрицательной обратной связи», при
наличии большого количества субстратов (ацетил-КоА, оксалоацетат), цикл активно
работает, а при избытке продуктов реакции (NADH, ATP) тормозится. Регуляция осуществляется
и при помощи гормонов, основным источником ацетил-КоА является глюкоза, поэтому
гормоны, способствующие аэробному распаду глюкозы, способствуют работе цикла
Кребса. Такими гормонами являются: инсулин и адреналин. Глюкагон стимулирует
синтез глюкозы и ингибирует реакции цикла Кребса.
Как правило работа цикла Кребса не прерывается за счёт анаплеротических
реакций, которые пополняют цикл субстратами: Пируват + СО2 + АТФ =
Оксалацетат(субстрат Цикла Кребса) + АДФ + Фн.
Цикл начинается с того, что ацетильный остаток конденсируется с
оксалоацетатом, в результате чего образуется шестиуглеродное соединение -
цитрат. На образование цитрата в каждом обороте цикла расходуется одна молекула
оксалоацетата; в результате завершения цикла происходит регенерация
оксалоацетата. Таким образом, одна молекула оксалоацетата может многократно
использоваться для окисления ацетильных остатков.
Задание № 10
Связь общих путей катаболизма основных пищевых веществ с целью переноса
электронов и протонов. Можно ли больному сахарным диабетом употреблять в пищу
лимон? Ответ обосновать с биохимической точки зрения? Какая реакция ЦТК в
наибольшей степени аналогична окислительному декарбоксилирования
6-фосфоглюконата в рибулозо-5-фосфат? Какого рода связанный с ферментом промежуточный
продукт образуется при обеих реакциях?
Углеводы, жирные кислоты и большинство аминокислот окисляются в конечном
счёте через цикл лимонной кислоты до СО2 и Н2О. Прежде, чем эти вещества
вовлекаются в заключительный этап катаболизма, их углеродный скелет
превращается в двухуглеродный фрагмент в форме ацетил-КоА (рис. 6). Именно в
этой форме большая часть «топливных» молекул включается в цикл лимонной
кислоты.
Ацетил-КоА образуется в специфических реакциях катаболизма жирных кислот
и некоторых аминокислот. Однако главным источником ацетил-КоА служит
пировиноградная кислота, образующаяся в реакциях катаболизма глюкозы и
некоторых аминокислот.
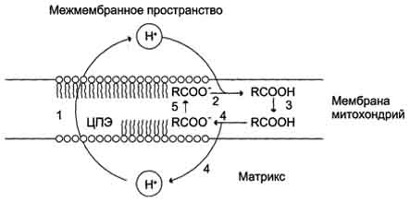
Рис. 5. Механизм разобщающего действия жирных кислот. 1- выкачивание
протонов дыхательной цепью; 2 - протонирование аниона жирной кислоты; 3 -
диффузия протонированной жирной кислоты к внутренней поверхности мембраны; 4 -
диссоциация RCOOH с образованием RCOO- и иона Н+; 5 - перенос RCOO- посредством
АТФ/АДФ-антипортера или разобщающего белка к наружной поверхности
митохондриальной мембраны.
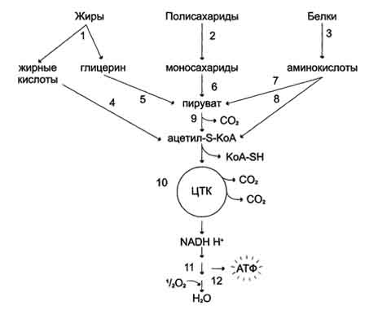
Рис. 6. Катаболизм основных пищевых веществ. 1-3 - пищеварение; 4-8 -
специфические пути катаболизма; 9-10 - заключительный (общий путь) катаболизма;
11 - ЦПЭ; 12 - окислительное фосфорилирование.
Превращение пирувата в ацетил-КоА происходит при участии набора
ферментов, структурно объединённых в пируватдегидрогеназный комплекс (ПДК).
Ацетильный остаток - ацетил- Ко А далее окисляется в цикле лимонной кислоты до
СО2 и Н2О. В этих реакциях окисления принимают участие NAD- и FAD-зависимые
дегидрогеназы, поставляющие электроны и протоны в ЦПЭ, по которой они
передаются на О2.
Цикл лимонной кислоты
Цикл лимонной кислоты (цитратный цикл, цикл Кребса, цикл трикарбоновых
кислот, ЦТК) - заключительный этап катаболизма, в котором углерод ацетильного
остатка ацетил- КоА окисляется до 2 молекул СО2. Атомы водорода,
освобождающиеся в окислительно-восстановительных реакциях, доставляются в ЦПЭ
при участии NAD- и FAD-зависимых дегидрогеназ, в результате чего происходят
синтез воды и окислительное фосфорилирование АДФ. Связь между атомами углерода
в ацетил-КоА устойчива к окислению. В условиях организма окисление ацетильного
остатка происходит в несколько этапов, образующих циклический процесс из 8
реакций.

Рис. 7. Липоевая кислота в составе дигидролипоилтрансацетилазы (Е2).
Липоевая кислота или липоильная группа могут существовать в окисленной
(дисульфидной ЛК-SS) и восстановленной (ЛК-(SН)2) формах. В составе
дигидролипоилтрансацетилазы липоевая кислота связана с белком через остаток
лизина амиднои связью. Липоевая кислота играет роль витамина или фактора роста
у некоторых микроорганизмов, тогда как высшие животные способны её синтезировать.
При сахарном диабете нельзя употреблять в пищу лимон (лимонную кислоту).
Особенно серьезные последствия имеет повышенная деградация жиров.
Накапливающиеся в больших количествах жирные кислоты частично используются в
печени в синтезе липопротеинов (гиперлипидемия), остальные распадаются до
ацетил-КоА. Избыточные количества ацетил-КоА, возникающие в результате
неспособности цитратного цикла полностью его утилизировать, превращаются в
кетоновые тела (см. с. 304). Кетоновые тела - ацетоуксусная и 3-гидроксимасляная
кислоты - повышают концентрацию протонов и влияют на физиологическую величину
рН. Вследствие этого может возникать тяжелый метаболический ацидоз
(диабетическая кома, см. с. 280). Образующийся ацетон придает дыханию больных
характерный запах. Кроме того, в моче увеличивается содержание анионов
кетоновых тел (кетонурия).
Пентозофосфатный путь (ПФП)
Наряду с гликолитическим путем распада глюкозы во многих клетках работает
пентозофосфатный путь (гексамонофосфатный шунт). Он не является основным для
метаболизма глюкозы и служит для генерации в цитоплазме клетки восстановленных
форм НАДФ. Данный кофермент необходим для реакций восстановительного синтеза
жирных кислот и стероидов, а также используется как донор водорода в реакциях
гидроксилирования с участием цитохром-Р450-зависимой системы. Все эти процессы
протекают преимущественно в клетках печени, молочной железы, коры надпочечников
и жировой ткани. Скелетные мышцы, где синтез жирных кислот протекает вяло,
практически лишены пентозофосфатного пути метаболизма глюкозы.
Реакции представлены окислительной и неокислительной ветвями.
Окислительная ветвь:
. Дегидрирование 1-го углеродного атома глюкозо-6-фосфата.
Е: глюкозо-6-фосфатдегидрогеназа. В качестве акцептора электронов
выступает НАДФ+. Образуется 6-фосфоглюколактон - внутренний эфир.
. 6-фосфоглюколактон очень нестабильное соединение, легко гидролизуется
до свободной кислоты с образованием 6-фосфоглюконата.
Е: фосфоглюколактоназа.
. Окислительное декарбоксилирование 6-фосфоглюконата с образованием рибулозо-5-фосфата.
Е: 6-фосфоглюконатдекарбоксилазы и 6-фосфоглюконатдегидрогеназы (акцептор
- НАДФ + ).
Т.о. окислительная ветвь завершается восстановлением двух молекул НАДФ+
Задание № 11
Переваривание углеводов: характеристика соответствующих ферментов ЖКТ.
Механизмы всасывания углеводов, переносчики глюкозы в различных тканях. Почему
амилаза синтезируется сразу в активной форме? Почему активные ферменты не
действуют на стенки ЖКТ? Имеет ли добавление соли к пище физиологический или
только вкусовой смысл?
Изучая процесс пищеварения углеводов, следует запомнить ферменты,
участвующие в нем, выяснить условия их действия в различных отделах
пищеварительного тракта, знать промежуточные и конечные продукты гидролиза.
Поступающие в организм человека сложные углеводы пищи имеют иную
структуру, чем углеводы человеческого тела. Так полисахариды, составляющие
растительный крахмал,- амилоза и амилопектин - представляют собой линейные или
слаборазветвленные полимеры глюкозы, а крахмал человеческого тела - гликоген,-
имея в основе те же глюкозные остатки, образует из них иную -
сильноразветвленную - полимерную структуру. Поэтому усвоение пищевых олиго- и
полисахаридов начинается с их гидролитического (под действием воды) расщепления
в процессе пищеварения до моносахаридов.
Гидролитическое расщепление углеводов в процессе пищеварения происходит
под действием ферментов гликозидаз, расщепляющих 1-4 и 1-6 гликозидные связи в
молекулах сложных углеводов. Простые углеводы пищеварению не подвергаются,
может только происходить брожение некоторой части их в толстом кишечнике под
действием ферментов микроорганизмов.
К гликозидазам относятся амилаза слюны, поджелудочного и кишечного соков,
мальтаза слюны и кишечного сока, конечная декстриназа, сахараза и лактаза
кишечного сока. Гликозидазы активны в слабощелочной среде и угнетаются в кислой
среде, за исключением амилазы слюны, которая катализирует гидролиз
полисахаридов в слабокислой среде и теряет активность при увеличении
кислотности.
В ротовой полости начинается пищеварение крахмала под воздействием
амилазы слюны , которая расщепляет 1-4 гликозидные связи между остатками
глюкозы внутри молекул амилозы и амилопектина. При этом образуются дектстрины и
мальтоза. В слюне содержится в небольших количествах и мальтаза, гидролизующая
мальтозу до глюкозы. Другие дисахариды во рту не расщепляются
Большая часть молекул полисахаридов не успевает гидролизоваться во рту.
Смесь крупных молекул амилозы и амилопектина с более мелкими - декстринами.
Мальтозой, глюкозой- поступает в желудок. Сильно кислая среда желудочного сока
угнетает ферменты слюны, поэтому дальнейшие превращения углеводов происходят в
кишечнике, сок которого содержит бикарбонаты, нейтрализующие соляную кислоту
желудочного сока. Амилазы поджелудочного и кишечного соков более активны, чем
амилаза слюны. В кишечном соке содержится также конечная декстриназа,
гидролизующая 1-6 связи в молекулах амилопектина и декстринов. Эти ферменты
завершают расщепление полисахаридов до мальтозы. В слизистой оболочке кишечника
вырабатываются также ферменты, способные гидролизовать дисахариды : мальтаза,
лактага, сахараза. Под воздействием мальтазы мальтоза расщепляется на две
глюкозы, сахароза под воздействием сахаразы - на глюкозу и фруктозу, лактаза
расщепляет лактозу на глюкозу и галактозу.
В пищеварительных соках отсутствует фермент целлюлаза, гидролизующая
поступающую с растительной пищей целлюлозу. Однако в кишечнике имеются
микроорганизмы, ферменты которых могут расщеплять некоторое количество
целлюлозы. При этом образуется дисахарид целлобиоза, распадающийся потом до
глюкозы.
Не расщепившаяся целлюлоза является механическим раздражителем стенки
кишечника, активирует его перистальтику и способствует продвижению пищевой
массы.
Под действием ферментов микроорганизмов продукты распада сложных углеводов
могут подвергаться брожению, в результате чего образуются органические кислоты,
СО2,СН4 и Н2. Схема превращений углеводов в пищеварительной системе
представлена на схеме.
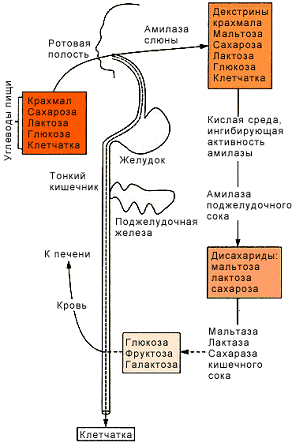
Образовавшиеся в результате гидролиза углеводов моносахариды по своей
структуре одинаковы у всех живых организмов. Среди продуктов пищеварения
преобладает глюкоза (60%), она же является главным моносахаридом, циркулирующим
в крови. В кишечной стенке фруктоза и галактоза частично превращаются в глюкозу,
так что содержание ее в крови, оттекающей от кишечника, больше, чем в его
полости.
Всасывание моносахаридов - активный физиологический процесс, протекающий
с затратой энергии. Ее обеспечивают окислительные процессы, происходящие в
клетках кишечной стенки. Моносахаориды получают энергию, взаимодействуя с
молекулой АТФ в реакциях, продуктами которых являются фосфорные эфиры
моносахаридов. При переходе из кишечной стенки в кровь фосфорные эфиры
расщепляются фосфатазами, и в кровоток поступают свободные моносахариды.
Поступление их из крови в клетки различных органов также сопровождается их
фосфорилированием.
Однако скорость превращения и появления в крови глюкозы из разных
продуктов разная. Механизм этих биологических процессов отражен в понятии
'гликемический индекс' (ГИ), которое показывает скорость превращения углеводов
пищи (крахмала, гликогена, сахарозы, лактозы, фруктозы и т.д.) в глюкозу крови.
Соль жизненно необходима для жизнедеятельности человека, равно как всех
прочих живых существ. Соль участвует в поддержании и регулировании
водно-солевого баланса в организме, натрий-калиевого ионного обмена. Тонкие
биологические механизмы поддерживают постоянной концентрацию хлористого натрия
в крови и в других жидкостях организма. Разность концентрации соли внутри
клетки и снаружи является основным механизмом для поступления питательных
веществ к клетке и выводу продуктов её жизнедеятельности. Этот же механизм
разделения концентрации соли используется в генерации и передаче нервных
импульсов нейронами. Кроме того, ион хлора в соли является основным материалом
для выработки соляной кислоты - важного компонента желудочного сока. Суточная
потребность в соли составляет 10-15 г, а в условиях жаркого климата, вследствие
повышенного потоотделения, - до 25-30 г. При экстремальных нагрузках на
организм суточная потребность в соли может достигать 100-150 г. Недостаток соли
организм восполняет разрушением костной и мышечной тканей. Недостаток соли
может привести к депрессиям, нервным и психическим заболеваниям, нарушением пищеварения
и сердечно-сосудистой деятельности, спазмам гладкой мускулатуры, остеопорозу,
анорексии. При хронической нехватке соли в организме возможен смертельный
исход.
Задание № 12
Гипо- и гипергликемия. Сахарный диабет, биохимические основы накопления кетоновых
тел при сахарном диабете. Для синтеза глюкозы в печени необходим
фосфоенолпируват. Однако его образование в печени окажется очень неэффективным,
если фосфоенолпируват будет дефосфорилироваться под действием пируваткиназы с
образованием пирувата. Как избежать этого холостого цикла? Почему этот механизм
не подходит для мышц?
Ги́пергликеми́я - клинический симптом, обозначающий
увеличение содержания глюкозы в сыворотке крови:
Гипогликемия - патологическое состояние, характеризующееся снижением
уровня глюкозы периферической крови ниже нормы (3,3 ммоль/л).
Особенно серьезные последствия имеет повышенная деградация жиров.
Накапливающиеся в больших количествах жирные кислоты частично используются в
печени в синтезе липопротеинов (гиперлипидемия), остальные распадаются до
ацетил-КоА. Избыточные количества ацетил-КоА, возникающие в результате неспособности
цитратного цикла полностью его утилизировать, превращаются в кетоновые тела
(см. с. 304). Кетоновые тела - ацетоуксусная и 3-гидроксимасляная кислоты -
повышают концентрацию протонов и влияют на физиологическую величину рН.
Вследствие этого может возникать тяжелый метаболический ацидоз. Образующийся
ацетон придает дыханию больных характерный запах. Кроме того, в моче
увеличивается содержание анионов кетоновых тел (кетонурия).
Глюконеогенез - синтез глюкозы из неуглеводных продуктов. Такими продуктами
или метаболитами являются в первую очередь молочная и пи-ровиноградная кислоты,
так называемые гликогенные аминокислоты, гли-церол и ряд других соединений.
Иными словами, предшественниками глюкозы в глюконеогенезе может быть пируват
или любое соединение, превращающееся в процессе катаболизма в пируват или один
из промежуточных продуктов цикла трикарбоновых кислот.
У позвоночных наиболее интенсивно глюконеогенез протекает в клетках
печени и почек (в корковом веществе).
Большинство стадий глюконеогенеза представляет собой обращение реакции
гликолиза. Только 3 реакции гликолиза (гексокиназная, фосфо-фруктокиназная и
пируваткиназная) необратимы, поэтому в процесс глю-конеогенеза на 3 этапах
используются другие ферменты. Рассмотрим путь синтеза глюкозы из пирувата.
Образование фосфоенолпирувата из пирувата. Синтез фосфоенолпирувата
осуществляется в несколько этапов. Первоначально пируват под влиянием.
По сравнению с другими органами печень отличается наиболее сложным
обменом глюкозы. Кроме пары противоположных процессов (синтеза и распада
гликогена), в печени могут происходить ещё два противоположно направленных
процесса - гликолиз и глюконеогенез. В большинстве других органов происходит
только гликолиз. Переключение печени с гликолиза на глюконеогенез и обратно
происходит с участием инсулина и глюкозагона и осуществляется с помощью:
аллостерической регуляции активности ферментов;
ковалентной модификации ферментов путём
фосфорилирования/дефосфорилирования;
индукции/репрессии синтеза ключевых ферментов.
Регуляторные воздействия направлены на ферменты, катализирующие
необратимые стадии гликолиза и глюконеогенеза, сочетание которых называют
«субстратными», или «холостыми» циклами.
«Субстратные» циклы - парные комбинации процессов синтеза и распада
метаболитов. Как уже упоминалось, сочетание процессов синтеза и распада
гликогена или необратимых реакций гликолиза и соответствующих им необратимых
реакций глюконеогенеза может составить подобный цикл. Название «субстратный
цикл» означает объединение реакций синтеза и распада субстрата. Название
«холостой» отражает результат работы подобного цикла, заключающийся в
бесполезном расходовании АТФ. Хотя существование «холостых» циклов нелогично,
тем не менее они могут функционировать. Более того, эти циклы могут быть
мишенью регуляторных воздействий, так как составляющие их реакции катализируют
разные ферменты. Реципрокное изменение активности этих ферментов предотвращает
одновременное протекание противоположных процессов.
Изменение в печени гликолитического направления на глюконеогенез и
обратно при смене абсорбтивного состояния на постабсорбтивное или при голодании
происходит главным образом в результате регуляции активности ферментов,
катализирующих реакции субстратных циклов. Эти циклы обозначены цифрами I, II,
III на рис. 9, представляющем общую картину регуляции гликолиза и
глюконеогенеза в печени.
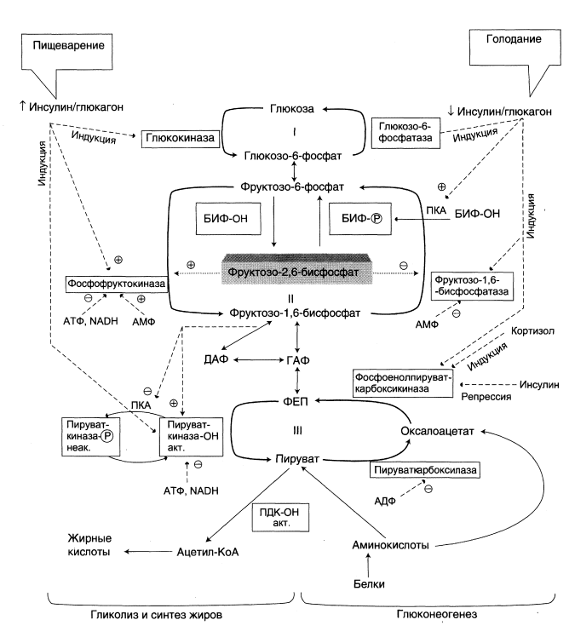
Рис. 9. Регуляция метаболизма глюкозы в печени. БИФ - бифункциональный
фермент (фруктозо-2,6-бисфосфатаза/фос-фофруктокиназа-2); БИФ-ОН - дефосфорилированный
фермент; БИФ-Р - фосфорилированный фермент, ПДК-ОН - дефосфорилированный
пируватдегидрогеназный комплекс; ПК-ОН - дефосфорилированная пируваткиназа; ГАФ
- глицеральдегидфосфат; ДАФ - дигидроксиацетонфосфат, ФЕП - фосфоенолпируват.
I-III - субстратные циклы: в рамках - регупяторные ферменты глиполиза и
глюконеогенеза.
Направление реакции первого субстратного цикла регулируется главным
образом концентрацией глюкозы. При пищеварении концентрация глюкозы в крови
повышается (до 8-10 ммоль/л). Активность глюкокиназы в этих условиях
максимальна. Вследствие этого ускоряется гликолитическая реакция образования
глюкозо-6-фосфата. Кроме того, инсулин индуцирует синтез глюкокиназы и ускоряет
тем самым фосфорилирование глюкозы. Поскольку глюкокиназа печени не
ингибируется глюкозо-6-фосфатом (в отличие от гексокиназы мышц), то основная
часть глюкозо-6-фосфата в абсорбтивном периоде направляется на синтез гликогена
и по гликолитическому пути.
Задание № 13
А. У грудного ребенка часто появляются судороги, при обследовании
отмечено увеличение размеров печени. В крови повышено содержание лактата и
пирувата, гипергликемия. При введение адреналина содержание сахара в крови не
возрастает, увеличивается количество молочной кислоты. О каком нарушении
углеводного обмена можно думать?
Б. Ребенок перенес инфекционное заболевание. Какие изменения белковых
фракций можно ожидать?
Гликогенозы. Ряд наследственных болезней связан с нарушением обмена
гликогена. Эти болезни получили название гликогенозов. Они возникают в связи с
дефицитом или полным отсутствием ферментов, катализирующих процессы распада или
синтеза гликогена, и характеризуются избыточным его накоплением в различных
органах и тканях.
Гликогеноз I типа (болезнь Гирке) встречается наиболее часто, обусловлен
наследственным дефектом синтеза фермента глюкозо-6-фосфатазы в печени и почках.
Болезнь наследуется по аутосомно-рецессивному типу. Патологические симптомы
появляются уже на первом году жизни ребенка: увеличена печень, нередко
увеличены почки. В результате гипогликемии появляются судороги, задержка роста,
возможен ацидоз. В крови - повышенное количество лактата и пирувата. Введение
адреналина или глюка-гона вызывает значительную гиперлактатацидемию, но не
гипергликемию, так как глюкозо-6-фосфатаза в печени отсутствует и образования
свободной глюкозы не происходит.
Гиперпротеинемия - увеличение общего содержания белков плазмы. Диарея у
детей, рвота при непроходимости верхнего отдела тонкой кишки, обширные ожоги
могут способствовать повышению концентрации белков в плазме крови. Иными
словами, потеря воды организмом, а следовательно, и плазмой приводит к
повышению концентрации белка в крови (относительная гиперпротеинемия).
При ряде патологических состояний может наблюдаться абсолютная
гиперпротеинемия, обусловленная увеличением уровня γ-глобулинов: например,
гиперпротеинемия в результате инфекционного или токсического раздражения
системы макрофагов; гиперпротеинемия при миеломной болезни.
Гипопротеинемия, или уменьшение общего количества белка в плазме крови,
наблюдается главным образом при снижении уровня альбуминов. Выраженная
гипопротеинемия - постоянный и патогенетически важный симптом нефротического
синдрома. Содержание общего белка снижается до 30-40 г/л. Гипопротеинемия
наблюдается также при поражении печеночных клеток (острая атрофия печени,
токсический гепатит и др.).
При многих заболеваниях очень часто изменяется процентное соотношение
отдельных белковых фракций, хотя общее содержание белка в сыворотке крови
остается в пределах нормы. Такое состояние носит название «диспротеинемия».
В течении многих болезней, связанных с общим воспалением (инфекционные
заболевания, ревматизм и т.д.), отмечается несколько стадий, что, несомненно,
сказывается и на белковом спектре крови.

Список
литературы
1. Днепровский А.С. Теоретические основы органической
химии/А.С.Днепровский, Т.И.Темникова: Учебник для вызов. - 2-е изд.,
перераб.-Л.: Химия, 1991;
2. Овчинников Ю.А. Биоорганическая химия. - М.:
Просвещение, 1987;
. Кнорре Д.Г., Мызина С.Д. Биологическая химия: Учеб.
для хим, биол. и мед. спец. вузов. - 3-у изд., испр. - М.: Высш.шк., 2000;
. Ермолаев М.В., Ильичевская А.Г. Биологическая химия.
- М.: Медицина, 1990.
. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. -
М.: Медицина, 1991.
. Шиманович И.Е. Общая химия в формулах, определениях,
схемах. Учебное пособие для студентов нехимических специальностей вузов. - М.:
Новая волна, 2002.
. Глинка Н.Л. Общая химия. - М.: Интеграл-пресс, 2002.
. Суворов А.В., Никольский А.Б. Общая химия. - Спб.:
Химия, 1995.
. Цветков Л.И. Органическая химия. - М.: Просвещение,
1988.
. Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. -
М.: Медицина, 1991.