Разработка методики исследования высокоэнергетических материалов на базе нанодисперсных компонентов
Введение
Нанотехнология - достаточно новая область науки и техники, появление
которой связано с обращением фундаментальных наук к наноразмерным объектам,
совершенно новым структурам, обладателям уникальных свойств в той или иной
области. Большинство этих свойств еще не изучены, еще не открыты многие
возможности, связанные использованием наноматериалов.
Одна из таких возможностей (чем и обусловлен интерес к наноструктурам, в
частности, ракетостроения) - применение подобных объектов в качестве
компонентов высокоэнергетических материалов - в частности, компонентов ракетных
топлив. Существует предположение о том, что введение в топливо тех или иных
компонентов в виде наночастиц значительно повысит энергетическую эффективность
этого топлива, что можно рассматривать как прорыв в ракетостроении.
В данной работе осуществляется разработка методики исследования ВЭМ на
базе нанодисперсных компонентов: производится анализ свойств наноразмерных
объектов и влияния их свойств на энергетическую эффективность топлив, разрабатываются
программные средства, позволяющие произвести оценку калорийности топлив на базе
нанокомпонентов, разрабатывается и описывается методика экспериментального
определения калорийности топлив.
Конструкторская
часть
Глава
1.Свойства наночастиц. Обоснование возможности использования наночастиц как
компонентов высокоэнергетических материалов (ВЭМ)
1.1 Определение
Судя по всему, эра «карликов» приходит на смену эре ЭВМ: появляется все
больше и больше научных работ, связанных с изучением и применением наночастиц.
Во многих отраслях науки уже используются их уникальные свойства, но
большинство этих свойств еще не изучены, еще не открыты многие возможности,
связанные использованием наноматериалов.
Что же это такое - наноструктуры?
Наноструктурами называют структуры малых форм вещества (нанос - карлик,
обычно от 1 до 1000нм). По мере измельчения вещества в нем могут возникать
новые структуры. Состояние и структура - не одно и то же: изменение состояния
фазы при изменении ее размера происходит всегда и описывается известными
термодинамическими соотношениями, а структурные изменения, хоть и подчиняются
термодинамике, - явление уникальное, установленное в эксперименте. Уже
проведено множество таких экспериментов, и обнаружены десятки типов таких
структур. В чем уникальность наноструктуры? [1]
Переход в мир наноразмерных объектов заставил обратить внимание на
физические эффекты и явления, обнаруженные ранее, но по разным причинам не
привлекавшие внимания или игнорировавшиеся.
Опытным путем выяснено, что наночастицы некоторых материалов имеют очень
хорошие каталитические и адсорбционные свойства. Другие материалы показывают
удивительные оптические свойства, например сверхтонкие пленки органических
материалов, применяют для производства солнечных батарей. Такие батареи, хоть и
обладают сравнительно низкой квантовой эффективностью, зато более дешевы и
могут быть механически гибкими. Удается добиться взаимодействия искусственных
наночастиц с природными объектами наноразмеров-белками, нуклеиновыми кислотами
и др., что отразится на химии, биологии, медицине. [2]
1.2
Особенности
Соизмеримость размеров наноматериала с характерным размером для того или
иного физического явления вызывает разнообразные размерные эффекты, а
увеличенная поверхностная энергия наночастиц приводит к метастабильному
состоянию материалов, находящихся в ультрадисперсном состоянии. Могут
изменяться межатомные расстояния и происходить перестройка кристаллической
структуры вплоть до перехода кристаллической структуры в аморфное состояние.
Поверхностные атомы подложки образуют силовое поле, которое способствует
образованию на поверхности подвижных групп атомов и кластеров, причем над
поверхностью подложки в процессе кристаллизации потенциал максимален, что
приводит к высокой вероятности ассоциации атомов в кластер и низкой вероятности
распада этого кластера.
Другой особенностью при создании наноструктур и наноэлементов является
характерная зависимость функциональных свойств от геометрических размеров.
Понятная на интуитивном уровне функциональная связь состав-свойство заменяется
на непривычную размер-свойство или число атомов-свойство. Если в
микроэлектронике изменение размеров структурных элементов вызывает только
изменение величины параметров, то в наноэлектронике возникают новые
функциональные возможности, требующие перехода к более упорядоченным средам.
При переходе к наноразмерам происходит, в частности, изменение среднего
координационного числа атомов в кристаллических наноструктурах в зависимости от
их линейных размеров. В результате увеличения координационного числа в
кристаллах диэлектрики переходят в металлическое состояние. Возможно также
существование структур, состоящих из столь небольшого количества атомов и
обладающих столь специфическими свойствами, что их можно трактовать как
находящиеся в расплавленном состоянии при любой температуре. С чем же связаны
такие свойства? В самом общем виде удаление от равновесия, и соответственно,
избыточная свободная энергия Гиббса могут быть связаны с характерным для
наноматериалов обилием поверхностей раздела, наличием неравновесных фаз и
пограничных сегрегаций, остаточных напряжений и повышенного содержания дефектов
кристаллического строения.
Дело в том, что в обычных макротелах число атомов на поверхности тела
невелико по сравнению с его объемом, поэтому все физические свойства тела
определяются физическими свойствами объемного образца. Особенность тонких
пленок состоит в том, что у них объем, занимаемый поверхностными, атомными или
молекулярными слоями, вполне сопоставим с объемом самой пленки. Пленку нанометровых
размеров можно рассматривать как особую двумерную систему, свойства которой
определяются исключительно свойствами поверхностного слоя, так как слоев,
соответствующих объемному образцу, практически не существует.
Чтобы обраться к наноразмерным эффектам, следует обратиться к специфике
малых систем, а она состоит в том, что чем меньше частицы вещества, тем большую
относительную роль играют в них поверхностные явления. Это связано с
уменьшением внутри наночастицы объемной фазы. В макрочастице: площадь поверхности
Ω=4πr2(~r2) а ее объем V=4/3 πr3 (~r3),т.е. Ω/V=1/r. При уменьшении размера частицы это нарушается, объемная
фаза внутри нее уменьшается и может вообще исчезнуть.
При диаметре частицы 1-1.5 нм практически вся она представляет собой
поверхность, и свойства ее будут совершенно уникальными. При диспергировании
резко возрастает активность вещества в твердом состоянии и скорость
физико-химического взаимодействия с окружающей средой. Скорость такого
взаимодействия всегда пропорциональна величине поверхности. Чем тоньше
структура вещества, тем быстрее оно растворяется, тем быстрее протекают
твердотельные реакции, например, при взрывах. Ярким примером этого является
фрактальный клубок, взрывчатая способность которого приближается к взрывчатой
способности лучших порохов. По плотности вещества это газ, но как связанное
состояние вещества, он может проявлять свойства и жидкости, и твердого тела.
Как система из нанометровых частиц, фрактальный клубок обладает большой
поверхностной энергией. Поскольку заметная доля находящихся в нем молекул
находится на поверхности частиц.
Для высокодисперсных частиц характерна структурная, фазовая и
концентрационная неоднородность, в них реализуется особый тип дальнего порядка,
при котором межатомное расстояние закономерно изменяется при переходе от центра
частицы к ее поверхности. Следствием этого является возбужденное состояние
атомов в решетке, что служит главной причиной повышенной физико-химической
активности высокодисперсных систем.
Зависимости физико-химических свойств от размера частицы оказывают
существенное влияние на оптические спектры, механические, магнитные и
электрические свойства, термодинамику, электрохимию, особенности
электропроводности и транспорта электронов. Специфические размерные эффекты
наиболее сильно проявляются в малых частицах и особенно характерны для
нанохимии, где преобладают нерегулярные зависимости свойств от размера.
Зависимость реакционной способности от размера частиц может быть связана с
изменением свойств частицы при ее взаимодействии с реагентом, корреляцией между
геометрической структурой и структурой электронной оболочки, симметрией
граничных орбиталей частицы относительно орбиталей адсорбируемой молекулы.
Понимание закономерностей, управляющих частицей размером 1нм и меньше, является
одной из основных проблем современной нанотехнологии.
1.3 Получение
Свойства многих наноматериалов становятся зависимыми от способа
получения, что делает проблематичным установление основных закономерностей,
обусловленных влиянием размера частиц на их физико-химические свойства. Особый
интерес представляет взаимодействие электромагнитного излучения оптического и
СВЧ диапазонов, с ансамблем, состоящим из наночастиц, при котором наблюдаются
различные аномальные эффекты. Ряд экспериментальных данных дает основание полагать,
что при гомогенном образовании зародыш кристаллической фазы может иметь другой
фазовый состав, чем образующийся из него массивный кристалл. Фазовый состав
одних и тех же веществ с одинаковым нанометрическим размером может быть разным
в зависимости от вклада энергии поверхности раздела в общую энергию
образующейся системы.
Получать наноструктуры можно двумя путями: либо тщательным измельчением
(диспергированием) объемных образцов - путь «сверху-вниз», либо получением
новой дисперсной фазы путем объединения молекул или ионов в кластеры,
монокристаллиты или капли нанометрового размера за счет действия молекулярных и
других сил - путь «снизу-вверх».
Роль среды диспергирования приобретает огромное значение. Релаксация
огромных напряжений может осуществляться путем распада структуры кристалла на
нанокристаллы. Распад структуры может происходить и отдельными нанокристаллами
(нульмерный распад), и отдельными, линейно связанными нанокристаллами
(одномерный распад), и отдельными слоями (двумерный распад).
Существует разные мнения по поводу того, что следует понимать под твердым
телом. Первая точка зрения - только кристаллическая структура, имеющая ярко
выраженный порядок может называться твердым телом. Но есть и другая, исходящая
из наличия достаточного потенциального барьера, который препятствовал бы
спонтанному переходу из одного равновесного состояния в другое. При достаточной
величине потенциального барьера система может быть весьма устойчивой, и
вероятность фазового перехода становится меньше, чем вероятность разрушения
структуры под воздействием случайных величин. Вообще, кристаллизация является
не основным видом отвердевания вещества. Физике твердотельных конденсированных
сред присущи свои законы, отличающие поведение неупорядоченных аморфных твердых
веществ от идеальных кристаллов, причем дефекты структуры вещества ведут себя
по-разному в идеальной кристаллической решетке и аморфной структуре с большим
количеством других дефектов. Поскольку у аморфных веществ внутреннее строение
существенно меньше упорядочено, чем у кристаллических, то для аморфных тел
характерны более высокие значения внутренней энергии и энтропии. Неустойчивость
приводит не просто к потере равновесия системы, но и к появлению качественно
новых физических эффектов, таких как самопроизвольное зарождение порядка в
неупорядоченной системе.
Предполагается, что наиболее общей характеристикой вещества является не
кристаллическая решетка, а его остов - непрерывная система межатомных связей.
Такая система объединяет атомы вещества независимо от того кристаллическое оно
или аморфное, в островки, цепи или каркасы, представляющие собой ноль - одно-
двух- и трехмерные остовы вещества соответственно. Тип строения и свойства
вещества при таком подходе определяются строением остова и его мерностью.
Сохранение и деструкция остова в ходе химического превращения определяет тип
этого превращения. Поэтому возможен синтез материалов на основе их
метастабильных состояний, что значительно расширяет круг используемых
материалов, тем более что аморфные материалы обладают некоторыми совершенно
уникальными свойствами, недостижимыми в кристаллическом состоянии.
Второй путь физических методов получения ультрадисперсных частиц это их
синтез на основе процессов испарения и конденсации, т.е. применение
модифицированного метода термического вакуумного испарения, но с особым
характером рабочей среды и особыми методиками организации процесса конденсации
и сбора получаемого порошка. Разработаны физические основы конденсации металлов
и предложены методы расчета распределения по размерам частиц аэрозоля металлов.
Возможно получение порошка со средним размером 3-5 нм.
К химическим методам получения наночастиц и наноструктур относятся
золь-гель - технологии, гидротермальный синтез, реакции в расплавах солей,
седиментацию, восстановление из оксидов и других соединений, термическое
разложение веществ. При этом основными условиями являются протекание реакции
вдали от равновесия и высокая скорость образования зародышей новой фазы в
сочетании с малой скоростью их роста. Это обеспечивается подбором температуры,
при которой химическая реакция идет достаточно интенсивно, а перенос через
газовую фазу еще заторможен.
К настоящему времени накоплен обширный научный материал по
экспериментально обнаруженным эффектам, связанным со слабыми и сверхслабыми
воздействиями различной природы на разнообразные физические и биологические
объекты и процессы. Несмотря на то, что интенсивность этих воздействий
исключительно мала, факты такого влияния однозначно зафиксированы для самых
различных типов воздействий и разнообразных физических систем. При изучении
влияния импульсных магнитных полей (ИМП) на конденсируемые среды установлено,
что кратковременное воздействие слабых ИМП вызывает долговременное изменение
структуры и физических свойств широкого класса немагнитных материалов, причем
наблюдается запаздывание проявления эффектов после окончания воздействия и
долговременный немонотонный характер кинетики этих процессов. Например,
меняется температура плавления, энергия активации и температура кристаллизации
через несколько часов после воздействия.
Установлено, что кратковременное воздействие ИМП приводит к топологии
поверхности. Зафиксированные изменения достигают максимума в районе 150-200
часов после снятия воздействия. Похожие эффекты наблюдаются в высокотемпературных
проводниках.
Поскольку практически все наноструктуры являются твердотельными, то в
них, как в упругой среде, могут возникать объемные и поверхностные волны,
локализованные вблизи границ зерен. Свойство поверхностных волн локализовать
энергию возмущений, созданных на поверхности в узком поверхностном слое,
приводит к резонансным явлениям, сопровождающим движение вдоль поверхности
источников возмущений. Можно предположить, что большинство наблюдаемых эффектов
воздействия слабых и сверхслабых возмущений на физические системы связано с
резонансными процессами.
Полученные в неравновесных условиях после прекращения технологического
процесса фрактальные структуры стремятся к равновесному состоянию, вследствие
чего в них продолжается процесс эволюции. Их состояние можно сравнить как бы с
резкой заморозкой и дальнейшим медленным эволюционным процессом перестройки их
структуры. Неверно определять эти процессы как деградацию или старение,
поскольку речь не идет об ухудшении каких-то характеристик или процессах распада,
здесь более уместен термин «созревание» или эволюционирование.
.4 Влияние на
энергетическую эффективность ракетных топлив
Основы коллоидной химии.
Коллоидная химия - наука, изучающая дисперсные системы и поверхностные
явления. К поверхностным явлениям относятся процессы, происходящие на границе
раздела фаз, в межфазном поверхностном слое и возникающие в результате
взаимодействия сопряженных фаз. Как уже было сказано выше, влияние
поверхностных явлений на процессы, происходящие в наноструктурах - важнейшая
особенность исследуемых систем. Поэтому перед тем как заняться детальным
рассмотрением и анализом энергетических свойств наноструктур необходимо
обозначить основные процессы и явления, характерные для таких систем а также
привести соотношения, выражающие основные закономерности коллоидной химии.
Признаки дисперсных систем:
. Дисперсность (раздробленность) - определяется размерами и геометрией
наноструктуры.
Важнейшей характеристикой дисперсности является:
Удельная поверхность частицы - площадь раздела фаз, приходящаяся на
единицу объема дисперсной фазы.
Sуд=S/V (1.1)
где S - площадь межфазной поверхности, V - объем частицы
Для системы, содержащей одинаковые частицы дисперсной фазы сферической
формы(исследуемый случай):
Sуд =6/a
где а - выбранный линейный размер частицы
При дроблении и измельчении тел увеличивается их удельная поверхность,
которая может достигать значительных величин. Размеры молекул обычно составляют
доли нанометра - при таких условиях удельная поверхность может иметь значения,
достигающие тысячи квадратных метров на кубический сантиметр. Используя
удельную поверхность как усредненную характеристику можно сравнивать различные
дисперсные системы между собой.
. Гетерогенность (многофазность) - признак, указывающий на наличие межфазной
поверхности (поверхностного слоя) в этих структурах. Поскольку коллоидная химия
концентрирует внимание на процессах, происходящих на межфазных границах, именно
этот признак обуславливает характерные свойства объектов.
Поскольку все дисперсные системы гетерогенны, они состоят как минимум из
двух фаз. Одна из них является сплошной и называется дисперсионной средой,
другая - раздроблена и распределена в первой; ее называют дисперсной фазой.
Поверхностные явления классифицируют в соответствии с объединенным
уравнением первого и второго начал термодинамики, в которое входят основные
виды энергии. Для любой гетерогенной системы его можно записать так
dG = - SdT +
Vdp + σds + 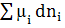
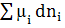 + φdq (1.2)
+ φdq (1.2)
где
G - энергия Гиббса; S - энтропия; T - температура; V -
объем; p - давление; σ - поверхностное натяжение; s -
площадь поверхности; 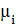
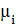 -
химический потенциал компонента i;
-
химический потенциал компонента i; 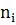
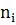 - число
молей компонента i;
- число
молей компонента i; 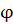 -
электрический потенциал; q - количество электричества.
-
электрический потенциал; q - количество электричества.
Величина
σds называется поверхностной энергией системы.Любая
дисперсная система обладает поверхностной энергией.
Уравнение
выражает приращение энергии Гиббса через алгебраическую сумму приращений других
видов энергии. Стрелки указывают на пять возможных процессов превращения
поверхностной энергии σds: а) в энергию
Гиббса б) в теплоту в) в химическую энергию г) в механическую энергию д) в
электрическую энергию. Превращение поверхностной энергии в представленные виды
энергии отвечает поверхностным явлениям, таким как измерение реакционной
способности с изменением дисперсности, адгезия и смачивание, капиллярность,
адсорбция, электрические явления.
Поверхностное
натяжение (σ)
- величина, характеризующая энергию единицы
поверхности. Поверхностное натяжение определяет степень гетерогенности,
резкость перехода от одной фазы к другой, различие между соприкасающимися
фазами. Чем сильнее выражена гетерогенность и чем более резко различаются по
природе сопряженные фазы, тем больше поверхностное натяжение. Запишем его для
гетерогенной системы относительно изменения внутренней энергии U:
dU = TdS -
pdV + σds + 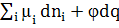
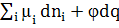 (1.3)
(1.3)
S - энтропия, T -
температура, V - объем, p - давление, σ - поверхностное натяжение , s - площадь
поверхности, 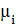
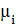 -
химический потенциал компонента i,
-
химический потенциал компонента i, 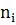
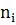 - число
молей компонента i,
- число
молей компонента i,  -
электрический потенциал, q - количество электричества
-
электрический потенциал, q - количество электричества
При
постоянных S, V, 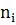
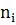 , q имеем
, q имеем
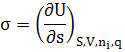
т.е.
поверхностное натяжение есть частная производная от внутренней энергии по
площади поверхности раздела фаз при постоянных энтропии, объеме, количестве
молей и заряде.
Так
как объединенное уравнение первого и второго начал термодинамики может быть
записано и относительно других термодинамических потенциалов, а именно энергии
Гиббса, энергии Гельмгольца и энтальпии H, то при
соответствующих постоянных параметрах получим

Таким
образом, поверхностное натяжение есть частная производная от любого
термодинамического потенциала по площади межфазной поверхности при постоянных
соответствующих параметрах. [4] Из данного определения поверхностного натяжения
следует, что при постоянных соответствующих параметрах и концентрациях
увеличение площади поверхности раздела фаз в квазистатическом процессе
сопровождается работой 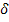
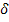 W причем
W причем
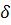
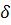 W = - σds
=> σ
= -
W = - σds
=> σ
= - 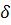
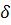 W/ds (1.5)
W/ds (1.5)
Поверхностное
натяжение, например, на границе жидкой с газовой фазой можно представить как
работу, расходуемую на обратимый разрыв столбика этой жидкости с поперечным
сечением ½ единице площади, т. к. при разрыве образуется новая
поверхность, равная единице площади (его можно рассматривать как работу
переноса молекул из объема тела на поверхность). Так как поверхностное
натяжение связано с работой, расходуемой на разрыв межмолекулярных связей, оно
ими и обусловлено. Чем сильнее межмолекулярные связи в данном теле, тем больше
поверхностное натяжение.
У
тел в твердом состоянии, по сравнению с жидким, силы межмолекулярного и
межатомного взаимодействия больше на величину, определяемую энтальпией
плавления (затвердевания). Соответственно, они имеют и большее поверхностное
натяжение.[5]
Отличия наносистем от дисперсных систем.
Несмотря на те же способы получения, некоторые свойства наноструктур
отличаются от свойств дисперсных систем.
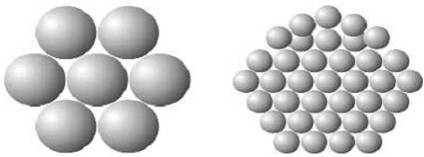
Рис.1.1 слева: сечение наночастицы, справа - сечение частицы дисперсной
фазы, под ними: слева - микрочастица, находящаяся в несимметричном силовом
поле, справа - микрочастица, находящаяся в симметричном силовом поле
Так как наночастица по размеру меньше частицы дисперсной фазы большинство
составляющих ее микрочастиц расположены на поверхности наночастицы ( т.е.
находятся в несимметричном силовом поле). Из этого следует, что поверхностная
энергия такой частицы больше, чем та, которой обладает частица дисперсной фазы.
Избыточная энергия
Как следует из определения, поверхностное натяжение различных
конденсированных тел на границе с газом непосредственно связано с
межмолекулярным и межатомным взаимодействием в конденсированной фазе.
Взаимодействие молекул внутри одной фазы называют когезией.
Когезионные силы называют силами притяжения. Когезия отражает
межмолекулярное взаимодействие внутри гомогенной фазы, поэтому ее могут
охарактеризовать такие параметры как энергия кристаллической решетки,
внутреннее давление, энергия парообразования и др.
В процессе испарения вещества происходит полный разрыв межмолекулярных
связей поэтому работа когезии определяется энтальпией парообразования:
∆Hп = ∆Gп + T∆Sп (1.6)
где ∆Gп - изменение энергии Гиббса при
парообразовании; ∆Sп - изменение энтропии при
парообразовании.
Энтальпия парообразования твердых тел равна энергии кристаллической
решетки.
В условиях равновесия между конденсированной и паровой фазами p = const. и
T = const.
∆G = 0, тогда:
∆Hп = T∆Sп
Следовательно, чем больше энтальпия парообразования, тем больше работа
когезии, а значит и поверхностное натяжение, его энтропия.
Говоря об избыточной энергии раздела фаз необходимо подчеркнуть
особенность термодинамического состояния вещества в поверхностных слоях. Эта
особенность в каждом отдельном случае проявляется в ненасыщенности определенных
физических сил и химических связей, характерных для конденсированных фаз, а для
твердых тел поверхностные свойства зависят также от типа кристаллических
решеток. Разные кристаллические структуры резко отличаются по свойствам, в том
числе и по энергии когезионных связей. Прослеживается уменьшение этой энергии в
ряду кристаллов:
ковалентные → ионные → металлические → молекулярные
Кроме того, химическая структура различных граней одного и того же
кристалла может существенно различаться.
В соответствии с известным уравнением энтальпия поверхности равна:
H = G + TS
По аналогии - избыток внутренней энергии поверхности конденсированных
систем:
Us = Gs + TSs
где s означает отнесение потенциалов к
единице поверхности
Учитывая, что Gs = σ , а также второе начало термодинамики,
получим:
Us = qs
+ σ
После некоторых преобразований при постоянстве всех параметров, кроме T:
Us = σ - T(∂σ/∂T)p (1.7)
Это соотнощение называется уравнением Гиббса-Гельмгольца. Оно связывает
полную поверхностную энергию с энергией Гиббса. Из этого уравнения следует, что
для определения полной поверхностной энергии необходимо знать зависимость
поверхностного натяжения от температуры. Конкретную зависимость можно получить
экспериментально, но можно сделать общий вывод: т.к. qs >0 всегда для индивидуальных
веществ, тогда и (∂σ/∂T)p > 0.
Исследования наночастиц алюминия
Приведенные выше утверждения и соотношения позволяют сделать вывод о
наличии у наночастиц избыточной энергии, обусловленной особенностями их
строения, что является следствием уменьшения размера частицы.
В работе Бабука В.А. и Салимуллина Р.М. «Наночастицы как компонент
высокоэнергетических конденсированных систем» были определены термодинамические
характеристики наночастиц (состоящих из различного количества молекул).
Для упрощения получения этих характеристик в указанной работе были
введены следующие допущения:
o Рассматривается макроскопическое количество наночастиц,
находящихся в равновесном состоянии.
o Отсутствует взаимодействие наночастиц как между собой, так и
с окружающей средой.
o Количество микрочастиц, входящих в состав наночастицы,
является фиксированным (заданным).
o Все микрочастицы, входящие в состав наночастицы, обладают
одинаковыми свойствами.
o В качестве размера наночастицы принимается радиус
эквивалентной сферы, описанной вокруг наночастицы.
o Свойства вещества наночастиц близки к свойствам плотной
жидкости.
o Парный потенциал взаимодействия зависит только от свойств
микрочастиц
Ниже кратко описан алгоритм расчета, используемый в указанной работе.
Для достижения равновесного состояния одна из термодинамических функций
должна быть минимальной. Учитывая заданные условия (достаточно низкие
температуры, молекулы почти неподвижны) такой функцией является потенциальная
энергия.
Задача состоит в следующем: необходимо найти такое пространственное
положение микрочастиц в наночастице, которое бы обеспечивало минимальное
значение потенциальной энергии. В качестве характерного размера наночастиц
используется радиальная координата (радиус эквивалентной сферы, описанной
вокруг наночастиц). [7]
Определяется минимум потенциальной энергии одной микрочастицы в
зависимости от радиальной координаты для каждой фазы. Радиус, на котором это
достигается есть равновесное расстояние. Этот расстояние определяют для каждой
фазы. Далее уточняется вид радиальной функции.
Радиальная функция - определяет характер взаимодействия между частицами,
в данном случае учитывает то обстоятельство, что взаимодействие между
молекулами происходит на близких расстояниях. Далее, с учетом равновесных
расстояний и плотной упаковки строится частица.
Удельная энтальпия продуктов сгорания определяется как сумма вещества
классической объемной фазы и разность удельной потенциальной энергии наночастиц
и удельной потенциальной энергии вещества классической объемной фазы.
Зная данные о строении наночастицы, можно определить ее термодинамические
характеристики.
|
n
|
13
|
20
|
40
|
60
|
|
ns
|
12
|
16
|
33
|
40
|
|
Rnp, нм
|
0.3001
|
0.4580
|
0.5518
|
0.6453
|
|
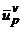 , Дж-2.29∙10-19 , Дж-2.29∙10-19
|
-2.48∙10-19
|
-3.30∙10-19
|
-3.40∙10-19
|
|
|
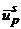 , Дж-1.51∙10-19-1.64∙10-19-2.08∙10-192.17∙10-19 , Дж-1.51∙10-19-1.64∙10-19-2.08∙10-192.17∙10-19
|
|
|
|
|
|
unp, Дж/кг
|
-3.51∙106
|
-4.03∙106
|
-5.12∙106
|
-5.66∙106
|
|
∆Н0f, пр Дж/кг
|
7.65∙106
|
7.13∙106
|
6.05∙106
|
5.5∙106
|
Таблица 1.1 Термодинамические характеристики наночастиц алюминия
Из таблицы видно, что по мере увеличения радиуса наночастицы Rnp , т.е. уменьшения параметра ns (количества молекул, находящихся на
поверхности частицы) энтальпия образования ∆H0f, пр существенно падает. И, наоборот, уменьшение размера частицы способствует
увеличению энтальпии ∆H0f, пр. То есть самой энергетически
выгодной является частица почти все молекулы которой находятся на поверхности,
самая маленькая.
ТРТ. Роль дисперсных компонентов.
Поскольку интересующий нас вопрос в рамках данного исследования -
возможности получения ракетного топлива, обладающего значительным избытком
энергии по сравнению со стандартным, рассмотрим, как же это можно сделать,
используя знания о строении и свойствах наночастиц, а также учитывая результаты
уже проведенных исследований.
Ракетное топливо - это источник энергии для ракетного двигателя. Ракетный
двигатель - это реактивный двигатель, задачей которого обычно является доставка
полезной массы на определенную дальность или высоту. Наиболее распространены химические
ракетные двигатели - двигатели, в которых применяются химические источники
энергии или химические топлива. Химическая энергия - энергия, выделяемая в ходе
химической реакции за счет уменьшения энергетических уровней молекул продуктов
реакции по сравнению с энергетическими уровнями атомов и молекул, вступающих в
реакцию.
В ходе таких реакций атомы одного вещества (окислитель) притягивают к
себе электроны, а атомы другого (горючее) отдают их. В результате происходит
взаимное переплетение электронных оболочек так, что некоторые электроны
оказываются одновременно на внешних оболочках двух атомов. Таким образом,
внешние электронные оболочки атомов в продуктах реакции оказываются более
заполненными, чем в реагирующих атомах. Поскольку заполнение внешней электронной
оболочки сопровождается падением энергетического уровня атома, продукты реакции
имеют более низкий энергетический уровень, чем исходные вещества. Разность этих
энергетических уровней и определяет величину химической энергии, выделяющейся
при реакции.
Наибольшими
тепловыми эффектами сопровождаются реакции горения, т.е. окисления различных
элементов кислородом или фтором, т.е. они являются окислителями. Топливо
химического ракетного двигателя является источником как тепловой энергии, так и
газообразного рабочего тела
<#"526824.files/image014.gif">
где
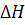
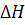 -
перепад энтальпий, характеризующий разность теплот реакций системы в условиях
камеры сгорания и выходного сечения сопла.
-
перепад энтальпий, характеризующий разность теплот реакций системы в условиях
камеры сгорания и выходного сечения сопла.
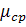
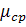 -
средняя молекулярная масса продуктов сгорания.
-
средняя молекулярная масса продуктов сгорания.
Роль
дисперсных компонентов:
Из
формулы 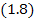
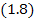 следует,
что
следует,
что 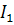
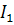 ~
~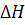
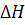 . То есть
единственным путем повышения энергоемкости топлива является повышение энтальпии
его образования.
. То есть
единственным путем повышения энергоемкости топлива является повышение энтальпии
его образования.
Как
уже известно из предыдущего параграфа, частицей, обладающей самой высокой энтальпией
образования является такая наночастица, почти все молекулы которой находятся на
поверхности. Таким образом, энтальпия образования любой нанодисперсной среды
выше, чем энтальпия образования стандартных веществ. Следовательно, введение
компонентов в топливо в нанодисперсном виде, позволит повысить его энергетику.
Нужно
заметить, что не все компоненты СТРТ можно ввести в виде наносред. Это возможно
для компонентов 1,3 и 4. Связующее горючее так ввести невозможно, так как его
задача - связывать все компоненты топлива в единую систему.
Применение
топлив с нанодисперсными компонентами кроме основного преимущества (высокой
энергетики топлива за счет повышения энтальпии его образования) имеет еще
несколько побочных, а именно:
1. Ведение компонента топлива в виде дисперсной фазы позволяет повысить
его термодинамическую реакционную способность, что повысит эффективность
прохождения всех химических реакций, следовательно, и уровень полноты сгорания
топлива, т.е. его эффективность.
. Наличие нанокомпонентов в топливе позволит снизить температуру его
воспламенения. [9]
Можно сделать вывод, что применение в топливах наноразмерных компонентов
связано с использованием энергии межмолекулярных связей вкупе с энергией
химических взаимодействий. Однако получение такого топлива связано с рядом еще
не решенных проблем. Одна из них - преждевременная коагуляция наночастиц,
обусловленная их высокой реакционной способностью.
Выводы по
главе
. Даны определения наноструктурам как уникальным объектам, введены
определения фазы и структуры, агрегатного состояния; обозначены различия между
ними. Перечислены некоторые области применения наноструктур.
. Выявлены особенности строения наноструктур, отличия их от
макросистем и молекул. Введены понятия поверхностного слоя и объемной фазы,
обозначены отличия. Приведены конкретные примеры кардинальной перемены свойств
материала при изменении размера. Объяснены причины интереса к наносистемам, как
к объектам будущего.
. Рассмотрены 2 способа получения наноструктур; кратко описаны
процессы и явления, сопровождающие каждый способ получения а также обозначено
их влияние на свойства будущих наноструктур.
. Приведены основные понятия и соотношения коллоидной химии,
обозначены отличия дисперсных систем от наносистем, рассмотрены процессы и
явления, происходящие в наноструктурах, объясняющие наличие в них избыточной
энергии. Доказано влияние размера частиц на их энергетические свойства на
примере алюминия. Оговорены преимущества и сложности применения ракетных топлив
на базе нанодисперсных компонентов.
Глава 2.
Анализ и выбор оборудования для изучения наночастиц
2.1
Характеристики наночастиц, описывающие дисперсность, состав, структуру. Обзор
методов измерения этих характеристик
Для того, чтобы с успехом использовать нанообъекты (в том числе и компоненты
топлива, введенные в нанодисперсном виде), необходимо подробно изучить
характеристики, описывающие их дисперсность, состав, структуру, внутреннее
строение, форму.
Из всех перечисленных характеристик наиболее важной для данного
исследования является дисперсность (распределение по размерам) наноструктуры:
дисперсность определяет энергетический потенциал структуры. Введем понятие
размера наночастицы. Поскольку такая частица не представляет собой в точности
какую-либо геометрическую фигуру, размер наночастицы будет определяться как
радиус (или диаметр) эквивалента сферы, т.е. сферы, описанной около нее.
На сегодняшний момент существуют следующие методы исследования наночастиц
(размером до 10нм):
§ Сканирующая электронная микроскопия;
§ Рентгено - дифракционный анализ;
§ рентгеновский фотоэлектронный спектроскопический анализ;
§ определение дисперсности по результатам взаимодействия зондирующего
излучения с объектом.
Перечисленные методы исследования позволяют определить все
вышеперечисленные характеристики. Рассмотрим их подробнее.
Сканирующая электронная микроскопия
Представляет собой исследование образца с помощью электронного
микроскопа.
Электронный микроскоп - это прибор, который позволяет получать сильно
увеличенное изображение объектов, используя для их освещения электроны.
Принцип действия сканирующего электронного микроскопа:
Электронный зонд в виде тонкого пучка электронов (диаметр пучка 10 нм)
сканирует участок образца точку за точкой. Электрический сигнал, возникающий
при бомбардировке объекта электронами пучка, используется для формирования
изображения на экране телевизионного кинескопа или электронно-лучевой трубки
(ЭЛТ), развертка которой синхронизирована с системой отклонения электронного
пучка. Первичный электронный луч (зонд) формируется в вакуумной колонке
(электронной пушке) электронного микроскопа. Электроны вылетают из
накаливаемого катода, и ускоряются электрическим полем напряжением 1-50 кВ. Луч
фокусируется тремя электромагнитными конденсорными линзами и с помощью
отклоняющих катушек сканируется по образцу.
Преимущества метода:
§ самый прямой и простой метод измерения
§ высокое увеличение (в десятки тысяч раз), т.е. возможность подробно
рассмотреть
очень маленькие объекты
Результат: есть возможность получать изображение поверхности образца,
т.е. можно увидеть форму наночастиц, структуру нанообъекта на отдельном
небольшом участке, но нет возможности вычислить, например, распределение по
размерам в данном нанообъекте, т.к. детальное исследование всех частиц займет
очень много времени.
Таким образом, с помощью электронной микроскопии можно определить форму,
размер некоторых частиц, но нельзя делать выводы о внутреннем строении всего
нанообъекта.
Рентгено-дифракционный анализ
Методы
исследования структуры вещества по распределению в пространстве и
интенсивностям рассеянного на анализируемом объекте рентгеновского излучения. В
основе метода лежит взаимодействие рентгеновского излучения с электронами
вещества, в результате которого возникает дифракция рентгеновских лучей
<#"526824.files/image019.gif">
Рис. 2.1 сканирующий электронный микроскоп SuperScan SS-550
.2.2 Распределение частиц по размерам. Horiba LA-950 - универсальный лазерный экспресс анализатор
распределения размеров частиц.
Технология использования метода.
Конструкция прибора включает в себя циркуляционную систему и оптическую
систему + программное обеспечение. Циркуляционная система служит для подготовки
образца к измерению, оптическая система - для самого измерения. Образец
находится в резервуаре. При нажатии команды “Fill” система циркуляции с помощью насоса немедленно
наполняет резервуар жидкой средой для измерения. На движущуюся «клетку»
подается определенное количество образца (контролируется датчиком). На образец
поступает свет от лазера (той или иной длины волны). Свет, рассеянный образцом
поступает на детекторы (какой-то из нескольких, расположенных под углами к
«клетке»), и затем на основной. Оттуда - на блок обработки ПО. Производится
необходимый расчет.
Достоинства метода
Широкий диапазон измерений(0.01-3000микрон), высокая точность (+_ 0.6%) и
репродуктивность (+_0.1%) или даже меньше гарантирована калибровкой с
использованием отслеживающих стандартных частиц NIST возможность исследовать токсичные образцы и
использовать токсичные распылители.
Оптическая система: Для измерения достаточно больших и маленьких частиц
используют разные длины волн источника. По данным эксперимента видно, что при
использовании лазерного света (λ=650нм) не видно разницы между частицами
диаметром 50 нм и 70 нм, их индикатрисы рассеяния сливаются.
Однако, при использовании диода (λ=405нм) разница видна четко. Преимущество
использования источников с разной длиной волн в создании инструмента, который
способен на измерение в широком диапазоне с высокой точностью.
Система циркуляции: циркуляционный насос имеет существенную мощность,
чтобы циркулировали все частицы. Это дает возможность системе управлять
образцами любого размера и веса. Насос 15-ти уровневый. Ультразвуковой зонд
может работать на одном из 7-ми уровней, в зависимости от образца. Кроме того,
циркуляционная система отличается высокой воспроизводимостью: от очистки до
демонстрации данных - 1 минута.
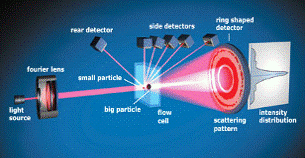
Рис. 2.2 Принцип действия Horiba
LA-950
.2.3
Определение химического состава. JPS-9010TR - фотоэлектронный спектрометр фирмы JEOL.
Сущность метода: фотоэлектронная спектроскопия.
Технология:
Производится травление образца пучком положительных ионов, которые
распыляет электронная пушка. Явление фотоэффекта. Пересчет измеряемых данных.
Анализ спектров. Получение данных о химическом составе в образце.
Достоинства:
Ионные пушки позволяют анализировать как атомные слои поверхности
различной толщины, так и слои образца размером порядка микрона. Камера
наблюдения образца и камера, где образец подвергается травлению, отделены друг
от друга вакуумным затвором. Это защищает от загрязнения в результате
распыления и облегчает получение сверхвысокого вакуума.
Данная серия спектрометров удобна в управлении, снабжена программным
обеспечением для MS Windows ME/2000/XP, что упрощает измерения и получение данных,
и позволяет получать более точную информацию.
Версия модели JPS-9010TR позволяет проводить сверхточный анализ самых
верхних слоев поверхности образца (глубина проникновения излучения много меньше
1 мкм), за счет уменьшения угла падения рентгеновских лучей. Прибор оснащен
высокоскоростной ионной пушкой, камерой пробоподготовки и другими
системами.[13]
Новейшие разработки крупнейших фирм-производителей приборов для
исследования наночастиц позволяют реализовать измерительно-исследовательский
комплекс с помощью которого возможно определить особенности их структуры и
свойств.

Рис. 2.3 JPS-9010TR - фотоэлектронный спектрометр фирмы JEOL
Технология определения характеристик наночастиц:
1. Начальный этап исследования - изучение образца с помощью
электронного сканирующего микроскопа SuperScan SS-550 фирмы Shimadzu: образец помещается на предметный
столик и исследуется. Увеличенное в 20-300000 изображение наноструктуры можно
наблюдать на мониторе компьютера, входящего в комплект. Разрешение прибора
позволяет увидеть наночастицы размером до 3.5 нм. Подготовка образца не
требуется, так как прибор имеет дополнительную опцию - система наблюдения при
низком вакууме (1-270 Пa) для непроводящих образцов.
На данном этапе происходит знакомство с внутренним строением, структурой
образца, производится приблизительная оценка размеров частиц в нанообъекте на
примере нескольких частиц. Также на этом этапе исследуется форма частиц.
. Следующий этап исследования (более детальный анализ образца)
оценка его химического состава с помощью JPS-9010TR -
фотоэлектронного спектрометра фирмы JEOL. В отдельной камере прибора образец подвергается травлению пучком ионов.
Электроны, вытравленные светом, поступают на блок обработки. Производится
оценка энергий связи электронов, используя уравнение фотоэффекта. По спектрам
производится химический анализ структуры.
. Заключительный этап исследования - определение ключевой для
данной работы характеристики наноструктуры - дисперсности (распределения по
размерам). Для проведения опыта образец, используемый в двух других,
измельчается. Опыт проводится в универсальном лазерном экспресс анализаторе
распределения размеров частиц Horiba
LA-950. Образец помещается в резервуар, рассеивается с помощью ультразвукового
зонда. Проводится эксперимент, состоящий в рассеянии наночастицами света, поступающего
от двух источников (с длинами волн 650нм и 450нм). Рассеянный свет попадает на
датчики, производится обработка данных на компьютере, строятся диаграммы
рассеяния. По теории Ми через интенсивности рассеянного света определяется
распределение наночастиц по размерам во всем нанообъекте, т.е. дисперсность
структуры.
Выводы по
главе
o Перечислены и объяснены основные методы измерения
характеристик наночастиц.
o Произведен анализ оборудования, базирующегося на этих
методах, и описана методика исследования наноструктур с помощью этого
оборудования.
Таким образом, используя данную методику с помощью приведенного комплекса
можно определить форму, строение, химический состав и распределение по размерам
частиц наноструктуры. Исследованию подвергаются частицы, размером не меньше 10
нм. Однако это обстоятельство является приемлемым, так как уже в диапазоне 20 -
10 нм необычные свойства наноструктур, описанные в предыдущей главе, начинают
проявляться.
Ключевым моментом данного исследования является определение дисперсности
и распределения наночастиц по размерам, так как (как уже было выяснено ранее)
именно эти характеристики определяют энергетический потенциал наноструктуры. То
есть обладая достоверной информацией о дисперсности того или иного образца,
можно сделать вывод об его энергетических способностях, что очень важно в
рамках данного исследования. Поэтому методика предполагает определение
вышеуказанных характеристик несколькими разными способами. Используя данные о
составе и структуре нанообъекта также можно оценить текущее энергетическое
состояние объекта через энергию химических связей. Данные о форме наночастиц
важны для оценки их поверхностной энергии (способности к коагуляции) в данное
время.
Тем не менее некоторые вопросы, связанные с изучением наночастиц остаются
открытыми. Сканирующая микроскопия, например, позволяет увидеть форму частиц,
но не позволяет составить распределение частиц по размерам, с ее помощью нельзя
составить полный анализ о внутреннем строении, так как исследования электронным
микроскопом имеют случайный характер. Химический анализ частиц определяет
глубина проникновения ионов. А поскольку метод фотоэлектронной спектроскопии
основан на явлении фотоэффекта, он имеет, скорее, поверхностный характер.
Глава 3. Разработка расчетных средств для прогнозирования калорийности
ВЭМ
Использование высокоэнергетических материалов в различных областях науки
и техники позволяет не только резко повысить эффективность и экономичность
многих технологий, но и создавать принципиально новые материалы, изделия и
технологические процессы. ВЭМ применяются при разведке и добыче нефти (газа), в
машиностроении, космической технике, при получении новых сверхтвердых
материалов. ВЭМ представляют собой: топлива, пороха, взрывчатые вещества. [15]
При использовании ВЭМ происходят химические реакции, в результате которых
выделяется энергия. Следовательно, важной характеристикой таких материалов
является тепловой эффект реакции - теплота (энергия), которая выделяется в ходе
химической реакции или калорийность ВЭМ - запас энергии, приходящийся на 1 кг
ВЭМ(складывается из химической энергии и начального теплосодержания 1 кг ВЭМ).
В этой главе описана методика прогнозирования калорийности ВЭМ. То есть с
помощью нижеизложенных методов можно рассчитать сколько теплоты (энергии)
выделяется при сгорании (взрыве) того или иного ВЭМ(если известен его состав).
Имея возможность рассчитать энергетику материала (зная калорийность того или
иного высокоэнергетического материала) материала можно сделать вывод о том, где
и как целесообразней его применить.
.1 Термодинамический метод
.1.1 Описание метода
Процедура расчета калорийности основана на использовании
термодинамического метода, который позволяет определять характеристики состава
продуктов сгорания (взрыва) ВЭМ и температуры в камере сгорания ракетного
двигателя (либо в камере, где тестируют взрывчатое вещество). Данные значения
являются основой для принятия решений и дальнейших расчетов. Использование
термодинамического метода исследования обеспечивает определение всех характеристик
продуктов сгорания (взрыва) ВЭМ в рамках идеализации процессов горения и
истечения. Этот метод является обязательным предварительным инструментом при
принятии решений по созданию ракетных топлив.
В связи со спецификой работы рассматриваются химические ракетные топлива
и процессы, протекающие в камере сгорания ракетного двигателя.
Процессы в камере сгорания двигателя: Основным процессом, определяющим
явления превращения энергии в камере сгорания, является горение топлива.
Процесс горения схематично можно представить следующим образом.
T
=> Г1 + … + Гn +
K1 + … + Km + П1 + …+ Пm + … + C + H + …
И1q1 + … + Иlql + E
где: Т - топливо; Гi - i-тое молекулярное газообразное
вещество (МГВ); Кj - j-тое конденсированное вещество (КВ); Пj
- насыщенный пар j-того КВ; С, H, O, - атомарные газообразные вещества (АГВ); qk
- кратность ионизации (qk > 0 для положительных ионов и qk <0
для отрицательных ионов); Ek-qk - k-тый отрицательный ион (ОИ); Ek+qk - k-тый положительный ион (ПИ); Е -
электронный газ.
При расчете применительно к камере сгорания традиционно делаются
следующие допущения о процессе сгорания.
1. Смесь продуктов сгорания является равновесной.
2. Горение осуществляется при постоянном давлении и отсутствии
теплообмена с окружающей средой в стационарном режиме.
. Смесь газообразных продуктов сгорания является идеальным газом.
. Конденсированные продукты сгорания не образуют растворы, как
между собой, так и с газообразными продуктами.
. Кинетическая энергия продуктов сгорания пренебрежимо мала в
сравнении с энергией теплового движения.
Рассмотрим камеру сгорания, как открытую термодинамическую систему (ТДС)
(рис.3.1.1). Особенностью этой системы является изменение во времени ее объема
вследствие сгорания топлива.

Рис.3.1.1 Схема, иллюстрирующая сгорание топлива (Х - пространственная
координата, т-т и о-о контрольные поверхности, соответствующие исходному
топливу и конечным продуктам сгорания).
Уравнения, описывающие изменение во времени энергии и вещества данной ТДС
в постановке Эйлера имеют следующий вид.


где:

 - приход
вещества в систему вследствие сгорания топлива;
- приход
вещества в систему вследствие сгорания топлива; 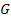
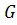 -
расход вещества из системы вследствие осуществления истечения;
-
расход вещества из системы вследствие осуществления истечения; 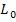
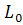 - работа
объемной деформации;
- работа
объемной деформации;

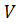
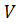 - объем
ТДС;
- объем
ТДС; 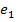
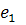 ,
, 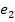
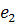 - удельный
запас энергии вещества, подводимого в систему и отводимого из нее:
- удельный
запас энергии вещества, подводимого в систему и отводимого из нее:
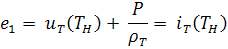
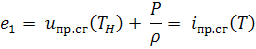
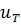
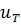 ,
, 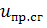
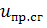 -
удельная внутренняя энергия топлива и продуктов сгорания;
-
удельная внутренняя энергия топлива и продуктов сгорания; 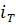
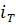 ,
, 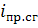
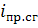 . - удельная энтальпия топлива и продуктов сгорания;
. - удельная энтальпия топлива и продуктов сгорания; 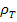
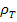 ,
, 
 -
плотность топлива и продуктов сгорания;
-
плотность топлива и продуктов сгорания;

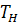 ,
,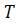
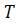 -
начальная температура топлива и температура продуктов сгорания;
-
начальная температура топлива и температура продуктов сгорания;
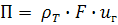

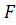 -
площадь поверхности горения;
-
площадь поверхности горения; 
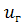 -
линейная скорость горения топлива.
-
линейная скорость горения топлива.
С
использованием стационарного приближения процесса горения уравнения
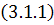 -
-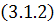
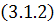 преобразуются к следующему виду.
преобразуются к следующему виду.

и

 Очевидным
следствием второго закона термодинамики с учетом принятых допущений является
следующее утверждение:
Очевидным
следствием второго закона термодинамики с учетом принятых допущений является
следующее утверждение:
ds ³ 0 (3.1.5)- удельная энтропия вещества ТДС.
В
соответствие с уравнениями 
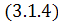 -
-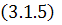
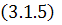 характер
изменения основных термодинамических функций соответствует показанному на рис.
3.1.2.
характер
изменения основных термодинамических функций соответствует показанному на рис.
3.1.2.
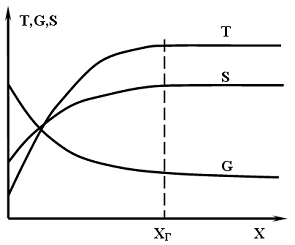
Рис.
3.1.2 Обобщенные зависимости температуры (Т), энергии Гиббса (G) и энтропии (S)
продуктов сгорания в процессе горения от пространственной координаты (Xг -
расстояние, на котором завершается процесс горения)
Для
решения задачи определения параметров равновесной смеси продуктов сгорания
могут быть использованы различные методы. Широкое распространение получили
методы, базирующиеся на использовании оптимизационной процедуры, а также
численного интегрирования систем обыкновенных дифференциальных уравнений. Ниже
рассматривается используемый метод - метод фиксированных состояний.
В
основе метода лежит процедура, в соответствие с которой для ряда фиксированных
температур определяется состав равновесной смеси и ее энтальпия. Температура,
при которой имеет место равенство энтальпий топлива и продуктов сгорания
считается истинной. Таким образом, основным содержанием используемой
математической модели является математическая модель формирования состава
равновесной смеси при постоянных давлении и температуре. [16]
.1.2
Математическая модель определения калорийности топлива
Задача
определения калорийности подразделяется на две задачи: первая - нахождение
состава газовой смеси и удельной энтальпии продуктов сгорания, вторая -
нахождение калорийности топлива с помощью этих величин.
Ниже
описана программа, с помощью которой производится расчет калорийности.
.1.2.1
Составление системы уравнений для нахождения параметров состава газовой смеси и
энтальпии продуктов сгорания.
Для
определения вышеуказанных параметров используется программа, основанная на
решении системы уравнений трех видов: уравнения материального баланса,
уравнения, выражающего закон действующих масс и уравнения, выражающие закон
Дальтона.
1. Уравнение материального баланса в общем виде выглядит так:
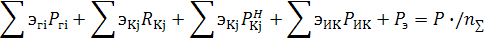
где

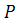 -
полное давление,
-
полное давление,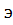
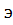 -
коэффициент в условной формуле при данном элементе,
-
коэффициент в условной формуле при данном элементе, 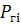
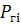 -
парциальное давление i-го МГВ (сумма по МГВ),
-
парциальное давление i-го МГВ (сумма по МГВ), 
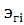 - число
молей элемента в одном моле i-го МГВ.
- число
молей элемента в одном моле i-го МГВ.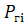
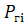
 - условное парциальное давление j-го
КВ.
- условное парциальное давление j-го
КВ. 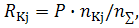
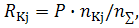
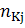
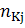 - число
молей j-го КВ в 1 кг продуктов сгорания,
- число
молей j-го КВ в 1 кг продуктов сгорания, 
 - число молей газообразных продуктов в 1 кг продуктов
сгорания,
- число молей газообразных продуктов в 1 кг продуктов
сгорания,

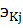 - число
молей элемента в одном моле j-го КВ,
- число
молей элемента в одном моле j-го КВ, 
 -
давление насыщающих паров j-го КВ,
-
давление насыщающих паров j-го КВ, 
 -
парциальное давление k-го иона,
-
парциальное давление k-го иона, 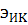
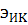 - число
молей элемента в одном моле k-го иона,
- число
молей элемента в одном моле k-го иона,
 -
парциальное давление атомарного элемента.
-
парциальное давление атомарного элемента.
2. Уравнения, выражающие закон действующих масс (уравнения
равновесия).
В равновесной смеси продуктов химического взаимодействия протекает
большое количество равновесных химических реакций, которые могут быть выражены
через, так называемые, независимые химические реакции. В качестве подобных
реакций могут быть выбраны, например, реакции диссоциации МГВ, КВ, ОИ, и ПИ на
АГВ и электронный газ.
Уравнения диссоциации и соответствующие уравнения равновесия будут иметь
следующий вид:
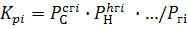
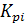
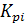 -
константа равновесия реакции диссоциации.
-
константа равновесия реакции диссоциации.
Число
этих уравнений должно быть равно количеству МГВ, КВ, ОИ, ПИ.
3. Уравнения, выражающие закон Дальтона.
Общий вид уравнения:
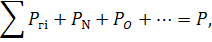
где суммирование производится по МГВ.
Решение
системы всех уравнений позволяет найти параметры состава смеси, а именно,
парциальные давления МГВ, АГВ, 
 , а также
энтальпии продуктов сгорания, необходимые для расчета калорийности топлива:
, а также
энтальпии продуктов сгорания, необходимые для расчета калорийности топлива:
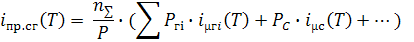
где
суммирование производится по МГВ, 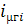
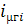 -
мольные энтальпии газов.
-
мольные энтальпии газов.
.1.2.2
Метод численного решения системы уравнений.
Для
определения параметров состава необходимо решение системы из  n+m+k +
n+m+k + 
 1
трансцендентных уравнений (
1
трансцендентных уравнений (
 -
количество элементов в составе топлива). Рассмотрим принятый метод решения для
случая, когда в продуктах сгорания отсутствует низкотемпературная плазма.
-
количество элементов в составе топлива). Рассмотрим принятый метод решения для
случая, когда в продуктах сгорания отсутствует низкотемпературная плазма.
Для
решения системы трансцендентных уравнений используется метод Ньютона.
Пусть
рассматривается система из 
 алгебраических
уравнений, следующего вида:
алгебраических
уравнений, следующего вида:
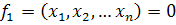
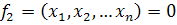
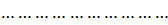
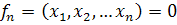
При
значениях аргументов 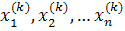
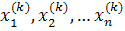
 осуществляется
линеаризация функций
осуществляется
линеаризация функций 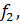
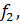 в
результате система уравнений превращается в систему линейных алгебраических
уравнений относительно
в
результате система уравнений превращается в систему линейных алгебраических
уравнений относительно 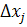
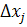 .
.
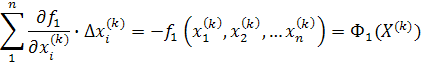
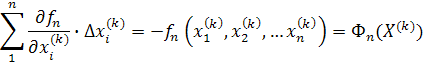
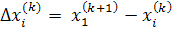
Расчет
с использованием системы линейных алгебраических уравнений заканчивается тогда,
когда нормы двух векторов 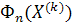
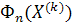 и
и 
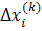 ) станут
меньше некоторой малой величины (d).
) станут
меньше некоторой малой величины (d).
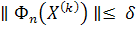
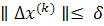
Предварительно
с целью уменьшения отличия в значениях искомых параметров осуществляется
логарифмирование уравнений данной системы. При этом они принимают следующий
вид:
Уравнения
материального баланса:
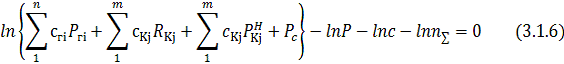

Уравнения
равновесия:
 =
1, 2, … n
=
1, 2, … n
 = 1, 2, …
n
= 1, 2, …
n
Уравнение,
выражающее закон Дальтона:
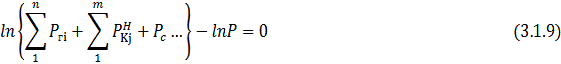
После
проведения необходимых преобразований уравнения для отыскания поправок (∆),
обеспечивающих определение логарифмов исковых величин, имеют следующий вид:
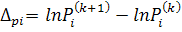
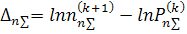
Линеаризованные
уравнения материального баланса:
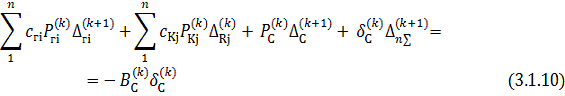
где:
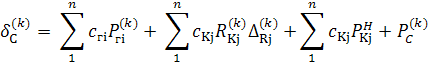
(
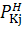 является
функцией только температуры)
является
функцией только температуры)
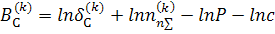
Линеаризованные
уравнения равновесия:
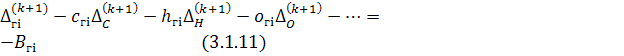
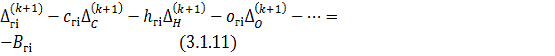
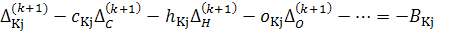
где:
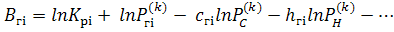
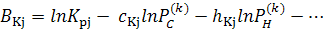
Линеаризованное уравнение, выражающее закон Дальтона:
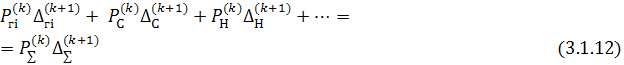
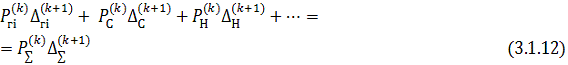
где:
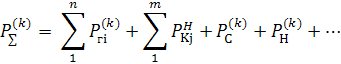
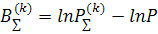
Расположим
уравнения для поправок в следующей последовательности:
· линеаризованные уравнения равновесия для МГВ;
· линеаризованные уравнения равновесия для КВ;
· линеаризованные уравнения материального баланса;
· линеаризованное уравнение, выражающее закон Дальтона.
В этом случае матрица для коэффициентов при неизвестных, а также
свободных членов примет вид соответствующий приведенному в приложении.
Система линейных алгебраических уравнений с учетом разбиения этой матрицы
может быть записана в следующем виде.

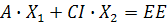
где:
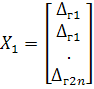
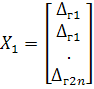
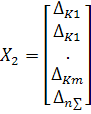
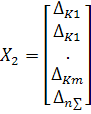

После
преобразований система решаемых уравнений приобретает следующий вид:

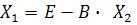
При
использовании метода Ньютона в обычной форме сходимость решения не
гарантируется. Для решения этой проблемы используется специальный прием,
который заключается в разложении функций в ряд Тейлора на частных интервалах.
Пусть
необходимо найти решение следующего уравнения 𝑓(
 )=0.
)=0.
Введем
обозначения:

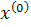 ,
, 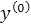
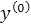 -
значения неизвестной и функции 𝑓 в
нулевом приближении.
-
значения неизвестной и функции 𝑓 в
нулевом приближении.
Будем
искать поправку 
 ,
позволяющую найти значение аргумента, при котором функция уменьшается на
некоторую величину
,
позволяющую найти значение аргумента, при котором функция уменьшается на
некоторую величину 
 .
.
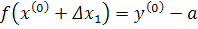
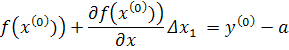
Таким
образом,


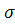 -
коэффициент шага;
-
коэффициент шага;
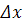
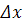 -
поправка при применении метода Ньютона в обычной форме.
-
поправка при применении метода Ньютона в обычной форме.
Для
системы уравнений вида 
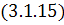 величину
величину
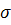
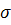 можно
определить с помощью следующего выражения:
можно
определить с помощью следующего выражения:


 -
эмпирический коэффициент (
-
эмпирический коэффициент (
 ~0,1-0,5);
~0,1-0,5);
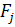
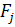 -
значение левой части j-того уравнения системы
-
значение левой части j-того уравнения системы 
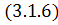 -
- 

Описанный
метод решения обладает следующими достоинствами:
· сравнительно малым временем численной реализации решения
(число арифметических действий при численном решении системы линейных
алгебраических уравнений пропорционально количеству уравнений в степени 3);
· возможностью создания универсальных алгоритмов расчета пригодных для
произвольного состава продуктов сгорания;
· надежностью получения решения.
Следует отметить, что рассмотренный метод может быть с успехом применен и
для расчета при наличии продуктов ионизации. В этом случае считается, что
топливо состоит из положительных ионов с максимальной кратностью ионизации и
электронного газа. Это обстоятельство находит свое отражение в записи условной
формулы топлива. Данные вещества в рамках приведенного описания выполняют роль
АГВ, а МГВ, АГВ и ОИ - МГВ.
.1.3 Калорийность топлив
Калорийность топлива (Е) определяется следующим образом:
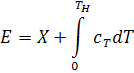

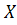 -
химическая энергия топлива
-
химическая энергия топлива

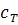 -
удельная теплоемкость топлива
-
удельная теплоемкость топлива
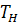
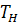 -
начальная температура топлива
-
начальная температура топлива
Величина

 определяется
изменением энергии Гиббса при осуществлении процесса горения (
определяется
изменением энергии Гиббса при осуществлении процесса горения (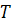
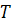 =const,
p=const). При
=const,
p=const). При 
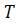 =0 °К это изменение эквивалентно изменению энтальпии, т.е.
=0 °К это изменение эквивалентно изменению энтальпии, т.е.
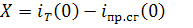
Или
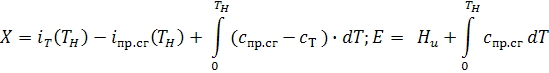

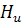 -
теплотворная способность топлива (количество тепла (по абсолютной величине),
выделяющегося при сгорании единицы массы топлива (
-
теплотворная способность топлива (количество тепла (по абсолютной величине),
выделяющегося при сгорании единицы массы топлива (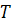
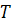
 =
=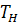
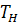
 , p=1
атм) при условии, что газообразные продукты не конденсируются).
, p=1
атм) при условии, что газообразные продукты не конденсируются).
Если
подставить выражение для 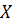
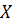
 в формулу для калорийности топлива, получим
следующее:
в формулу для калорийности топлива, получим
следующее:
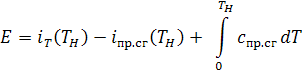

С
использованием стационарного приближения процесса горения можно записать, что:
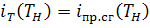
Тогда
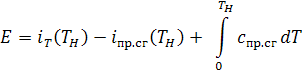
Поскольку
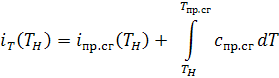
Подставив
это выражение в формулу для 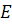
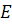
 , получим:
, получим:
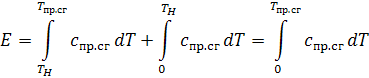
По
этой формуле можно оценить калорийность топлива, пользуясь термодинамическими
функциями-энтальпиями, если известен состав продуктов сгорания, т.е. число
молей каждого компонента в 1кг продуктов сгорания nj
или массовая доля компонента gj. Энтальпия продуктов сгорания равна
Δ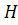
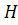
 пр = ∑
nj∙Δ
пр = ∑
nj∙Δ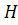
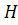
 j = ∑1000∙ gj∙Δ
j = ∑1000∙ gj∙Δ
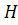 j
/μj
, где
j
/μj
, где
μj
- молекулярный вес j - го компонента [17]
.1.3.2
Оценка калорийности топлива
Оценка
калорийности топлива осуществляется в 2 этапа:
1. Нахождение истинной температуры продуктов сгорания (температура,
при которой удельная энтальпия топлива с точностью до 1% равна удельной
энтальпии продуктов сгорания).
. Нахождение калорийности топлива.
Калорийность
топлива (
 )
определяется следующим образом:
)
определяется следующим образом:

Где

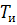 -
истинная температура для определенного топлива.
-
истинная температура для определенного топлива.
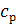
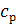 -
удельная теплоемкость продуктов сгорания при постоянном давлении.
-
удельная теплоемкость продуктов сгорания при постоянном давлении.


 - температура.
- температура.
Удельная
теплоемкость продуктов сгорания 
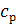 есть
производная энтальпии продуктов сгорания топлива по температуре:
есть
производная энтальпии продуктов сгорания топлива по температуре:
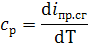

где

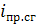 -
удельная энтальпия продуктов сгорания топлива
-
удельная энтальпия продуктов сгорания топлива
Оценить
калорийность топлива можно численно взяв интеграл 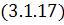
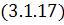 .
.
Алгоритм
расчета калорийности топлива:
.
Выполняется подбор истинной температуры для данного топлива.
.
Исходя из величины истинной температуры продуктов сгорания выбирается шаг по
температуре 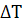
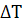
 для вычисления
для вычисления 
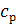 . С
помощью шага
. С
помощью шага 
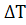 производится
нахождение расчетных точек.
производится
нахождение расчетных точек.
.
Для каждого значения температуры вычисляется значение энтальпии продуктов
сгорания данного топлива 
 .
.
.
Производится вычисление удельной теплоемкости продуктов сгорания 
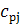 в каждой
из расчетных точек:
в каждой
из расчетных точек:
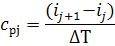

 -
энтальпия продуктов сгорания топлива, соответствующая текущей расчетной точке.
-
энтальпия продуктов сгорания топлива, соответствующая текущей расчетной точке.

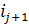 - энтальпия продуктов сгорания топлива,
соответствующая следующей расчетной точке.
- энтальпия продуктов сгорания топлива,
соответствующая следующей расчетной точке.
.Строятся
и анализируются зависимости величин 
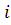 и
и 
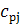 от
температуры.
от
температуры.
.Производится
приблизительная оценка калорийности топлива по формуле:

.1.3.2
Пример
В
качестве примера рассмотрим оценку калорийности топлива с условной формулой N9.2721O34.23H31.397C24.23
и энтальпией 
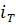 = -2.44∙106
Дж/кг.
= -2.44∙106
Дж/кг.
.
Истинной температурой для этого топлива является 
 = 2040К,
при которой
= 2040К,
при которой

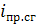 =
= 
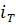 = -2.44∙106
Дж/кг.
= -2.44∙106
Дж/кг.
.
Выбираем шаг 
 =50К,
находим расчетные точки: 1т .
=50К,
находим расчетные точки: 1т .
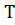 =750К
(ниже этой температуры производить расчет не имеет смысла, т.к. вклад в
калорийность невелик по сравнению с наиболее высокотемпературным участком); 2т.
=750К
(ниже этой температуры производить расчет не имеет смысла, т.к. вклад в
калорийность невелик по сравнению с наиболее высокотемпературным участком); 2т.

 =800К;
3т.
=800К;
3т. 
 =850К …
посл.т.
=850К …
посл.т. 
 =2040К
=2040К
.
Приведены значения энтальпий продуктов сгорания первых четырех расчетных точек:
т.
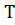 =750К
=750К 
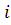 =-4.82∙106
Дж/кг.
=-4.82∙106
Дж/кг.
т.
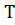 =800К
=800К 
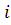 =-4.72∙106
Дж/кг.
=-4.72∙106
Дж/кг.
т.
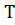 =850К
=850К 
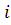 =-4.62∙106
Дж/кг.
=-4.62∙106
Дж/кг.
т.
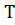 =900К
=900К 
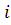 =-4.52∙106
Дж/кг
=-4.52∙106
Дж/кг
…………………………………………………..
Посл.т.

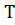 =2040К
=2040К 
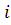 = -2.44∙106
Дж/кг.
= -2.44∙106
Дж/кг.
.
Приведены значения удельной теплоемкости продуктов сгорания для первых трех
расчетных точек:
В
данном случае удельные теплоемкости для всех расчетных точек будут равны

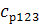 =(-4.72-(-4.82))∙106/50=(-4.62-(-4.72))∙106/50=(-4.52-(-4.62))∙106/50=2000
Дж/кг∙K
=(-4.72-(-4.82))∙106/50=(-4.62-(-4.72))∙106/50=(-4.52-(-4.62))∙106/50=2000
Дж/кг∙K
.
На рисунках 3.1.3 и 3.1.4 приведены зависимости удельной энтальпии продуктов
сгорания и удельной теплоемкости продуктов сгорания от температуры (
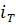 ),
), 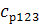
 (
(
 )).
)).
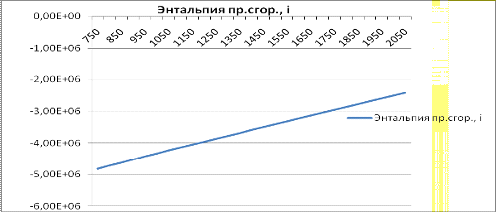
Рис. 3.1.3 Зависимость удельной энтальпии продуктов сгорания от температуры
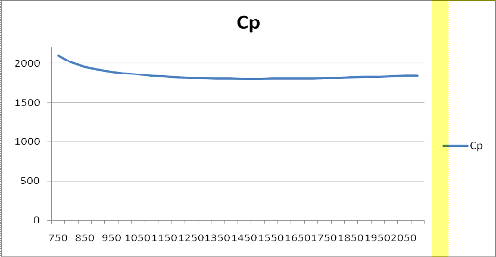
Рис.3.1.4.Зависимость удельной теплоемкости продуктов сгорания от
температуры
Выводы
- Энтальпия продуктов сгорания с повышением температуры растет,
причем зависимость почти линейная.
Теплоемкоcть
газовой смеси: зависимость теплоемкости от температуры неоднозначная.
На первом участке (750 - 1450К) происходит падение теплоемкости с ростом
температуры
На втором участке (1450 - 2100 К) теплоемкость начинает плавно расти.
Во всем диапазоне температур теплоемкость меняется незначительно.
По законам термодинамики теплоемкость в зависимости от температуры для
отдельного газа должна только плавно расти (то есть наличие второго участка не
вызывает вопросов). Поскольку речь идет о газовой смеси, можно сделать
предположение о том, что наличие
первого участка - следствие взаимодействия газов между собой (то есть
химических реакций, которые происходят между газами), т.о. уменьшение
теплоемкости связано с изменением состава смеси. Вывод об изменении состава
газовой смеси можно сделать используя данные о
парциальных давлениях продуктов сгорания топлива. Найдем количество молей
в 1кг продуктов сгорания тех веществ, вклад которых в смесь наиболее
существенен и представим их в таблице 1.Вычисления произведем по формуле
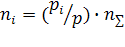
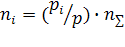
 где
где 
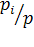 -
отношения парциальных давлений продуктов сгорания топлива к давлению смеси,
-
отношения парциальных давлений продуктов сгорания топлива к давлению смеси, 
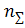 -
число молей газообразных продуктов в 1 кг продуктов сгорания топлива.
-
число молей газообразных продуктов в 1 кг продуктов сгорания топлива.
Таблица3.1.
Количество молей в 1кг продуктов сгорания веществ, вклад которых в теплоемкость
наиболее существенен для температур 750К и 1450К
|
Температура смеси
|
750К
|
1450К
|
|
Количество молей в 1 кг
продуктов сгорания, 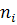 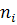
|
|
|
|
H2 Н2О N2
NH3 CO CO2
|
13,67 1,32 4,41 0,441 15,44
8,82
|
9,81 5,35 4,46 0,0045 19,62
4,014
|
Рассмотрим
газы, которые оказывают наибольшее влияние на изменение теплоемкости продуктов
сгорания топлива(H2, N2, CO, CO2, Н2О).
Из таблицы видно, что количество молей H2 в 1 кг продуктов сгорания уменьшается на 3.9 единиц,
для N2 -
уменьшается на 0.05 единиц, для CO же увеличивается на 4.2 единицы - уменьшение и
увеличение 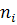
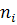 приблизительно
в равной степени - не влияют на теплоемкость. Для CO2 параметр
приблизительно
в равной степени - не влияют на теплоемкость. Для CO2 параметр 
 уменьшается на 4.8 единиц, для Н2О
уменьшается на 4.8 единиц, для Н2О 
 увеличивается
на 4 единицы, т.е. теплоемкость уменьшится. К тому же, учитывая, что мольные
теплоемкости этих веществ при температуре большей, чем 900 К равны 54,3 и 39,3
соответственно, а также формулу
увеличивается
на 4 единицы, т.е. теплоемкость уменьшится. К тому же, учитывая, что мольные
теплоемкости этих веществ при температуре большей, чем 900 К равны 54,3 и 39,3
соответственно, а также формулу 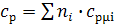
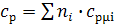
 можно утверждать, что общая теплоемкость продуктов
сгорания уменьшится вследствие падения
можно утверждать, что общая теплоемкость продуктов
сгорания уменьшится вследствие падения 
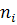 СO2, нежели увеличится вследствие роста
СO2, нежели увеличится вследствие роста 
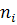 Н2О,
чем и обусловлено наличие первого участка.
Н2О,
чем и обусловлено наличие первого участка.
.
В соответствии с формулой (3.1.18) произведем оценку калорийности данного
топлива:
E= (2000∙3
+ 1800∙24)∙50 = 2.4∙106 Дж/кг
.2
Программные средства
Для
автоматизации оценки калорийности топлива необходима соответствующая программа.
Алгоритм
нахождения оценочного значения калорийности должен состоять из двух частей.
.
Нахождение истинной температуры для выбранного топлива.
.
Расчет калорийности этого топлива.
.2.1
Информация об исследуемом топливе. Файл исходных данных.
Перед
произведением расчета составляется файл исходных данных, в котором содержится
информация об исследуемом топливе.
В
данном случае (для топлива с условной формулой N9.2721O34.23H31.397C24.23) файл исходных данных выглядит так:
NS P0 E R0 CK
.00 40. 1E-3 8.314 0.01M K
14
0 4ИВ R РАЗМЕРНОСТИ М
МАССИВ
W2 РАЗМЕРНОСТИ M*KАССИВ Р РАЗМЕРНОСТИ N
.67
6.67 6.67 6.67 1.67 1.67 1.67 1.67 1.67 1.67 1.67 1.67 1.67 1.67АССИВ
Р1 РАЗМЕРНОСТИ К
.01
0.01 0.01 0.01АССИВ C РАЗМЕРНОСТИ К
.2721
34.23 31.397 24.23
МАССИВ
W1 РАЗМЕРНОСТИ N*K
0
2 0
1
2 0
1
1 0
0
0 0
1
0 0
1
0 0
0
2 0
0
3 0
1
0 1
2
0 1
0
1 1
0
2 1
0
3 1
0
1 0АССИВ H РАЗМЕРНОСТИ М+K+N*9
.782816
-2119.4816 7476.2362 -1133.0154 1070.0343 -375.27906 69.808944 -6.7118939
0.26221123
.6277
-60008.456 7369.7266 504.14536 1003.769 -481.74652 102.47379 -10.692381
0.44473991
.560373
7185.7819 7514.0699 -1193.6487 1225.4837 -466.28289 92.951841 -9.5273706
0.39463884
.722143
-1885.3493 6183.1319 939.61975 7.4290406 -98.957196 29.645176 -3.6804323
0.17165783
.142797
17305.389 6060.1548 6913.5391 -3265.1473 958.79436 167.70955 15.966009
-.63457855
.654617
19688.53 5986.4853 1702.7013 -548.08811 99.756451 9.0098314 0.23100461
0.010371999
.008475
39454.629 6927.2776 1485.3507 338.61179 -269.75885 66.52999 -7.6326178
.34109395
.565099
-13012.66 5383.1393 5237.9606 -783.047 -42.3283 35.372988 -4.843263 0.2235078
.708419
-28282.284 5982.3212 1370.6198 -281.80495 1.6967626 10.307196 -1.7365992
0.091892333
.176023
-96249.681 5689.7647 6948.0348 -3187.2165 907.51942 -154.34752 14.331037
-0.5571496
.597815
140059.73 6603.0981 129.43656 573.42149 -267.64451 59.411375 6.3600005
.26818599
.878124
88144.439 5131.3385 4513.1517 -1238.9165 194.63229 -15.017215 .232008
.023195333
.128062
32192.071 4491.728 6248.7738 -1167.0905 -11.704995 43.652820 -6.8574345
.34726656
.727304
79175.58 6873.6705 -285.17319 683.60135 -277.72871 57.192553 -5.9895783
.25327447
.725638
111509.41 5015.7889 -92.295094 83.547477 -38.540677 8.9155623 -0.91401847
0.034707465
.168916
58008.607 5353.7423 -412.44632 246.19247 -86.140481 17.415382 -1.8288189
0.077299666
Где NS - значение n∑ в первом приближении, P0 - давление в камере сгорания,
E -
точность расчета, R0 - газовая
постоянная, СК - коэффициент, обеспечивающий сходимость решения.
Для дальнейшего заполнения файла необходимо приблизительно определить
список веществ, образующихся в результате сгорания данного топливо. Для этого
нужно определить коэффициент избытка окислительных элементов:
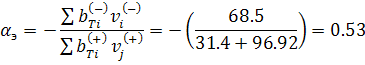
Где

 ,
, 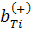
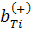 -
коэффициенты в условной формуле топлива при окислительных и горючих элементах,
-
коэффициенты в условной формуле топлива при окислительных и горючих элементах, 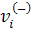
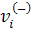 ,
, 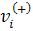
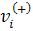 -
наивысшая валентность окислительных и горючих элементов. В данном топливе -
избыток горючих элементов.
-
наивысшая валентность окислительных и горючих элементов. В данном топливе -
избыток горючих элементов.
Вещества
списка нужно разбить на 3 группы: МГВ (молекулярные газообразные вещества), АГВ
(атомарные газообразные вещества) и КВ (конденсированные вещества)
В
данном случае список такой:
МГВ: H2, H2O, OH, N2,
N2O, NO, NH2, NH3, CO, CO2, CH, CH2,
CH3, NH
КВ
-
АГВ:
N, O, H, C
C помощью списка
веществ составляются матрицы W1 и С.
Как
получить W1 - в соответствии с выбранным порядком МГВ
расписывается количество в каждом соединении атомов АГВ (тоже по порядку).
Массив
С - это коэффициенты в условной формуле топлива при элементах (по порядку).
Массивы
P и P1 - для записи парциальных давлений МГВ и АГВ
соответственно. Используя этот файл, программа может подсчитать энтальпию для
данного топлива при любой температуре.
.2.2
Оценка калорийности топлива
Определяем
переменные
logical
tff ! объявляем логическую переменную tff
для проверки 1-го эксперимента
real sum !
объявляем переменную sum, которая накапливает калорийность
real Ent !
удельная энтальпия топлива
tff = .true.
! присваиваем переменной tff значение ‘истина’= 0 ! присваиваем переменной sum
значение 0
………………………………………………………(*,*) 'Entalpy→' 1(*,*) Ent
2=750 3
JPR=0
………………………………………………………= Ht0 5
………………………………………………………
Т = Т + 50 6(abs(HT0 - Ent) < abs(Ent)*.01)
goto 96 7(.not.tff) then 8= (HT0-tmph)/50 9(*,*)" difference -> "
,Cp 10= sum + Сp * 50 11(1,*)"
difference -> " ,Cp 12 13
14=.false. 15(1,*) '---------------------------------------------------'
go to 1987
Алгоритм:
1. Нахождение истинной температуры.
В строке 7 записано условие, позволяющее автоматизировать подбор истинной
температуры. Производится оценка модуля разности значение энтальпии продуктов
сгорания HT0 и Ent (энтальпии топлива), введенной с клавиатуры (строка
1). Если модуль разности значений не превышает точности 1% от удельной
энтальпии топлива, то текущая температура считается истинной. Начальное
значение температуры с клавиатуры не вводится, оно задается в строке
3(минимальное значение, при котором имеет смысл проводить расчет). Затем
перебираются все температуры до определения истинной.
. Оценка калорийности топлива.
В
строке 5 вводится переменная tmph для запоминания текущего значения энтальпии.
Переменная tff вводится для того, чтобы пропустить 1 реализацию,т.к.
в формуле удельной емкости 
 разница
будет равно нулю (результат непредсказуем), а также для того, чтобы этот
результат не учитывался при подсчете суммы (калорийности в строке 11).При
определении значение переменной tff ‘истина’, т.е. в соответствии со строкой 8 первая
реализация пропускается, затем значением переменной становится ‘ложь’ и
начинается подсчет. Переменной sum присваиваем значение 0 опять же с целью избежания
непредсказуемого результата. Значения энтальпий, теплоемкостей и калорийности
выводятся на экран и записываются в файл.
разница
будет равно нулю (результат непредсказуем), а также для того, чтобы этот
результат не учитывался при подсчете суммы (калорийности в строке 11).При
определении значение переменной tff ‘истина’, т.е. в соответствии со строкой 8 первая
реализация пропускается, затем значением переменной становится ‘ложь’ и
начинается подсчет. Переменной sum присваиваем значение 0 опять же с целью избежания
непредсказуемого результата. Значения энтальпий, теплоемкостей и калорийности
выводятся на экран и записываются в файл.
.2.3 Листинг программы
INTEGER P3,Y,F1
DIMENSION
P(40),R(5),P1(10),H(60,9),W1(40,10),(5,10),B(40,10),A(10,40),C1(10,10),E(40),EE(10),(10),KR(40),EE1(10),(40),C(10),ST(60),HT(60),KR1(5),FAQ(40),FAQ1(5)NS,KR,KR1,
Ent, tmph
logical tff ! для проверки 1 опыта
real sum ! калорийность
топлива
CHARACTER FLDK*4FLDN*4(*,*)'Name of input file (4
letters)'(*,501)FLDN
FORMAT(A4)(2,FILE=FLDN//'.DAT',STATUS='OLD', err=999)(2,1000)
FORMAT(1X)(2,*)NS,P0,ET,R0,CK(2,1000)(2,*)N,M,K(*,*)'M=',M(2,1000)(M.EQ.0)
GOTO 100(2,*)(R(I),I=1,M)
READ(2,1000)(M.EQ.0) GO TO 101(2,*)((W2(I,J),J=1,K),I=1,M)
READ(2,1000)(2,*)(P(I),I=1,N)(2,1000)(2,*)(P1(I),I=1,K)(2,1000)(2,*)(C(I),I=1,K)(2,1000)(2,*)((W1(I,J),J=1,K),I=1,N)(2,1000)(2,*)((H(I,J),J=1,9),I=1,N+M+K)(UNIT=2)
tff =
.true. !присваиваем переменной значение
'истина'
sum = 0(*,*) 'name of output file is "outf.dat"' !выходной файл(перезаписывается)=
'outf.dat'(1,file="con")(1,file=fldk//'.dat')
! write(*,*)'Temperature' !вводим с клавиатуры температуру топлива
! read(*,*) T(*,*)'Entalpy->' !вводим с клавиатуры удельную энтальпию
топлива(*,*) Ent=750 !начинаем с 750
! WRITE(*,*)'Name of output file (4 letters)'
! READ(*,501)FLDK
! OPEN(1,FILE=FLDK//'.DAT',STATUS='NEW')
1987 JPR=0 ! цикл по температуре
P3=1
DO 2 J=M+1,M+K3 I=1,N
B(I,J)=W1(I,P3)*(-1)
P3=P3+1
! WRITE(1,*)'B MAIN'
! WRITE(1,*)((B(I,J),J=1,K+M+1),I=1,N)
! write(*,*)' B=1'
DO4 I=1,N=M+15 J=1,K(Y,I)=W1(I,J)*P(I)
Y=Y+1
A(Y,I)=P(I)
! WRITE(1,*)'A M'
! WRITE(1,*)((A(Y,I),I=1,N),Y=1,M+K+1)
! write(*,*)' B=2'6 J=1,K=0.I=1,N=W1(I,J)*P(I)
S1=S1+U1=0.I=1,M=W2(I,J)*R(I)
S2=S2+U2
D(J)=S1+S2+P1(J)
! WRITE(1,*)'D M'
! WRITE(1,*)(D(J),J=1,K)
! write(*,*)' B=3'(M.EQ.0) GOTO 1319 I=1,K=M+I10 J=1,M
C1(Y,J)=W2(J,I)*R(J)
CONTINUE11 I=1,M12 J=1,K=M+J(I,Y)=W2(I,J)*(-1)
CONTINUE
CONTINUE
P3=1=K+M+1111 J=1,K=J+M(J1,J1)=P1(P3)(F1,J1)=P1(P3)
P3=P3+1=1141 I=1,K=I+M(I1,F1)=D(P3)
P3=P3+1
! WRITE(1,*)'C1 M'
! WRITE(1,*)((C1(I,J),j=1,M+K+1),I=1,M+K+1)
! write(*,*)' B=4'(JPR.EQ.1) GO TO 600=1=T*1E-314
I=1,M+N+K(I)=(H(I,2)+H(I,3)*T+H(I,4)*T**2+H(I,5)*T**3+H(I,6)*T**4+
* H(I,7)*T**5+H(I,8)*T**6+H(I,9)*T**7)*4.19
ST(I)=(H(I,1)+H(I,3)*ALOG(T)*1E-3+H(I,4)*T*2E-3+
* H(I,5)*T**2*1.5E-3+H(I,6)*T**3*1.3E-3+H(I,7)*T**4*1.25E-3+
* H(I,8)*T**5*1.2E-3+H(I,9)*T**6*1.17E-3)*4.19
! WRITE(1,*)(HT(I),I=1,M+N+K)
! WRITE(1,*)(ST(I),I=1,M+N+K)=T*1E315 I=1,N=M+N+1=0=HT(I)-ST(I)*T16
J=1,K=(HT(P3)-ST(P3)*T)*W1(I,J)=S60+SP
P3=P3+1=S60-SP1(I)=-G/(R0*T)
KR(I)=EXP(FAQ(I))(M.EQ.0) GOTO 171=1=M+N+1=0.17
I=N+1,N+M=HT(I)-ST(I)*T=I-N18 J=1,K=(HT(P3)-ST(P3)*T)*W2(IH,J)=S90+SP2
P3=P3+1=S90-SP1(Y)=-G/(R0*T)(Y)=EXP(FAQ1(Y))
Y=Y+1
! 171write(*,*)' B=5'
CONTINUE19 I=1,N=0.20 J=1,K(P1(J).LT.1E-38) GO TO 800TO 810
write(*,*)'Computation can not be completed at this
temperature'
Q5=W1(I,J)*ALOG(P1(J))
S5=S5+Q5
E(I)=(FAQ(I)+ALOG(P(I))-S5)*(-1)
! WRITE(1,*)'E M'
! WRITE(1,*)(E(I),I=1,N)
! write(*,*)' B=6'(M.EQ.0) GOTO 21321
I=1,M=0.J=1,K=W2(I,J)*ALOG(P1(J))
S6=S6+Q6
EE(I)=(FAQ1(I)-S6)*(-1)
P3=123
I=M+1,M+K(I)=(-1)*D(P3)*(ALOG(D(P3))+ALOG(NS)-ALOG(P0)-ALOG(C(P3)))
P3=P3+1=M+K+1=0.24 P3=1,N=P(P3)
S7=S7+Q7=0.25 P3=1,K=P1(P3)
S8=S8+Q8=S7+S8(I)=PS*(-1)*(ALOG(PS)-ALOG(P0))
! WRITE(1,*)'EE M'
! WRITE(1,*)(EE(I),I=1,M+K+1)
! write(*,*)' B=7'=M+K+1UMD(A,B,C1,E,EE,EE1,X,K1,N)=0.44
I=1,N
S20=S20+ABS(E(I))=0(M.EQ.0) GOTO 4546 I=1,M
S5=S5+ABS(EE(I))
S30=047 I=M+1,M+K=I-M
S30=S30+ABS(EE(I))/ABS(D(J))=0.48 P3=1,N+K(P3.LE.N) GOTO
49=P3-N=P1(I)48
S6=P(P3)
PS=PS+S6=ABS(EE(K1))/PS=S20+S5+S30+S40
! write(*,*)' FS=',FS,' PS=',PS(FS.GT.ET) GOTO 53
! WRITE(1,*)'T= ',T,' K'
! WRITE(1,*)'Partial pressures of molecular gaseous subst.,
atm'
! WRITE(1,*)(P(I),I=1,N)(M.EQ.0) GOTO 510
! WRITE(1,*)'Conditional partial press. of condensed subst.,
atm'
! WRITE(1,*)(R(I),I=1,M)
!510 WRITE(1,*)'Partial pressures of atomic gaseous subst.,
atm '
! WRITE(1,*)(P1(I),I=1,K)
continue
! WRITE(1,*)'NS= ',NS, ' mole/kg'=0.=0.601 I=1,N=Z10+P(I)*ST(I)-8.314*P(I)*ALOG(P(I))
S10=S10+P(I)*HT(I)=0.=0.(M.EQ.0) GO TO 602603
I=1,M=I+N=Z20+R(I)*ST(J)
S20=S20+R(I)*HT(J)
CONTINUE=0=0604
I=1,K=N+M+I=Z30+P1(I)*ST(J)-8.314*P1(I)*ALOG(P1(I))
604 S30=S30+P1(I)*HT(J)= Ht0 !
запоминаем текущее удельной энтальпии продуктов сгорания
HT0=(NS/P0)*(S10+S20+S30)=(NS/P0)*(Z10+Z20+Z30)(1,*)'Enthalpy
of combustion products ',HT0,' J/kg'(*,*)'Enthalpy of combustion products
',HT0,'J/kg'(1,"(a, f6.0)") " T= ", t
t = t + 50 ! изменение температуры
! WRITE(1,*)'Entropy of combustion products ',ST0,' J/kg/K'
if(.not.tff) then ! пропускаем 1 эксперимент
Cp = (ht0-tmph)/50 !теплоемкость(*,*)" difference -> " ,Cp= sum + cp * 50 !калорийность топлива(1,*)" difference -> " ,Cp
endif
tff=.false. ! не первый эксперимент(abs(HT0
- Ent) < abs(ent)*.01) goto 96 ! нахождение истинной температуры
Write(1,*) '---------------------------------------------------'(1,*)to
1987 ! заново96
SIG=(N+M+K+1)*CK/FS
! write(*,*)'SIG=',SIG
! write(*,*)' -€Љ‹'(SIG.GT.1) SIG=1.054 I=1,N
P(I)=P(I)*EXP(X(I)*SIG)(M.EQ.0) GOTO 55155 I=1,M
R(I)=R(I)*EXP(EE1(I)*SIG)
P3=156 I=M+1,M+K(P3)=P1(P3)*EXP(EE1(I)*SIG)
P3=P3+1=M+K+1=NS*EXP(EE1(I)*SIG)
GOTO 70
CONTINUE(*,*) 'E = ', sum !выводим значение калорийности топлива на экран
Write(1,*) '---------------------------------------------------'
write(1,*)(1,*)
'E = ', sum !выводим значение калорийности топлива в выходной файл
CLOSE(UNIT=1)
write(*,*) "file ", trim(fldn//'.dat'), ' is not
found'UMD(A,B,C1,E,EE,EE1,X,K1,N)A(10,40),B(40,10),C1(10,10)
* EE(10),X(40),E(40),EE1(10)A1(10,10),C2(10,10)
* B1(40),A2(10),IP(10),WOR(10)
! WRITE(1,*)'N=',N,'K1=',K1
! WRITE(1,*)'A'
! WRITE(1,*)((A(I,J),J=1,N),I=1,K1)
! WRITE(1,*)'B'
! WRITE(1,*)((B(I,J),J=1,K1),I=1,N)GMPRD(A,B,A1,10,40,10)
! WRITE(1,*)'A1'
! WRITE(1,*)((A1(I,J),J=1,K1),I=1,K1)1 J=1,K11 I=1,K1
C2(I,J)=C1(I,J)-A1(I,J)
! WRITE(1,*)'C2'
! WRITE(1,*)((C2(I,J),I=1,K1),J=1,K1)GMPRD(A,E,A2,10,40,1)
! WRITE(1,*)'A2'
! WRITE(1,*)(A2(I),I=1,K1)2 J=1,K1
EE1(J)=EE(J)-A2(J)
! WRITE(1,*)'EE1'
! WRITE(1,*)(EE1(J),J=1,K1)DECOMP(10,K1,C2,COND,IP,WOR)
! WRITE(1,*)'COND=',COND=COND+1(CONDP.EQ.COND)
STOPSOLVE(10,K1,C2,EE1,IP)
! WRITE(1,*)(EE1(I),I=1,K1)GMPRD(B,EE1,B1,40,10,1)
! WRITE(1,*)(B1(I),I=1,N)3 J=1,N
X(J)=E(J)-B1(J)
! WRITE(1,*)(X(J),J=1,N)
.3 Результаты исследования калорийности
of combustion products -4822002. J/kg= 750.
--------------------------------------------------of
combustion products -4716822. J/kg= 800.-> 2103.600
--------------------------------------------------of
combustion products -4616116. J/kg= 850.-> 2014.110
--------------------------------------------------of
combustion products -4518102. J/kg= 900.-> 1960.290
--------------------------------------------------of
combustion products -4421898. J/kg= 950.-> 1924.070
--------------------------------------------------of
combustion products -4327050. J/kg= 1000.-> 1896.960
--------------------------------------------------of
combustion products -4233276. J/kg= 1050.-> 1875.470
--------------------------------------------------of
combustion products -4140378. J/kg= 1100.-> 1857.970
--------------------------------------------------of
combustion products -4048203. J/kg= 1150.-> 1843.500
--------------------------------------------------of
combustion products -3956610. J/kg= 1200.-> 1831.855
--------------------------------------------------of
combustion products -3865486. J/kg= 1250.-> 1822.490
--------------------------------------------------of
combustion products -3774723. J/kg= 1300.-> 1815.255
--------------------------------------------------of
combustion products -3684232. J/kg= 1350.-> 1809.825
--------------------------------------------------of
combustion products -3593929. J/kg= 1400.-> 1806.060
--------------------------------------------------of
combustion products -3503751. J/kg= 1450.-> 1803.560
--------------------------------------------------of
combustion products -3413635. J/kg= 1500.-> 1802.310
--------------------------------------------------of
combustion products -3323532. J/kg= 1550.-> 1802.075
--------------------------------------------------of
combustion products -3233398. J/kg= 1600.-> 1802.670
--------------------------------------------------of
combustion products -3143198. J/kg= 1650.-> 1804.010
--------------------------------------------------of
combustion products -3052895. J/kg= 1700.-> 1806.055
--------------------------------------------------of
combustion products -2962464. J/kg= 1750.-> 1808.620
--------------------------------------------------of
combustion products -2871876. J/kg= 1800.-> 1811.745
--------------------------------------------------of
combustion products -2781108. J/kg= 1850.-> 1815.380
--------------------------------------------------of
combustion products -2690132. J/kg= 1900.-> 1819.510
--------------------------------------------------of
combustion products -2598920. J/kg= 1950.-> 1824.240
--------------------------------------------------of
combustion products -2507446. J/kg= 2000.-> 1829.475
--------------------------------------------------of
combustion products -2415676. J/kg
T= 2050.
-------------------------------------------------
Калорийность топлива:
E =
2.4∙106
Выводы по главе
. Даны определения теплового эффекта химической реакции и калорийности
ВЭМ. Объяснена актуальность создания методики прогнозирования калорийности ВЭМ.
Представлено описание метода, используемого при расчете калорийности. С
учетом специфики работы: обозначены основные процессы и явления, происходящие в
камере сгорания ракетного топлива, представлены основные соотношения и
допущения термодинамического метода. Произведено описание математической модели
и численного метода для определения состава продуктов сгорания.
. Представлен вывод используемого при расчете соотношения для определения
калорийности. Описан алгоритм расчета калорийности, приведен пример.
. Приведен образец и пример заполнения исходного файла расчетной
программы, листинг программы с необходимыми комментариями, а также выходной
файл, включающий значение калорийности.
Глава 4.
Численный анализ характеристик ВЭМ на базе нанокомпонентов
4.1 Описание
выбранного топлива
Объектом анализа выбрано высокоэнергетическое ракетное топливо, состоящее
из следующих компонентов (приведены химические либо условные формулы
компонентов):
. С71.809H136.404
- каучук
. C4H8O8N8 - октоген
. NH4ClO4 - перхлорат аммония
. Al - алюминий
Удельные
энтальпии компонентов топлива при начальной температуре (
 ) равны
соответственно:
) равны
соответственно:
.
С71.809H136.404 -
-3.485∙106 Дж/кг
.
C4H8O8N8 - 3.24∙105
Дж/кг
.
Al - 0
Массовые
доли компонентов выбраны так, чтобы исследуемое топливо по составу
соответствовало бы реальному:
1. С71.809H136.404 - 0.12
. C4H8O8N8 -
0.12
. NH4ClO4 - 0.56
. Al - 0.2
4.1
Определение калорийности выбранного топлива.
С помощью разработанных программных средств производится оценка
калорийности топлива выбранного состава. В процессе расчета учитывается
изменение свойств Al2O3 (оксида алюминия - единственного конденсированного
вещества в продуктах сгорания) при превышении температуры свыше 2300 вследствие
изменения его агрегатного состояния.
Оценка калорийности проводится для 3-х случаев:
1. Удельная энтальпия алюминия равна 0 (стандартный случай)
2. Удельная энтальпия алюминия равна 2∙106 Дж/кг
(вариант наноалюминия)
. Удельная энтальпия ½ перхлората аммония заменяется на 3∙106
(топливо содержит наночастицы ПХА)
Результаты расчета занесены в таблицу:
Таблица 4.1.
|
№ случая
|
Энтальпия Al
|
Энтальпия топлива (  , Дж/кг , Дж/кг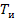 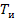 ,ККалорийность
топлива(E), Дж ,ККалорийность
топлива(E), Дж
|
|
|
|
1
|
0
|
-1.77∙106
|
3220
|
6.25∙106
|
|
2
|
2∙106
|
-1.37∙106
|
3355
|
6.64∙106
|
|
3
|
2∙106
|
0.13∙106
|
3755
|
8.14∙106
|
Анализ таблицы: для случая 2 (наноалюминий) энтальпия Al вместо 0 становится равной 2∙106
Дж/кг, следовательно, и калорийность топлива возрастает.
Резкий прирост калорийности топлива в случае 3 связан с влиянием на
процесс горения топлива наночастиц ПХА (который составляет 56% топлива).
наночастица
высокоэнергетический материал калорийность
Выводы по
главе
В текущей главе проведены исследования высокоэнергетических ракетных
топлив на базе нанодисперсных компонентов.
· Осуществлено описание состава выбранного топлива.
· С помощью программных средств произведена оценка калорийности
выбранного топлива для трех вариантов: стандартно изготовленного топлива,
топлива с нанодисперсным алюминием, топлива с нанодисперсными алюминием и ПХА.
Приведены результаты расчетов, доказывающие значительный прирост
калорийности выбранного топлива с внедрением в него компонентов в
нанодисперсном виде, и более резкий прирост - с увеличением доли таких
компонентов в топливе.
5. Анализ и
выбор оборудования для определения калорийности ВЭМ
5.1. Выбор
метода измерения калорийности
Любое оборудование, применяемое для измерения той или иной
характеристики, реализует метод измерения этой характеристики. Калорийность ВЭМ
- не является исключением, следовательно необходимо произвести обзор методов,
позволяющих определять калорийность ВЭМ.
Калориметрия.
Калориметрия
(от лат. calor - тепло и ...метрия
<#"526824.files/image209.gif"> 
Рис.5.1 Калориметрическая бомба в разобранном и собранном виде
2.
При подготовке к проведению опыта используются аналитические весы АВ310-01С
<#"526824.files/image211.gif">
Так
как 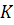
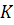 и
и 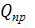
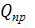 - не
являются измеряемыми в данном опыте величинами, инструментальная погрешность
определения калорийности ВЭМ определяют величины
- не
являются измеряемыми в данном опыте величинами, инструментальная погрешность
определения калорийности ВЭМ определяют величины 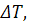
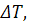
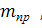
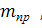
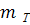
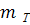
Для
определения количественной меры инструментальной погрешности используется метод
линеаризации. Тогда:
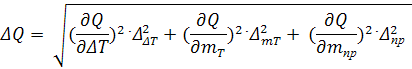
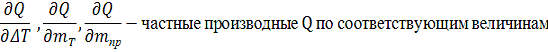
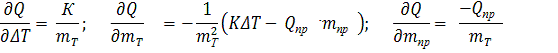
Подставим
числовые значения:

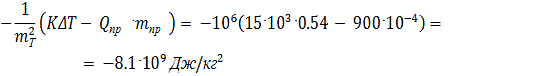
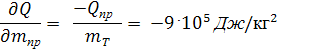
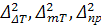
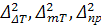 -
квадраты абсолютных погрешностей измерения величин
-
квадраты абсолютных погрешностей измерения величин
Найдем
значения этих абсолютных погрешностей:
· Относительная
погрешность измерения δ = 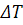
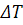

 0.1%
(техническая характеристика калориметра Та-5 «Тантал»)
0.1%
(техническая характеристика калориметра Та-5 «Тантал»)
С
помощью известного значения теплоемкости калориметра произведем оценку 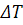
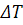 :
:
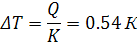
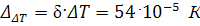
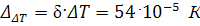
· Погрешность
измерения 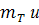
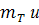
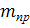
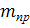 рассчитаем,
воспользовавшись данными о погрешности аналитических весов АВ310-01С
<#"526824.files/image229.gif">
рассчитаем,
воспользовавшись данными о погрешности аналитических весов АВ310-01С
<#"526824.files/image229.gif">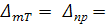 0.0001 г
0.0001 г
Подставив
численные значения в формулу, получим:
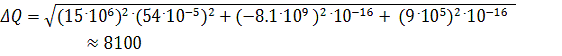
Наибольший
вклад в абсолютную ошибку вносит погрешность измерения температуры калориметром
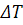
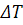 .
.
Относительная
погрешность измерения:
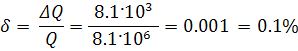
Выводы по
главе
В данной главе произведен обзор существующих методов определения
калорийности, выбран конкретный метод исследования, а также выбрано
измерительное оборудование, подходящее для выполнения поставленной задачи.
Сравнивая процесс горения образцов топлива содержащего нанокомпоненты и
несодержащего их, можно сделать заключение либо о всплеске тепловой энергии в
первом, либо об отсутствии его. С помощью данной методики возможно исследование
горения образцов топлива, анализ этих процессов и последующее утверждение либо
опровержение вышеуказанных предположений.
Технико-экономический
раздел
Экономическое обоснование выбора оборудования для
измерения калорийности.
Произведем сравнительный расчет затрат, необходимых
для проведения калориметрического опыта, состоящего в сжигании топлива с
содержанием нанодисперсных компонентов в выбранном бомбовом калориметре ТА-5
«Тантал» и в калориметре АБК-1.
. Затраты на заработную плату работников
Определяется по штатному расписанию при современной
оплате труда и по нормам выработки при сдельной оплате труда. При расчете
учитываются штатные работники, совместители, работники, принятые по контракту.
Затраты включают в себя основную и дополнительную зарплату, оплату отпусков и др.
виды зарплат, предусмотренные законодательством. Проведение исследований и
обработка результатов эксперимента заняли в общей сложности 1 рабочий день, а
рабочих дней в месяце 24.
|
ТА-5 «Тантал»
|
АБК-1
|
|
Эксперимент проводили: 1.Инженер
|
|
Инженер проводит опыт
длительностью 23 минуты, а также некоторые необходимые расчеты, что займет не
более 20 минут. Таким образом, время работы инженера составляет 43 минуты,
т.е. 0.717ч.
|
Опыт, проводимый инженером
длится 20 минут. Столько же - расчеты. То есть общее время работы инженера -
40 минут, т.е. 0.667ч
|
|
ССредняя заработная плата
инженера в Санкт-петербурге на 2009 год составляет 30000р. Исходя из этих
данных: Затр. на зп инж./ч = 30000/192ч = 156.25р/ч,тогда
|
|
Затр. на зп. инж. =
156.25р/ч ∙ 0.717ч = = 112р
|
Затр. на зп инж. =156.25р/ч
∙ 0.667ч =104.22р
|
|
2.Техник Техник проводит
работы, связанные с подготовкой к опыту (взвешивание и прессование образца,
взвешивание нити с запальной проволокой, наполнение калориметрической бомбы
кислородом, помещение бомбы в калориметрический сосуд) и сбросом давления из
бомбы после окончания измерения. В общей сложности длительность выполнения
всех работ, связанных с обслуживанием обоих приборов(следовательно и время
работы техника) примерно одинакова и составляет 1,5 часа. Средняя заработная
плата техника в Санкт-петербурге на 2009 год составляет 15000р. Таким образом:
|
|
Затр. на зп. техн./час =
15000р/192ч = =78.12р, тогда Затр. на зп. техн. = 78.12р /ч ∙ 1.5 ч =
117.3р
|
|
В итоге затраты на
заработную плату работников в ходе данного эксперимента составляют:
|
|
Сэл =112р +
117.3р =229.3р
|
Сэл =104.22р+
117.3р=221.5р
|
|
|
|
|
2. Электроэнергия на
технологические цели
Стоимость электроэнергии для коммунальных нужд
(освещение и т. п.) определяется по одноставочному тарифу за потребленную
энергию. Для производственных нужд, где используются энергоёмкие основные фонды
мощностью 750кВт и более, действует двуставочный тариф.
|
Энергозатраты на
эксперимент, включают в себя: Электронергию, необходимую для работы
собственно калориметра
|
|
Потребляемая мощность калориметра
ТА-5 «Тантал» равна 200Вт. За 23 минуты эксперимента расход составит: 0.2кВт∙0.383ч=0.0767кВтч
|
Потребляемая мощность
калориметра АБК-1 равна 100Вт. За 20 минуты эксперимента расход составит:
0.1кВт∙0.333ч=0.0333кВтч
|
|
Электроэнергию, необходимую
для работы компьютера Компьютеры в обоих случаях одинаковые, потребляемая
мощность 200Вт Время работы компьютера включает в себя время проведения
эксперимента а также расчеты после него и распечатку результатов. Т.е. и в
том и в другом случае равно времени работы инженера, т.е. 43 и 40 минут.
Расход равен:
|
|
0.2кВт∙0.717ч=0.143кВтч
|
0.2кВт∙0.667ч=0.133кВтч
|
|
3.Электроэнергию,
необходимую для работы принтера Принтеры в обоих случаях одинаковые,
потребляемая мощность в режиме печати 1200Вт, время печати 10 минут, т.е.
0.167ч. Тогда расход cоставит:
|
|
1.2кВт∙0.167ч=0.2кВтч
|
|
4.Электроэнергию,
необходимую для работы аналитических весов Весы в обоих случаях одинаковые,
потребляемая мощность 10Вт, время работы 5минут, т.е. 0.0833ч. Тогда расход cоставит:
|
|
0.01кВт∙0.0833ч=0.000833кВтч
|
|
5.Электроэнергию,
необходимую для освещения помещения, в котором проводится эксперимент. Для
обоих случаев помещения примерно одинаковые, т.е. для достаточно двух ламп
накаливания мощностью по 100Вт. Для расчета возьмем полное время, необходимое
для эксперимента, его подготовки, расчетов, т.е. 1.5ч.
|
|
0.1кВт∙3∙1.5ч=0.45кВтч
|
|
В итоге затраты на
потребленную электроэнергию в ходе данного эксперимента есть сумма
энергозатрат по всем 5 пунктам, домноженная на стоимость 1 кВтч в
Санк-петербурге на 2009 год, а именно на 1.85р.
|
|
Сэл= (0.0767 +
0.143 + 0.2 + 0.000833 + +0.45)∙1.85 =1.61р
|
Сэл=(0.0333 +
0.133 + 0.2 + +0.000833+0.45)∙1.85=1.51р
|
|
|
|
. Затраты на амортизацию оборудования
|
Средний процент годовой
нормы амортизации на используемое оборудование можно принять равным 12. В
ходе эксперимента использовалось следующее оборудование:
|
|
Калориметр Та-5 «Тантал» -
985000р СА1 = 985000р ∙ 0.12 ∙ 0.383/1800 = 25.15р
|
Калориметр АБК-1 - 1800000р
СА = 1800000р ∙ 0.12 ∙ 0.333/1800 = 39.96р
|
|
Аналитические весы(точность
0.0001) - 10000 (одинаковы в обоих случаях) СА2 = 10000р ∙
0.12 ∙ 0.0833/1800 = 0.056р
|
|
Таким образом затраты на
амортизацию оборудования составляют:
|
|
СА=25.15р + 0.056р +0.0667р+20= 25.27р
|
СА=39.96р + 0.056р +0.0667р+20= 40.08р
|
4. Затраты на сырье
|
В ходе данного эксперимента
использовались следующие материалы:
|
|
нанодисперсное топливо 1г -
100р
|
|
Итого затраты на сырье и в
том и а другом случае составили 100р
|
. Затраты по использованию производственных зданий
|
Площадь, необходимая для
проведения эксперимента включает площадь занимаемую:
|
|
Калориметром - 0.117 м2
|
Калориметром - 0.142 м2
|
|
Принтером - 0.045 м2 Аналитическими
весами - 0.04 м2
|
Итого общие затраты на эксперимент составили:
Выводы по главе: В главе произведен сравнительный
расчет затрат на проведение калориметрического опыта для выбранного и
альтернативного прибора. В итоге ясно, что проведение опыта с помощью
калориметра ТА-5 «Тантал» (выбранного) экономически более выгодно.
Раздел охраны
труда
Обеспечение требований охраны труда и экологии при проведении
калориметрического опыта.
В данном разделе будут рассмотрены вопросы, связанные с обеспечением
требований охраны труда и окружающей среды при работе на ЭВМ (управление опытом
и обработка результатов осуществляется на ЭВМ, разработка программного
обеспечения для прогнозирования калорийности ВЭМ также производится на ЭВМ); а
также - вопросы, связанные с вентиляцией и пожарной безопасностью помещения, в
котором проводится опыт.
1.
Обеспечение требований охраны труда и окружающей среды при работе на ЭВМ
Работа оператора ЭВМ относится к категории работ, связанных с опасными и
вредными условиями труда. В процессе труда на оператора ЭВМ оказывают действие
следующие опасные и вредные производственные факторы: физические (повышенные
уровни электромагнитного, рентгеновского, ультрафиолетового, инфракрасного
излучений; повышенный уровень шума и.т.д.); химические (повышенное содержание в
воздухе рабочей зоны двуокиси углерода, озона, аммиака, фенола, формальдегида и
полихлорированных бифенилов); психофизиологические (напряжение зрения,
внимания; интеллектуальные и эмоциональные нагрузки и т.д.); биологические
(повышенное содержание в воздухе рабочей зоны микроорганизмов).
Требования к
помещениям с ЭВМ
Помещения с ЭВМ должны удовлетворять 2 разряду зрительной работы,
подразряду В. При этом, в силу специфики работы на ЭВМ, освещение должно быть
искусственным; температура воздуха 22-25 °С, относительная влажность 40-60%,
скорость движения воздуха 0,1-0,2 м/с; содержание вредных химических веществ не
должно превышать ПДК; уровень шума - не более 50 дБА; уровень вибрации -
корректированные значения по виброускорению - не более 30 дБ, по виброскорости
- не более 72 дБ. внутренняя отделка интерьера с использованием диффузно-отражающих
материалов с коэффициентом отражения для потолка - 0,7-0,8, для стен - 0,5-0,6
и для пола - 0,3-0,5; поверхность пола должна быть ровной, нескользкой, удобной
для влажной уборки, обладать антистатическими свойствами.
В таблице 1 приведены нормы микроклимата в холодный и теплый период года
для работ этой категории согласно СанПиН 2.2.2./2.4.1340-03.
Таблица 1. Нормы микроклимата
|
Параметр
|
Оптимальные значения
|
Допустимые значения
|
|
Периоды года
|
Периоды года
|
|
Холодный
|
Теплый
|
Холодный
|
Теплый
|
|
Температура, 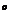 C C
|
22 - 24
|
23 - 25
|
21 - 25
|
22 - 28
|
|
Относительная влажность
воздуха, %
|
40 - 60
|
40 - 60
|
не более 75
|
не более 75
|
|
Скорость движения воздуха,
м/с
|
не более 0.1
|
не более 0.1
|
не более 0.1
|
не более 0.1
|
Освещенность на поверхности стола в зоне размещения рабочего документа
должна быть 300-500 лк. Освещение не должно создавать бликов на поверхности
экрана. Освещенность поверхности экрана не должна быть более 300 лк.
Рабочие столы следует размещать таким образом, чтобы видеодисплейные
терминалы были ориентированы боковой стороной к световым проемам, чтобы
естественный свет падал преимущественно слева.
Следует ограничивать прямую блесткость от источников освещения, при этом
яркость светящихся поверхностей (окна, светильники и др.), находящихся в поле
зрения, должна быть не более 200 кд/м².
Светильники местного освещения должны иметь непросвечивающий отражатель с
защитным углом не менее 40°. В качестве источников света при искусственном
освещении следует применять преимущественно люминесцентные лампы типа ЛБ и
компактные люминесцентные лампы (КЛЛ). В светильниках местного освещения
допускается применение ламп накаливания, в том числе галогенных.
Общее освещение при использовании люминесцентных светильников следует
выполнять в виде сплошных или прерывистых линий светильников, расположенных
сбоку от рабочих мест, параллельно линии зрения пользователя при рядном
расположении видеодисплейных терминалов. При периметральном расположении
компьютеров линии светильников должны располагаться локализованно над рабочим
столом ближе к его переднему краю, обращенному к оператору.
В помещениях ежедневно должна проводиться влажная уборка систематическое
проветривание после каждого часа работы на ЭВМ.
Высота зала над технологическим полом до подвесного потолка должна быть 3
- 3,5 м. Расстояние подвесным и основным потолками при этом должно быть 0,5 -
0,8 м. Высоту подпольного пространства принимают равной 0,2 - 0,6 м.
Требования к
ЭВМ
ЭВМ должен обеспечивать фронтальное наблюдение экрана с поворотом корпуса
по горизонтали и вертикали в пределах 60 град, и фиксацией в заданном
положении. Яркость знака должна быть от 35 до 120 кд/м², внешняя освещенность экрана от 100
до 250 лк, угловой размер знака от 16 до 60 угл. мин. Площадь на 1 рабочее
место с ЭВМ должна быть не менее 6 м² , объем - не менее 20 м³, расстояние между экранами соседних
мониторов - не менее 2 м, боковыми поверхностями - не менее 1,2 м.
Таблица 2. Визуальные параметры ВДТ, контролируемые на рабочих местах
|
Параметры
|
Допустимые значения
|
|
Яркость белого поля
|
Не менее 35 кд/м²
|
|
Неравномерность яркости
рабочего поля
|
Не более ±20%
|
|
Контрастность (для
монохромного режима)
|
Не менее 3:1
|
|
Временная нестабильность
изображения (мелькания)
|
Не должна фиксироваться
|
|
Пространственная
нестабильность изображения (дрожание)
|
Не более 2·10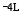 , где L - проектное расстояние наблюдения, мм , где L - проектное расстояние наблюдения, мм
|
Рассмотрим специфические вредные факторы, действующие на оператора при
работе с компьютером.
Особенности функционирования монитора приводят к возникновению целого
спектра полей различной физической природы, обладающих различными
характеристиками: электромагнитного поля отклоняющей системы электронно-лучевой
трубки (ЭЛТ), высокочастотного электромагнитного поля строчного трансформатора,
электромагнитного поля трансформаторов блока питания монитора,
электростатического поля, вызванного наличием высоковольтных цепей постоянного
тока в разгонной системе ЭЛТ.
Нужно отметить, что поля и излучение, создаваемые видеомонитором,
являются биологически активными и отрицательно воздействуют на здоровье
человека. Частотный диапазон переменного электрического и магнитного полей
расположен в пределах 5 Гц. - 400 кГц.
Кроме перечисленных полей, монитор является источником жесткого
рентгеновского излучения, вызванного свечением фосфорсодержащих веществ,
входящих в состав люминофора ЭЛТ, и источником ультразвуковой частоты строчного
трансформатора.
Значительное воздействие на глаза оператора, работающего с компьютером,
оказывает мерцание, вызванное сменой кадров на экране монитора. Для дисплеев на
ЭЛТ частота обновления изображения должна быть не менее 75 Гц при всех режимах
разрешения экрана, гарантируемых нормативной документацией на конкретный тип
дисплея, и не менее 60 Гц для дисплеев на плоских дискретных экранах (жидкокристаллических,
плазменных и т.п.).
Таблица 3. Временные допустимые уровни ЭМП, создаваемых ПЭВМ на рабочих
местах
|
Наименование параметров
|
ВДУ
|
|
Напряженность
|
в диапазоне частот 5 Гц-2
кГц
|
25 В/м
|
|
электрического поля
|
в диапазоне частот 2
кГц-400 кГц
|
2,5 В/м
|
|
Плотность магнитного
|
в диапазоне частот 5 Гц-2
кГц
|
250 нТл
|
|
потока
|
в диапазоне частот 2
кГц-400 кГц
|
25 нТл
|
|
Напряженность
электростатического поля
|
15 кВ/м
|
Для борьбы с электромагнитными и электростатическими полями мониторов в
их конструкцию вводят специальные экраны, поглощающие или отражающие до 95%
всех полей. Для современных мониторов негласным промышленным стандартом
является перенаправление основного потока вредного электромагнитного излучения
не в сторону оператора, а назад, за пределы рабочей зоны. Этот факт следует
учитывать при организации рабочих мест для групп пользователей - необходимо
размещать рабочие места в помещении таким образом, чтобы свести к минимуму
вероятность подвергнуть электромагнитному излучению оператора соседнего рабочего
места.
Борьба с ультразвуком сводится к экранированию строчного трансформатора
монитора специальным пластиком, поглощающим ультразвуковую волну. Стандарт TCO’92 предусматривает полное отсутствие
ультразвукового излучения в процессе работы монитора.
В случае источников бесперебойного питания (ИБП) двумя основными
факторами являются электромагнитное излучение и опасность поражения
электрическим током при неправильной эксплуатации. Если борьба с первым из этих
факторов сводится к простому экранированию корпусов ИБП и сосредоточению их в
одном месте, желательно удаленном или экранированном дополнительными экранами,
то для борьбы со вторым фактором требуется проведение периодических
инструктажей по технике безопасности и недопущение обслуживания системы питания
неподготовленными лицами. Наиболее действенным способом борьбы с двумя этими
факторами (и наиболее дорогим) является применение специальных шкафов-стоек для
организации системы бесперебойного питания, в состав которой входят обычно один
или несколько ИБП, специальные фильтры, коммутаторы и автоматы отключения
потребителей. Такие шкафы оборудованы специальными экранирующими панелями и
имеют средства для предотвращения несанкционированного доступа.
Потенциальным источником поражения сетчатки глаза являются
высокоскоростные волоконно-оптические системы передачи данных, имеющие в своем
составе лазеры с высокой интенсивностью излучения. Опасность поражения
возникает, как правило, в случае выхода из строя сетевого оборудования или
обрыва (излома) волоконно-оптического кабеля.
Электрические установки, к которым относится практически все оборудование
ЭВМ, представляют для человека большую потенциальную опасность, так как в
процессе эксплуатации или проведении профилактических работ человек может
коснуться частей, находящихся под напряжением. Специфическая опасность
электроустановок: токоведущие проводники, корпуса стоек ЭВМ и прочего
оборудования, оказавшегося под напряжением в результате повреждения (пробоя)
изоляции, не подают каких-либо сигналов, которые предупреждают человека об
опасности. Реакция человека на электрический ток возникает лишь при протекании
последнего через тело человека.
В вычислительных центрах и на рабочих местах пользователей ЭВМ (в
дальнейшем сокращенно ВЦ): разрядные токи статического электричества чаще всего
возникают при прикосновении к любому из элементов ЭВМ.
Такие разряды опасности для человека не представляют, но кроме неприятных
ощущений они могут привести к выходу из строя ЭВМ. Для снижения величины
возникающих зарядов статического электричества в ВЦ покрытие технологических
полов следует выполнять из однослойного поливинилхлоридного антистатического
линолеума. Другим методом защиты является нейтрализация заряда статического
электричества ионизированным газом. В промышленности широко применяются
радиоактивные нетрализаторы. К общим мерам защиты от статического электричества
в ВЦ можно отнести общие и местное увлажнение воздуха.
В производственных помещениях при выполнении основных или вспомогательных
работ с использованием ЭВМ уровни шума на рабочих местах не должны превышать
предельно допустимых значений, установленных для данных видов работ в
соответствии с действующими санитарно-эпидемиологическими нормативами.
При выполнении работ с использованием ЭВМ в производственных помещениях
уровень вибрации не должен превышать допустимых значений вибрации для рабочих
мест (категория 3, тип "в") в соответствии с действующими
санитарно-эпидемиологическими нормативами.
Согласно СанПиН 2.2.2./2.4.1340-03, на рабочих местах при широкополосном
шуме устанавливаются допустимые уровни звукового давления. Допустимые уровни
звукового давления для программистов ЭВМ приведены в таблице 4.
Таблица 4. Допустимые уровни звукового давления для программистов ЭВМ
|
Среднегеометрические
частоты октавных полос, Гц
|
Уровни звука и
эквивалентные уровни шума, дБА
|
|
31.5
|
63
|
125
|
250
|
500
|
1000
|
2000
|
4000
|
8000
|
|
|
Уровни звукового давления,
дБ
|
|
|
86
|
71
|
61
|
54
|
49
|
45
|
42
|
40
|
39
|
50
|
Шумящее оборудование (печатающие устройства, серверы и т.п.), уровни шума
которого превышают нормативные, должно размещаться вне помещений с ПЭВМ.
Помещения, где размещаются рабочие места с ЭВМ, должны быть оборудованы
защитным заземлением (занулением) в соответствии с техническими требованиями по
эксплуатации.
. Вентиляция
Вентиляция - это комплекс устройств для обеспечения нормальных
метеорологических условий и удаления вредных веществ из производственных
помещений.
В производственных помещениях система отопления, вентиляции и
кондиционирования воздуха обеспечивает определенные условия:
· температура
воздуха: 17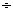 220С;
220С;
· относительная
влажность: 60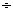 40%;
40%;
· скорость
движения воздуха 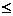 0,2 м/с.
0,2 м/с.
Вентиляция может быть естественной (аэрация) и механической в зависимости
от способа перемещения воздуха. В зависимости от объема вентилируемого
помещения различают обще обменную и местную вентиляцию. Общеобменная вентиляция
обеспечивает удаление воздуха из всего объема помещения. Местная вентиляция
используется для удаления выделяющихся вредных веществ от источников. Она может
быть вытяжной и приточной. Разновидностями вытяжной вентиляции являются:
защитные кожухи, вытяжные шкафы, кабины, аспирационные устройства. К приточной
местной вентиляции относятся воздушные души, воздушные оазисы, завесы.
По способу действия различают вентиляцию приточную, вытяжную и
приточно-вытяжную, а также аварийную. Аварийная предназначена для устранения
загазованности помещения в аварийных ситуациях.
Независимо от типа вентиляции к ней предъявляются следующие общие
требования: объем приточного воздуха должен быть равен объему вытяжного
воздуха; элементы системы вентиляции должны быть правильно размещены в
помещении; потоки воздуха не должны поднимать пыль и не должны вызывать
переохлаждения работающих; шум от системы вентиляции не должен превышать
допустимого уровня.
В основе устройства вентиляции лежит воздухообмен, то есть объем воздуха
помещения, заменяемый в единицу времени L (м/ч). Потребный воздухообмен
определяется в соответствии со СНиП 2.04.05-86 расчетным путем из условий
удаления из воздуха помещения избыточных вредных веществ, теплоты и влаги.
Оценка влияния производственных факторов в окружающей среде и на рабочих
местах.
Опыт проводится в калориметре ТА-5 «Тантал». После окончания опыта
вскрывается калориметрическая бомба и осуществляется выброс из нее вредных
веществ, образовавшихся во время опыта, и тепла, выделившегося в процессе
эксперимента.
В процессе эксперимента образуются вредные вещества:
§ Монооксид углерода
§ Диоксид азота
2. Тепло, выделившееся в процессе эксперимента
=8.1кДж
Пдк вредных веществ
§ Монооксид углерода - 20 мг/м3
§ Оксид азота NO2 - 2 мг/м3
Расчет вентиляции.
Для защиты атмосферы рабочего места от выделяемых вредных веществ при
механической обработке деталей, над рабочим местом устанавливается один из
видов местных отсосов, а именно вытяжной зонт (рис.1).

Рис.1. Схема вытяжного зонта: 1 - вытяжная панель; 2 - калориметр.
Исходные данные:
G =
1.91 мг/c - производительность по газовым
выбросам;
h =
1.5м - высота расположения отсоса;
a×2b -
размер источника, где a=0.13м,
b=0.13м;=0.54кВт - производительность
источника по теплоте;
Wв=0.2 м/c - скорость движения воздуха в помещении;
A= a + 0.24h = 0.49 м
B= 1.2b=0.26 м
Определим осевую скорость и расход воздуха в струе на уровне всасывания.
Находим эквивалентный по площади радиус.
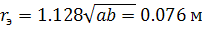
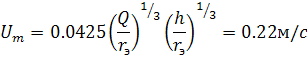
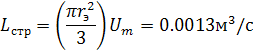
Определяем поправочный коэффициент, учитывающий подвижность воздуха в
помещении.

где
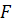
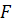 -
площадь всасывающего отверстия;
-
площадь всасывающего отверстия; 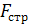
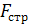 - площадь
сечения затопления струи;
- площадь
сечения затопления струи; 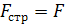
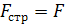 - на
разгонном участке конвективной струи.
- на
разгонном участке конвективной струи.
Находим
относительный предельный расход отсоса:
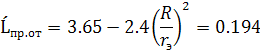
где
R = 1.2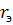
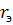
Находим
предельный расход отсоса, обеспечивающий полное улавливание струи, при
минимальной производительности отсоса.
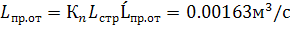
Определим предельную и относительную предельную избыточную концентрацию
вредных веществ в удаляемом отсосом воздухе, соответствующего режиму
предельного улавливания.
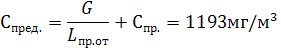
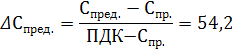
где
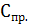
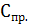 -
концентрация вредных примесей в приточном воздухе общеобменной вентиляции; ПДК
- предельно допустимая концентрация вредных веществ в воздухе рабочей зоны.
-
концентрация вредных примесей в приточном воздухе общеобменной вентиляции; ПДК
- предельно допустимая концентрация вредных веществ в воздухе рабочей зоны.
Определяем
оптимальное значение эффективности улавливания вредных веществ
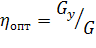
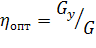
и
соответствующее значение
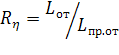
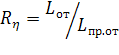 .
. 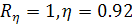
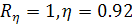
Определяем
требуемую производительность отсоса, обеспечивающего оптимальную эффективность
улавливания вредных веществ.
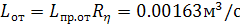
Определяем
количество уловленных и концентрацию выделения вредных веществ в воздухе,
отсасываемых местным отсосом
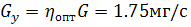
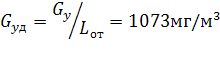
Расчет
вентилятора.
Схема
вентилятора представлена на рис. 2.
Исходные
данные:
L=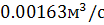
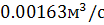 -
производительность вентилятора;
-
производительность вентилятора;
P=2000Па - напор
вентилятора;=2900 об/мин - частота вращения вентилятора.
Находим
критерий быстроходности:
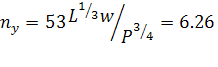
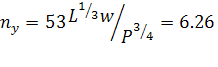
где
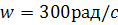
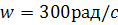 .
.
Определяем
диаметр входа в вентилятор:
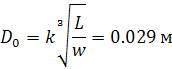
Где
k=1.65.
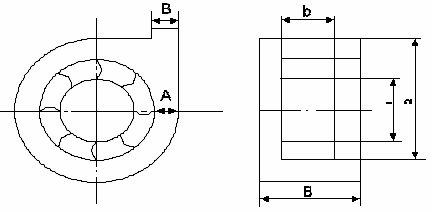
Рис.
2. Схема вентилятора
Диаметр
входа в колесо (на лопатки колеса) D0 принимаем, по конструктивным соображением, равным D1= 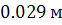
Определяем
диаметр колеса.
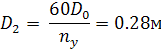
Определяем
ширину корпуса.
В=0,885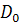
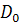 = 0,03 м
= 0,03 м
Определяем
ширину колеса.
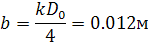
Определяем
величину раскрытия корпуса.
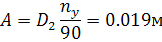
Определяем
число лопаток.
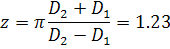
Определяем
мощность вентилятора.
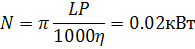
где
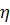
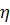 - КПД
вентилятора.
- КПД
вентилятора.
Определяем
мощность электродвигателя.
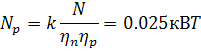
где
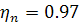
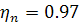 -
коэффициент, учитывающий потери на трение в подшипниках;
-
коэффициент, учитывающий потери на трение в подшипниках; 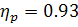
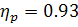 -
коэффициент, учитывающий потери в передаче от двигателя к вентилятору;
-
коэффициент, учитывающий потери в передаче от двигателя к вентилятору; 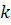
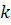 =1.14 -
коэффициент запаса мощности.
=1.14 -
коэффициент запаса мощности.
По
расчетной мощности электродвигателя и частоте вращения выбираем
электродвигатель:
· Асинхронный электродвигатель Ao2-11-2;
· Мощность 0.8 кВт;
· Частота вращения 3000 об/мин;
· КПД=77.5%.
Выводы по главе: В данном разделе произведен расчет вентиляции для
калориметрического опыта, а также приведены инструкции для обеспечения
безопасной работы на ЭВМ.
Заключение
Результатом данной работы является разработанная методика исследования
ВЭМ на базе нанодисперсных компонентов.
Методика обеспечивает экспериментальное определение дисперсности, формы и
оценку состава наночастиц.
Разработана расчетная методика определения калорийности
высокоэнергетических материалов. Показана возможность существенного увеличения
калорийности при использовании малоразмерных наночастиц.
Предложена методика экспериментального определения калорийности ВЭМ на
базе нанодисперсных компонентов. Выбрано оборудование, определена технология
проведения экспериментальных работ, проведена оценка точности получения искомых
величин.
Разработанная методика призвана обеспечить создание нового поколения ВЭМ
- энергетических материалов на базе нанокомпонентов.
Список
литературы
1. Русанов
А.И. Удивительный мир наноструктур// Журнал общей химии. - Санкт-Петербург:
Наука, 2002.т.72. Вып.4. - 532-533с
2. http://www.nanorf.ru/
. council.gov.ru/files/journalsf/item/20070420103719.pdf.
4. Фролов
Ю.Г. Курс коллоидной химии. Поверхностные явления и дисперсные системы.Учебник
для вузов. - 2-е изд., перераб. и доп. - М: Химия, 1989.- 464с
5. Захарченко
В.Н. Коллоидная химия. - 2-е изд., перераб. и доп. - М: Высшая школа., 1989. -
238с
. Рыбалкина
М., Нанотехнологии для всех - М.: Nanotechnology News Network, 2005. - 444 с
. Бабук В.А.,
Салимуллин Р.М. Наночастицы как компонент высокоэнергетических конденсированных
систем. Сборник трудов Шестой Всероссийской конференции "Внутрикамерные
процессы и горение в установках на твёрдом топливе и в ствольных системах"
(ICOC-2008). Россия, С.-Петербург, 8-10 сент. 2008 г. - Ижевск: ИПМ УрО РАН,
2008, с. 292-301.
8.
Valery A. Babuk, Runar M. Salimullin. Thermodynamic Method of Determination of
Nanocomponent’s Characteristics of High Energy Material. Proceedings of the
Fourth International Symposium on Non-equilibrium Processes, Plasma,
Combustion, and Atmospheric Phenomena (held in Sochi, Russia, October 5 - 9,
2009).
9. Родионов
Г.В. Твердые ракетные топлива. Учебное пособие. - Ленинград: ЛМИ, 1976 - 206с.
. Де Лука
Л.Т., Галфетти Л., Северини Ф., Меда Л., Марра Ж., Ворожцов А.Б., Седой В.С.,
Бабук В.А.. Физика горения и взрыва. - 2005г, т.41, №6
11.
www.eunnet.net/metod_materials/borisov/chapter6/6_2.pdf
<http://www.eunnet.net/metod_materials/borisov/chapter6/6_2.pdf>
.
www.eunnet.net/metod_materials/borisov/chapter6/6_2.pdf
.www.element.ur.ru
<http://www.element.ur.ru>
. www.tokyo-boeki.com
<http://www.tokyo-boeki.com>
. Целинский И.В. Применение
высокоэнергетических материалов в технике и народном хозяйстве//Соросовский
образовательный журнал.- Москва: Международная Соросовская Программа
Образования в Области Точных Наук <http://ru.wikipedia.org/w/index.php?title=ISSEP&action=edit&redlink=1>,
2001. Вып.11. - 46-47с
. Бабук В.А. Параметры
продуктов сгорания в камере и на срезе сопла ракетного двигателя. Методические
указания к лабораторной работе. - Санкт-Петербург: БГТУ, 2001. - 13с
. Родионов Г.В. Твердые
ракетные топлива. - Санкт-Петербург: ЛМИ, 1976. - 206 с.
.<http://www.krugosvet.ru/enc/nauka_i_tehnika/tehnologiya_i_promyshlennost/KALORIMETRIYA.html#lit>
. Кирьянов К.В.
Калориметрические методы исследования. Учебно методический материал по программе
повышения квалификации «Современные методы исследования новых материалов
электроники и оптоэлектроники для информационно-телекоммуникационных систем». -
Нижний Новгород, 2007 - 76 с.
.Походун А.И., Шарков А.В.
Измерение теплофизических величин. Учебное пособие// Экспериментальные методы
исследований. - Санкт-Петербург: ИТМО, 2006. - 69-84с/