Способы получения и свойства красителей и оптических отбеливателей
Введение
Красители синтетические - органические соединения,
используемые для крашения различных (преимущественно волокнистых) материалов и
изделий. Представляют собой главным образом окрашенные соединения, некоторые
бесцветные соединения, например отбеливатели оптические, а также
соединения, из которых красители образуются после нанесения на окрашиваемый
материал, например азогены, фталоцианогены, кубогены, исходные вещества для
окислительного крашения. Цвет красителя обусловлен наличием в его молекуле хромофорной
системы - достаточно развитой открытой или замкнутой системы сопряженных
кратных связей и связанных с ней электронодонорных и (или) электроноакцепторных
заместителей. Кроме того, в молекулах красителей могут содержаться
заместители, придающие им различные свойства, например: способность
растворяться в водных (SO3H, COOH, аммониевые или др. ониевые группы) или
неводных (додецил, тpeт-бутил или др. алкил) средах; образовывать
внутрикомплексные соединения с металлами (напр., группы ОН и СООН в opтo-положении
друг к другу); химически связываться с окрашиваемым материалом (остаток моно-
или дихлортриазина, группа SO2CH2CH2OSO3H и др.). Красители синтетические
должны образовывать окраски, устойчивые к различным физико-химическим
воздействиям в процессах последующей переработки окрашенных материалов и при их
эксплуатации, например к обработке горячей водой (заварка) и насыщенным паром
(декатировка), к действию активного хлора, высоких температур (в расплавах
полимеров), света, морской воды, к погодным условиям, стирке, глажению, поту,
трению в сухом и мокром состояниях. Эти свойства оцениваются по пятибалльной
шкале, только прочность к свету - по восьмибалльной. Набор требований,
предъявляемых к красителю, определяется назначением и способом производства окрашенного
материала. Помимо устойчивости к различным воздействиям, красители
синтетические характеризуют также по окраске, чистоте их оттенка.
Целью проекта является собрать и проанализировать
литературный материал по красителям, оптическим отбеливателям, способам их
получения, свойства.
Общие сведения
В течение многих веков для крашения тканей, изготовления
косметических препаратов, а позднее и художеств, красок применяли красители
природные-ализарин, индиго, кармин и др. (всего ок. 30). В 1771 действием
HNO3 на индиго получен первый краситель синтетический - пикриновая кислота; в
1843 ее получили из более доступного сырья - фенола, что позволило в 1849
начать производство кислоты для крашения шелка. Возникновение промышленности
синтетических красителей стало возможным лишь после открытия Н.Н. Зининым
(1842) универсального метода получения анилина и других ароматических аминов
(см. Зинина реакция). В 1855 Я. Натансон получил из анилина
красный синтетический краситель, вторично открытый в 1859 Э. Вергеном и
названный фуксином (цвет фуксии). В 1856 У. Перкин старший синтезировал
розоватолиловый мовсин (цвет мальвы). Огромная заслуга Перкина в том, что он
оценил практическое значение своего открытия и уже через год начал
промышленного производство мовсина, а также нитробензола и анилина, необходимых
для его производства. Год 1856 считается датой возникновения промышленности
синтетических красителей, названной анилинокрасочной. В 1858 П. Грисс открыл
реакцию диазотирования, а в 1864 - азосочетания, что привело к
синтезу азокрасителей. В 1869 К. Гребе и К. Либерман осуществили синтез
ализарина, с которого началось производство антрахиноновых синтетических
красителей; в развитии его большую роль сыграл каталитический способ получения
1-антрахинонсульфокислоты, открытый М.А. Ильинским. В 1880 А. Байер
синтезировал индиго, промышленное производство которого началось в 1896, после
чего последовал синтез других индигоидных красителей. В 1873 открыты сернистые
красители, а с 1893 организовано их промышленное получение. В 1901 получен
первый синтетический кубовый краситель индантрон, в 1903 налажено производство
полиметиновых красителей, в 1936 - фталоцианиновых, начало 20 в. Синтетические
красители почти полностью вытеснили природные. Крупнейшие достижения после 2-й
мировой войны - выпуск активных и дисперсных красителей. Общее число известных
К. составляет св. 6500, а производимых в мире - около 1500. До 1914
монополистом в области производства была Германия, на долю которой (вместе с
филиалами ее фирм за рубежом) приходилось около 90% мирового прoизводства,
равного 150,3 тыс. т/год. В СССР анилинокрасочная промышленность создана в годы
первой пятилетки при активном участии видных ученых - Н.Н. Ворожцова-старшего,
В.М. Родионова, М.А. Ильинского, А.Е. Порай-Кошица, В.А. Измаильского, Р.К.
Эйхмана и др. К 1937 крупные пром. производства красителей. организованы в 18
странах, и потребление красителей достигло 235 тыс. т/год. В 80-х гг. 20 в.
производство К. составило 770-860 тыс. т/год, причем 70% этого количества
приходится на долю США, ФРГ, СССР, Японии, Англии, Швейцарии и Франции. Термин
"краситель" введен в 1908 А.Е. Порай-Кошицем.
Номенклатура
Красители выпускают в продажу обычно под торговыми
названиями. За рубежом - это фирменные названия, защищенные патентами. Поэтому
часто одинаковые по химическому строению красители разные фирмы выпускают под
различными названиями. Перечень выпущенных на рынок красителей с указанием
фирмы-изготовителя, свойств и, если известно, строения приводятся в справочнике
Colour Index. В основе отечеств, номенклатуры лежит техническая классификация
К. Первое слово в названии К. определяет принадлежность к классу или группе по
технической классификации (например, прямой, кислотный, катионный,
жирорастворимый, пигмент), второе - цвет красителя (желтый, сине-черный,
чисто-голубой, ярко-красный и т.п.). Затем могут перечисляться наиболее важные
свойства красителя (например, светопрочный, прочный) или указывается его
принадлежность к классу по химической классификации (например, антрахиноновый,
фталоцианиновый), а также специфические области применения (для кожи, меха и
т.п.). После слов в необходимых случаях вводят буквы, указывающие на оттенок
окраски: Ж, К, С, 3, О - соответственно желтоватый, красноватый, синеватый,
зеленоватый, основной оттенок данного цвета; цифры перед буквами означают более
резко выраженный оттенок (напр., красный 2С имеет более синеватый оттенок, чем
красный С). Другие буквы указывают на особые свойства красителя. Так,
"X" в названии прямых К. означает, что устойчивость окраски к стирке
может быть повышена обработкой солями хрома, а в названия кубовых и активных -
что крашение можно производить по так называемому холодному способу (при
пониженной температуре 30-40 °С), "М" в название прямых, кислотных и
дисперсных К. с. указывает, что они являются комплексами металлов (Сu, Со или
др.), в названиях кубовых - что они предназначены для крашения меха, в названия
лаков - что это соли марганца. Сохранились традиционные названия, например
индиго, ализарин, сафранин.
Классификация
Существуют техническая (по областям применения) и химическая
(по химическому строению) классификации красителей синтетических. Первой
пользуются в практической работе - при применении и определении потребностей в
данной группе красителей, при планировании и статистической отчетности, второй
- при изучении химии и технологии красителей.
Техническая классификация учитывает свойства
красителей, природу окрашиваемых материалов, способы крашения, характер связи
красителя с субстратом. По растворимости красители делят на водорастворимые,
нерастворимые в воде, нерастворимые в воде и органических растворителях и
растворимые в органических средах. К последним относятся ацетонорастворимые
красители, жирорастворимые красители, спирторастворимые красители. К
водорастворимым относятся кислотные, основные, протравные, прямые, активные
красители. Кислотные красители - главным образом соли
сульфокислот, реже - карбоновых, а также анионные комплексы некоторых
красителей с металлами, преимущественно с Сr и Со; основные красители - соли
органических оснований. В водных растворах кислотные - диссоциируют с
образованием цветных анионов, основные - цветных катионов. Обладают сродством к
субстратам амфотерного характера (шерсть, натуральные шелк и кожа,
синтетические полиамиды); основные К. с., применяемые для крашения
полиакрилонитрильного волокна (называется катионными красителями) обладают
сродством к субстратам кислотного характера. Окрашивают из водных растворов,
вступая в солеобразование с имеющимися в молекулах указанных субстратов
основными или кислотными группами соответственно. Удерживаются на субстрате
главным образом с помощью ионных связей. К целлюлозе сродства не имеют, но
основные красители могут окрашивать целлюлозные материалы после предварительной
обработки их ("протравления") веществами кислотного характера,
например таннинами, фенольными смолами (так называемое крашение по танниновой
или др. протравам). Протравные красители содержат заместители, способные
образовывать устойчивые комплексы с металлами. Не обладают достаточным
сродством к целлюлозе, но закрепляются на ней по "протраве" солями
металлов (напр., Сr3+, Al3+, Fe2+) вследствие образования нерастворимых
внутрикомплексных соединения. При наличии кислотных групп обладают сродством к
субстратам амфотерного характера и окрашивают их подобно кислотным красителям,
причем при обработке солями металлов (главным образом Сr3+ ) также образуется
комплекс (протравные для шерсти, или хромовые К. с.). Прямые красители - соли
сульфокислот. В водных растворах диссоциируют с образованием цветных
анионов, обладающих сильно выраженной способностью к ассоциации. Обладают
сродством к целлюлозным материалам и окрашивают их из водных растворов в
присутствии электролитов (NaCl, Na2SO4 или др.) без протравы. Удерживаются на
целлюлозных волокнах силами Ван-дер-Ваальса и водородными связями. Активные
красители содержат в молекулах группы, способные в процессе крашения
реагировать с ОН-, NH2- и др. группами окрашиваемых субстратов, образуя с ними
устойчивые ковалентные связи. Окрашивают целлюлозные, белковые и синтетические
полиамидные материалы. К нерастворимым в воде относятся кубовые, сернистые,
дисперсные красители, к нерастворимым в воде и органических средах - пигменты
органические и лаки (напр., лаки основные), представляющие
собой нерастворимые соли или внутрикомплексные соединения, растворимых
красителей; цвет и оттенок пигмента (лака) зависят не только от химической
природы, но и от структуры кристаллической решетки и размеров частиц. Кубовые
красители содержат в молекуле две сопряженные друг с другом карбонильные
группы; в щелочной среде восстанавливаются, например действием Na2S2O4, с
образованием растворимых солей, обладающих сродством к целлюлозным
материалам. После крашения лейкосоединения под действием воздуха (О2+СО2)
переходят в исходный нерастворимый краситель, закрепляющийся в микропорах
субстрата. Сернистые красители аналогично кубовым при применении
восстанавливаются под действием Na2S в щелочной среде в растворимые
лейкосоединения, обладающие сродством к целлюлозным материалам. Дисперсные
красители окрашивают ацетаты целлюлозы и синтетические гидрофобные, главным
образом полиэфирные, материалы из водных дисперсий. При крашении образуют
твердый раствор в субстрате; удерживаются силами Ван-дер-Ваальса и водородными
связями. Растворимые производные нерастворимых красителей - кубозоли, тиозоли,
цианалы- производные соответствующих кубовых, сернистых,
фталоцианиновых. Их выпускают для упрощения процессов крашения и расширения
областей применения. Обладают свойствами растворимых красителей (прямых -
кубозоли и тиозоли, основных - цианалы). После крашения кубозоли и тиозоли
превращаются на субстрате в исходные нерастворимые в воде соответсвующие
кубовые и сернистые красители, цианалы - в нерастворимые производные
фталоцианиновых красителей. Особую группу представляют нерастворимые,
синтезируемые в процессе крашения непосредственно на субстратах из
промежуточных продуктов - азогенов, компонентов для окислительного
крашения (чаще всего ароматические амины, диамины и аминофенолы или их смеси), кубогенов,
фталоцианогенов, образующих соответствующие азокрасители, ариламиновые
(азиновые), кубовые и фталоцианиновые красители.
Производство, выпускные формы, применение
Производство красителей - отрасль промышленности тонкого
органического синтеза. Их получают в результате проведения многостадийного
химического синтеза из промежуточных продуктов, производимых, в свою очередь,
из ароматических и гетероароматических соединений, вырабатываемых угле- и
нефтехимической промышленностью. Часто из одного промежуточного продукта
получают несколько красителей. Промежуточные продукты, кроме того, широко
используют для производства лекарственных веществ, пестицидов, ростовых веществ
и многих других продуктов. Как правило, производство промежуточных продуктов
организовано на заводах, которые вырабатывают красители. Для промышленности
характерны: многоассортиментность, малотоннажность отдельных производств,
многостадийность получения большинства красителей (иногда 10 и более стадий).
Это затрудняет механизацию и автоматизацию производства и, следовательно,
улучшение экономических показателей. Основные пути прогресса в промышленности:
разработка для каждого вида крашения триад красителя (желтый - пурпурный -
голубой), смешением которых по данным расчета цветности на ЭВМ можно получить
смесовые марки любых цветов и оттенков; организация гибких производств,
позволяющих с помощью небольшого числа аппаратов повышать мощности производить
широкий ассортимент продукции; изыскание возможностей использования одних и тех
же промежуточных продуктов для синтеза возможно большего числа и применения в
качестве промежуточных продуктов соединений, производимых для синтеза
лекарственных веществ, пестицидов, фотоматериалов и др. Полученные в результате
химического синтеза красителей обычно мало пригодны для непосредственного
применения в крашении и особенно в печатании. Чтобы красители были удобны в
применении и для повышения степени их использования (например, исключение
механических потерь, более полная выбираемость из красильных ванн) из них
готовят выпускные формы. Это стандартизованные товарные формы, в которых К. с.
поступают потребителям; кроме красителя, взятого в строго определенной
концентрации, в их состав входят различные вспомогательные вещества. Основные
выпускные формы: непылящие порошки, содержащие краситель, ингибитор пыления
(например, авиационное или трансформаторное масло, силоксановая жидкость либо
дибутилфталат; в количестве обычно около 1,5%), диспергатор, смачиватель (для
нерастворимых в воде), соль минералов, кислоты - обычно NaCl, Na2SO4 или Na2CO3
(для водорастворимых), стабилизатор и др.; гранулы, содержащие краситель,
связующее, диспергатор, смачиватель; пасты, содержащие краситель, смачиватель,
диспергатор, антифриз; жидкости - растворы красителей главным образом в воде,
реже в органических растворителях. На основе одного и того же красителя может
быть приготовлено несколько выпускных форм. Так, прямые, кислотные, протравные
и активные красители производят в виде непылящих порошков, реже гранул и
жидкостей, кубозоли - в виде непылящих порошков, катионные - в виде растворов и
непылящих порошков. Применяют их для крашения волокон и различных текстильных
материалов, кожи, мехов, бумаги, древесины и др.; растворимые в органических
средах - для окрашивания бензинов, парафина, спиртов, восков, растительных
жиров, синтетических волокон при получении их формованием в массе, пластмасс,
резин. Их используют также в цветной и черно-белой кинематографии и фотографии,
в электрофотографии аналитической химии, в медицине (средства диагностики, при
биохимических исследованиях), в жидкостных лазерах, в различных физических
приборах в качестве полупроводников и элементов, обладающих фотопроводимостью и
некоторыми другими свойствами, как катализаторы.
Отбеливатели
оптические
Многие материалы белого цвета имеют неприятные для глаза
(большей частью, желтоватого) оттенки. Это означает, что такие тела отражают
падающий не них белый свет не полностью; часть лучей, преимущественно
фиолетовых, синих и зеленых, поглощается телом.
В промышленности для отбеливателя натуральных волокон и
целлюлозы уже давно используются гипохлориты натрия и кальция и другие
вещества, обесцвечивающие окрашенные примеси в результате их окисления и
хлорирование или, реже, восстановления, например, дитионитом натрия
(«химическое отбеливание»).
В быту, а также при производстве бумаги, белых красок и
эмалей также давно практикуется подкраска желтоватых материалов красителями
синего цвета (ультрамарин и др.).
Смешение желтых и дополнительных синих лучей создает впечатление
белизны; однако это является результатом поглощения части (желтых и синих)
лучей, т.е. степень белизны понижена. Кроме того, и желтые, и синие лучи в
данном случае не спектрально-чистые, поэтому материалы приобретают сероватый
оттенок.
С конца тридцатых для придания белизны изделиям стали
применяться флуоресцирующие вещества - оптические отбеливатели.
Отбеливатели оптические (флуоресцентные отбеливатели) -
бесцветные или слабоокрашенные органические соединения, способные поглощать
ультрафиолетовые лучи в области 300-400 ммк и преобразовывать их в синий
или фиолетовый свет с длиной волны 400-500 ммк, который компенсирует
недостаток синих лучей в отражаемом материалом свете.
Благодаря этому при нанесении отбеливателя на желтоватые
материалы в спектре отражения не только компенсируется недостаток фиолетовых,
голубых и синих лучей, но спектр становится даже богаче этими лучами по
сравнению со спектром падающего света. Глаз воспринимается это как более
высокую степень белизны. Конечно, эффект отбеливания достигается только в том
случае, если источник света содержит ультрафиолетовые лучи; при освещении
электрическими лампами накаливания флуоресцентные отбеливатели не «работают».
Нужно отметить, что оптические отбеливатели эффективны только для слегка желтоватых
или желтовато-сероватых материалов. Более интенсивно окрашенные материалы,
например натуральные волокна или бумагу, предварительно отбеливают химически.
Эффективность действия оптических отбеливателей резко падает в присутствии
солей железа и других тяжелых металлов, а также ароматических и
гетероциклических соединений, сильно поглощающих ультрафиолетовые лучи.
Большая часть отбеливателей, выпускаемых для целлюлозных
материалов, принадлежит к стильбен-триазиновым производным:

Их применяют на различных стадиях изготовления и обработки
натуральных и синтетических материалов. Методы оптического отбеливания в
основном близки способам крашения; в частности, отбеливание целлюлозных
материалов сходно с крашением их прямыми красителями. Однако для достижения
нужного эффекта требуется значительно меньшее количество отбеливателей, чем
красителей. Водонерастворимые отбеливатели можно применять в высокодисперсной
форме или в виде раствора в органических растворителях. Промышленность
выпускает отбеливатели под названием «белофоры» («бланкифоры»).
Отбеливающее действие отбеливателей оптических основано на том,
что излучаемый ими свет компенсирует недостаток синих лучей в свете, отражаемом
материалом (в этом их коренное отличие от химических отбеливателей, напр. Сl2,
Н2О2). В отличие от подсинивания ультрамарином
<#"522963.files/image002.gif">
Соединения I обладают сродством к целлюлозе
<#"522963.files/image003.gif">
Соединения III и IV отбеливают природные, полиамидные и ацетатные
волокна <#"522963.files/image004.gif">
Методы оптического отбеливания в основном аналогичны методам
крашения <#"522963.files/image005.gif">
Нитратор представляет собой стальной аппарат с рубашкой и
двумя охлаждающими змеевиками. Он снабжен двумя мешалками - турбинной и
пропеллерной, посаженными на один вал. Верхняя мешалка служит для интенсивного
смешенного подаваемых на нее из мерников бензола, нитросмеси и отработанной
кислоты. Нижняя мешалка (пропеллерная) работает как осевой насос. Подача
бензола и нитросмеси автоматически регулируется по заданному соотношению, а
количество отработанной кислоты - по температуре в реакторе, которая
поддерживается на уровне 50-60 С. Реактор работает в режиме полного смешения.
Из нитратора реакционная масса подается в спиральные теплообменники, где
охлаждается до 25 - 30 С. Из холодильника реакционного масса поступает в
отстойник непрерывного действия, где происходит разделение нитробензола и
отработанной кислоты. Так как разность плотностей нитробензола и отработанной кислоты
велика, расслаивание происходит быстро. Перед утилизации этой кислоты из нее
экстрагируют нитробензол. Экстракцию ведут бензолом, который частично нитруется
азотной кислотой, содержащихся в отработанной серной кислоте. Бензол со следами
нитробензола подается в емкость, а оттуда в нитратор. А отработанную кислоту
отправляют на денитрацию.
Материальный баланс
Материальный баланс рассчитан на схему, производительность
которой составляет 10000 тонн бисбензоксазола в год. Расчет материального
баланса приведен в таблице.
Стадия получения нитробензола
|
Приход
|
|
|
№
|
М, кг/кмоль
|
кг/ч
|
кмоль/ч
|
%масс.
|
|
Бензол
|
78
|
1,66
|
0,021
|
20
|
|
Азотная кислота
|
63
|
1,328
|
0,021
|
16
|
|
Серная кислота
|
98
|
3,96
|
0,04
|
47,7
|
|
Вода
|
18
|
1,355
|
0,075
|
16,33
|
|
Сумма
|
|
8,3
|
|
100
|
|
Расход
|
|
|
Нитробензол
|
123
|
0,97
|
0,0079
|
11,69
|
|
Серная кислота
|
98
|
3,96
|
0,04
|
|
Вода
|
18
|
1,503
|
0,084
|
18,11
|
|
Азотная кислота
|
63
|
0,811
|
0,013
|
9,77
|
|
Динитробензол
|
168
|
0,02
|
0,00012
|
0,241
|
|
Бензол
|
78
|
0,9956
|
0,0128
|
12
|
|
Сумма
|
|
8,3
|
|
100
|
Теоретический выход нитробензола m=14538,7*123/78=22926,4кг/год
Фактический выход нитробензола m=0,37*22926,4=8482,77кг/год
Из справочника: конверсия бензола=40%; концентрация
бензола=99%масс; состав нитрующей смеси, %масс: азотная кислота =20; серная
кислота = 59,6; вода = 20,4. Массовое соотношение бензол: нитрующая смесь=1:4.
Потери бензола = 4%масс. Динитробензол =2%масс.
. Мтех(C6Н6)=14538,7/365/24=1,66кг/ч
. Мчист.(С6Н6)=1,66*0,99=1,64кг/ч
Mприм(С6Н6)=1,66-1,64=0,02кг/ч
. Потери бензола 4%масс.
Мп(С6Н6)=1,64*0,04=0,0656кг/ч
М(С6Н6)=1,64-0,0656=1,57кг/ч
V(С6Н6)=1,57/78=0,02кмоль/ч
. Получение в целевой реакции нитробензола
V(С6Н5NO2)=Vпрор(С6Н6)
Vпрор(С6Н6)=0,02*0,4==0,0081кмоль/ч
Мпрор(С6Н6)=0,0081*78=0,63кг/ч
М(С6Н5NO2)=0,0081*123=0,996кг/ч
. Количество динитробензола, 2%масс.
М(С6Н5(NO2)2)=0,996*0,02=0,02кг/ч
V(С6Н5(NO2)2)=0,02/168=0,000119кмоль/ч
. Количество прореагировавшего нитробензола
Vпрор(С6Н5NO2)=V(С6Н5(NO2)2)=0,000119кмоль/ч
Vост(С6Н5NO2)=V(С6Н5NO2)-Vпрор(С6Н5NO2)
Vост(С6Н5NO2)=0,0081-0,000119=0,008кмоль/ч
Мост(С6Н5NO2)=0,008*123=0,97кг/ч
. Не прореагировавший бензол
V(С6Н6)=V(С6Н6)-Vпрор(С6Н6)
V(С6Н6)=0,02-0,0081=0,012кмоль/ч
М(С6Н6)=0,012*78=0,93кг/ч
. Общая количество нитрующей смеси
Мсмеси=4*Мтех(НNO3)=4*1,66=6,64кг/ч
. Нитрующая смесь
Мвсего(НNO3)=Мсмеси*0,2=6,64*0,2=1,328кг/ч
Vвсего(НNO3)=1,328/63=0,0211кмоль/ч
М(Н2SO4)=Мсмеси*0,596=6,64*0,596=3,96кг/ч
Vвсего(Н2SO4)=3,96/98=0,04кмоль/ч
М(Н2О)=6,64*0,204=1,355кг/ч
V(Н2О)=1,355/18=0,075кмоль/ч
. Количество прореагировавшей азотной кислоты
V0(НNO3)=Vпрор.цел(НNO3)+Vпобоч.(НNO3)
V0(НNO3)=0,0081+0,000119=0,00822кмоль/ч
. Количество не прореагировавшей азотная кислота
Vост(НNO3)=V(НNO3)-V0(НNO3)
Vост(НNO3)=0,0211-0,00822=0,0129кмоль/ч
Мост(НNO3)=0,0129*63=0,811кг/ч
. Количество образовавшей воды
V(Н2О(1))=V(С6Н5NO2)=0,0081кмоль/ч
V(Н2O(2))=V(С6Н5NO2)=0,000119кмоль/ч
М(Н2O(1))=0,0081*18=0,146кг/ч
Стадия получения нитротолуола
|
Приход
|
|
|
№
|
М, кг/кмоль
|
кг/год
|
кмоль/год
|
%масс.
|
|
Нитробензол
|
123
|
8482,77
|
68,97
|
70,89
|
|
Метиленхлорид
|
50,5
|
3482,76
|
68,97
|
29,11
|
|
Сумма
|
|
11965,54
|
|
100
|
|
Расход
|
|
|
Нитротолуола
|
137
|
9448,29
|
68,97
|
78,96
|
|
Соляная кислота
|
36,5
|
2517,25
|
68,97
|
21,04
|
|
Сумма
|
|
11965,54
|
|
100
|
Стадия получения 4-хлор-3-нитротолуола
|
Приход
|
|
|
№
|
М, кг/кмоль
|
кг/год
|
кмоль/год
|
%масс.
|
|
Нитротолуол
|
137
|
9448,29
|
68,97
|
65,87
|
|
Хлор
|
71
|
4896,56
|
68,97
|
34,13
|
|
Сумма
|
|
14344,85
|
|
100
|
|
Расход
|
|
|
4-хлор-3-нитротолуол
|
171,5
|
11827,6
|
68,97
|
82,45
|
|
Соляная кислота
|
36,5
|
2517,24
|
68,97
|
17,55
|
|
Сумма
|
|
14344,85
|
|
100
|
Стадия получения 4-гидрокси-3-нитротолуола
|
Приход
|
М, кг/кмоль
|
кг/год
|
кмоль
|
%масс.
|
|
4-хлор-3-нитротолуол
|
171,5
|
11827,6
|
68,97
|
90,5
|
|
Вода
|
18
|
1241,38
|
68,97
|
9,5
|
|
Сумма
|
|
13068,97
|
|
100
|
|
Расход
|
|
|
4-гидроксинитротолуола
|
153
|
10551,73
|
68,97
|
80,74
|
|
Соляная кислота
|
36,5
|
2517,24
|
68,97
|
19,26
|
|
Сумма
|
|
13068,97
|
|
100
|
Стадия получения 3-амино-4-гидрокситолуола
|
Приход
|
|
|
№
|
М, кг/кмоль
|
кг/год
|
кмоль/год
|
%масс.
|
|
4-гидрокстинитротолуола
|
153
|
10551,73
|
68,97
|
96,23
|
|
Водород
|
6
|
413,79
|
68,97
|
3,77
|
|
Сумма
|
|
10965,52
|
|
100
|
|
Расход
|
|
|
3-амино-4-гидрокситолуола
|
123
|
8482,76
|
68,97
|
77,36
|
|
Вода
|
36
|
2482,76
|
68,97
|
22,64
|
|
Сумма
|
|
10965,52
|
|
100
|
Стадия получения отбеливателя бисбензоксазола
|
Приход
|
|
|
№
|
М, кг/кмоль
|
кг/год
|
%масс.
|
|
3-амино-4-гидрокситолуол
|
246
|
8482,76
|
34,48
|
67,96
|
|
Малеиновая
кислота
|
116
|
4000
|
34,48
|
32,04
|
|
Сумма
|
|
12482,76
|
|
100
|
|
Расход
|
|
|
Бисбензоксазол
|
290
|
10000
|
34,48
|
80,11
|
|
Вода
|
72
|
2482,76
|
34,48
|
19,89
|
|
Сумма
|
|
12482,76
|
|
100
|
Расходные коэффициенты, материальный индекс и
коэффициент безотходности
Расходные материалы:
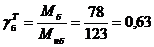 , кг/кг
, кг/кг 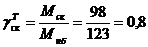 кг/кг
кг/кг
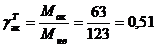 , кг/кг
, кг/кг
Материальный индекс:

Коэффициент безотходности:
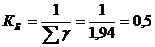
Расчет аппарата
Проектный
расчет
Температурная
схема теплообменного аппарата.
краситель
отбеливатель химический производство

Из справочника:
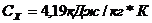 , при
, при 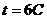
 {1}
{1}
Разница температур
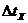 =24-18=6
=24-18=6
Тепловая нагрузка
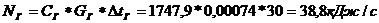

Массовый расход для воды


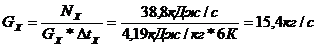
Температурный напор по концам теплообменника
 =60-24=36
=60-24=36 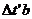 =20-18=2
=20-18=2
Средний температурный напор
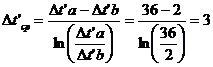
Средняя температура каждого вещества


Оцениваем поверхность теплообменника

Из справочник: коэффициент
теплопередачи  {1}
{1}
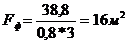
Из справочника:
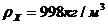 ,
, 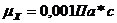 {1}
{1}
Необходимая скорость при  , диаметр труб. пространства
, диаметр труб. пространства 
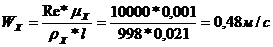
Сечение труб. Пространства

Из таблицы 4.12 {1} находим:
Условие 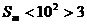 и
и 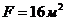 удовлетворяет двухходовому теплообменнику:
удовлетворяет двухходовому теплообменнику:
диаметром кожуха D=400мм,
длиной труб 
общее число труб n=100
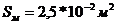 межтрубное проходное сечение
межтрубное проходное сечение
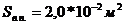 внутреннее проходное сечение
внутреннее проходное сечение
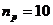 число рядов труб по вертикали для горизонтальных аппаратов
число рядов труб по вертикали для горизонтальных аппаратов
h=250мм расстояние между перегородками
Поверочный тепловой расчет
коэффициент теплоотдачи
число Рейнольдса для холодного вещества, зная, что 
скорость холодного вещества
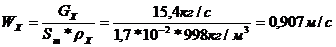
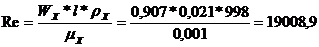

Из справочника С(вода)=4,19кДж/кг*К, 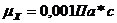 ,
,  {1}
{1}
Критерий Нуссельта {1}

Где  ,
, 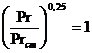
Критерий Прандтля {1}

Находим критерий Нуссельта

Коэффициент теплоотдачи для воды {1}
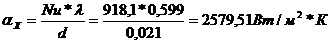
Коэффициент теплоотдачи для горячего вещества {1}
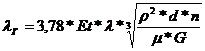
Температура в К
Т=40+273=313К
Коэффициент теплопроводности 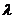 {5}
{5}
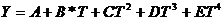
Где 

Массовая плотность для горячего вещества 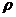 {5}
{5}
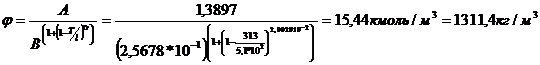
Где 
Динамическая вязкость горячего вещества 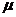 {5}
{5}

Где 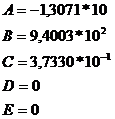
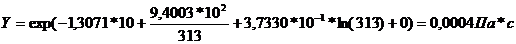
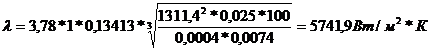
Тепловая нагрузка
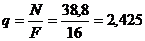
Температурный напор для подведения тепла со стороны горячего теплоносителя к
стенке
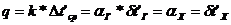
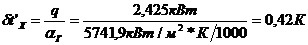

Температура стенки со стороны горячего

Температура стенки со стороны холодного теплоносителя на стенку
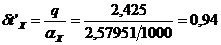
Температура стенки со стороны холодного
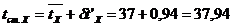
Термическое сопротивление стенки
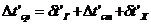

Сопротивление стенки, учитывающее степень загрязнения: {1}
Материал стенки - сталь нержавеющая,  -к. теплоперед.
-к. теплоперед.
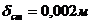 - толщина
- толщина
Из справочника находим {1}

Сопротивление стенки

Константа теплопередачи
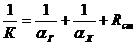

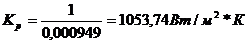
Поверхность теплообмена


Погрешность состоит 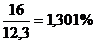
Следовательно, l=2м с F=16, запас поверхности 16/12,3=1,301%
Гидравлический расчет
Межтрубное пространство
Сечение в штуцерах диаметром d=0,15м{4}
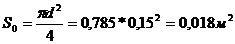
Плотность водяного пара
Средняя линейная скорость потоков



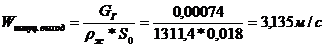
Трубное пространство
Средняя линейная скорость потоков

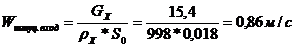
Гидравлическое сопротивление, при  (число ходов)=2
(число ходов)=2
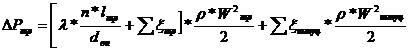
Коэффициент гидравлического трения
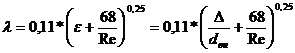
Из справочника: {4}

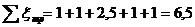
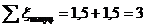
Тогда
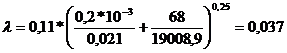
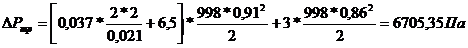
Очистка сточных вод в
производстве красителей
Производство красителей связано с
использованием огромного количества воды, значительная часть которой раньше
сбрасывалась в загрязненном состоянии.
Наибольшее распространение дли очистки
сточных вод от красителей получили метод окисления активным хлором,
электролитические методы. На АО «ХИМПРОМ» осуществляется очистка сточных вод
производств красителей и полупродуктов на одной установке с раствором
гипохлорита натрия, а на другой газообразным хлором в присутствии раствора едкого
натра. В последнем случае в реакторе из хлора и едкого натра или воды
образуются гипохлорит натрия и хлорноватистая кислота:
Cl2+ 2NaOH = NaOCl + NaCl + Н2О
Cl2 + Н2O = HOCl + HCl
В настоящей работе изучается очистка
сточных вод от красителей активным хлором.
Физико-химические основы процесса. Органические
красители являются сложными органическими соединениями с определенными
функциональными группами. Например, молекула красителя «Активный ярко-желтый
53» имеет следующее строение:
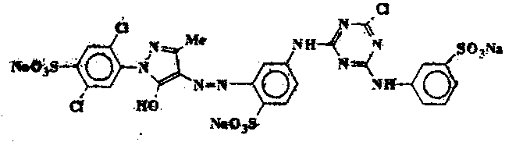
Фильтраты, образующиеся при производстве
красителей, характеризуются следующими показателями: цвет, рН, ХПК, порог
разбавления по цвету, сухой и прокаленный остатки. В частности для фильтратов
активных красителей величина порога разбавления, имеет огромное значение и в
зависимости от типа красителя колеблется в пределах 15000-500000. ХПК
колеблется в пределах 1-30 г О2/л. Раствор гипохлорита натрия образуется в ходе
производства жидкого хлора в качестве побочного продукта с концентрацией 80-185
г/л.
При обработке сточных вод, содержащих
красители, раствором гипохлорита натрия происходит разрушение молекулы
красителя с образованием углекислоты, карбоновых кислот и неорганических
соединений:
Обеззараживание воды, отправляемой на очистные сооружения
производится хлором, гипохлоритом натрия, получаемым на месте в электролизерах,
или прямым электролизом сточных вод.
Расчетная доза активного хлора берется в зависимости от
предшествующей очистки сточных вод (после механической очистки - 10 мг/л; после
механической очистки при эффекте отстаивания более 70 и неполной биологической
очистки - 5 мг/л; после полной биологической, физико-химической очистки - 3
мг/л.).
Сооружение для обеззараживания состоит из установки для
хлорирования, склада хлора, смесителя и контактного резервуара. Хлорное хозяйство
должно обеспечивать возможность увеличения расчетной дозы хлора в 1,5 раза без
изменения вместимости складов для реагентов.
Установки для хлорирования похожи на установки, используемые
для обеззараживания природных вод.
Установки для обеззараживания должны обеспечивать уменьшение
бактериальных загрязнений до нормативных. Количество бактерий кишечной группы,
оставшихся в воде после обеззараживания, а также по концентрации остаточного
хлора при обеззараживании хлором или его производными дают представление о
эффективности работы сооружений. Количество остаточного хлора должно составлять
не менее 1,5 мг/л при обязательном контакте воды с хлором не менее 30 мин, а
бактерий кишечной группы в 1 л сточной воды до 1000 шт.
При обработке сточных вод, содержащих красители,
раствором гипохлорита натрия происходит разрушение молекулы красителя с
образованием углекислоты, карбоновых кислот и неорганических соединений:
Красители + NaOCl (HOCl) = CO2 + продукты
окисления(Карбоновые кислоты) + N2 + Na2SO4 + NaCl (HCl)
Скорость и степень очистки зависят от
температуры, рН, продолжительности процесса и расхода окислителя
"активного хлора". В качестве критерия снижения цветности выбран
порог разбавления по цвету. При обработке стоков гипохлоритом натрия происходит
снижение суммы органических примесей, которые оцениваются ХПК, определяемым
бихроматным методом.
Заключение
Отбеливатели оптические (флуоресцентные отбеливатели) -
бесцветные или слабоокрашенные органические соединения, способные поглощать
ультрафиолетовые лучи. Они применяются для оптического отбеливания хлопка,
синтетических волокон, бумаги, шерсти, натурального шёлка, кожи, меха,
пластических масс и других материалов. Бесцветные материалы приобретают при
этом высокую степень белизны, а окрашенные - яркость и контрастность.
Их применяют на различных стадиях изготовления и обработки
натуральных и синтетических материалов. Методы оптического отбеливания в
основном близки способам крашения; в частности, отбеливание целлюлозных
материалов сходно с крашением их прямыми красителями. Однако для достижения
нужного эффекта требуется значительно меньшее количество отбеливателей, чем
красителей. Водонерастворимые отбеливатели можно применять в высокодисперсной
форме или в виде раствора в органических растворителях. Промышленность
выпускает под названием «белофоры» («бланкифоры»).
В этой работе были изучены свойства бисбензоксазола,
рассмотрены все стадии его получения.
Бисбензоксазол широко применяется для отбеливания
пластических масс и синтетических волокон в массе, особенно полиэфирных;
мировое производство достигается 50 тыс.т.
В настоящее время из общего количества отбеливателей около
50% расходуется для изготовления моющих средств, 10-15% непосредственно в
текстильной промышленности, 20-25% для отбеливания бумаги. Текстиль отбеливают
в процессе изготовления волокон и поверхностного - на текстильных фабриках и в
быту. Так, отбеливатели обычно добавляют в синтетические моющие средства (1%).
При стирке изделий одновременно производится и их отбеливание. При действии света
их волокна и нанесенные на них отбеливатели постепенно приобретают желтоватый
оттенок, добавление отбеливателей в моющие средства позволяет снять эту
желтизну.
Однако, промышленности необходимы универсальные отбеливатели
стойкие ко всем воздействиям (солнечный свет, влажность и т.д.). Следует
ожидать, что это произойдёт.
В условиях переходной экономики, международного
экономического кризиса российская анилинокрасочная промышленность практически
перестала функционировать, что само собой оттолкнула нас от достижения этой
цели практически на несколько десятков лет.
Список использованной литературы
1. Павлов
К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и
аппаратов химической технологии. - Л.:Химия, 2006. - 576 с.
2. Чекалин
М.А., Пасет Б.В., Иоффе Б.А. Технология органических красителей и промежуточных
продуктов. - Л.:Химия, 1980.-472 с.
3. База
данных ChemCAD
4. Электронный
ресурс http://ru.wikipedia.org/wiki/
5. Электронный
ресурс http://www.prochrom.ru/ru/view/
6. Электронный
ресурс http://www.chemistry.ssu.samara.ru/
7. Электронный ресурс
http://slovari.yandex.ru/