Роль фельдшера в профилактике анемии у детей младшего возраста
Введение
По данным ВОЗ, в мире, население которого сейчас приближается к 6 млрд
человек, около 2 млрд страдает ЖДА.
Из всех анемий 80% составляет ЖДА. Возрастные группы, в которых анемия
встречается чаще, - это женщины детородного возраста, беременные и дети 12-17
лет. Распространенность ЖДА у детей меняется с возрастом. В период быстрого
роста дефицит железа достигает 50% и превалирует у девочек (они быстрее растут,
и у них появляются менструальные кровопотери). Среди детей от многоплодной
беременности и детей с опережающим обычные нормы ростом ЖДА на первом году
жизни выявляется более чем в 60% случаев. В пожилом возрасте половые различия
постепенно исчезают, и даже отмечается преобладание мужчин с дефицитом железа.
По данным официальной статистики Минздрава России, из числа родивших женщин в
2009 г. имели анемию 34,4%, а в 2010 г. - 43,9%- В отдельных группах населения
частота встречаемости железодефицитных состояний достигает 50% и даже 70-80%.
Дефицит железа, по данным ВОЗ 2010 г., определяется у 20-25% всех младенцев,
43% детей в возрасте до 4 лет и до 50% подростков (девочки).
Анемии иногда представляют непосредственную угрозу жизни и сопровождаются
отстаиванием детей в физическом, а иногда и в умственном развитии.
За последние 10 лет в области гематологии внедрены новые биохимические,
иммунологические, цитологические, молекулярно генетические методы исследования.
Благодаря созданию метода клонирования кроветворных клеток в селезенке
облученных мышей, хромосомного анализа, трансплантации костного мозга доказана
роль стволовой клетки как основополагающей единицы кроветворения. Крупным
достижением является факт установления первичного поражения стволовых клеток
при апластических анемиях. В связи с вышеизложенным данная темя представляется
весьма актуальной.
Цель работы - изучение болезненности ЖДА у детей г.о. Сызрань и роль
фельдшера в их профилактике.
Задачи работы:
· Рассмотреть теоретические основы анемии у детей.
· Изучить учебную, методическую литературу, монографии, статьи,
информацию Интернета по исследуемой теме.
· Провести анализ статистических данных болезненности ЖДА у
группы детей, проживающих в районе обслуживания ДП №2, с выделением групп
риска, факторов, причин названной патологии.
· Проанализировать работу фельдшера в профилактике заболеваемости
ЖДА
Объект исследования: история развития детей форма №112, отчеты главного
специалиста г.о. Сызрани
1. Анатомо-физиологические особенности крови и органов
кроветворения у детей
На ранних этапах развития эмбриона (на 3-й неделе гестации) очаги
кроветворения появляются в так называемых кровяных островках - скоплениях
мезенхимальных клеток, расположенных в стенке желточного мешка. Наружные
элементы такого очага в результате дифференцировки уплощаются и образуют
эндотелий будущих сосудов, тогда как внутренние, округляясь и освобождаясь от
межклеточных связей, дают начало первичным кровяным тельцам. На 4-5-й неделе
эмбриогенеза выявляются примитивные кроветворные клетки. В этот период развития
зародыша человека кроветворение происходит внутри сосудов и называется стадией
ангиобласта.
В конце 5-6-й недели делящиеся кроветворные клетки обнаруживаются между
печеночными клетками, а также вне сосудов. К этому времени кроветворение в
желточном мешке постепенно прекращается, и печень становится центром гемопоэза.
Этот период может быть назван стадией экстрамедуллярного, в частности
печеночного, кроветворения. Кроветворная функция печени интенсивно развивается
до 5-7-го месяца внутриутробной жизни плода, затем начинает ослабевать, и к
моменту рождения ребенка в печени остаются лишь небольшие островки кроветворных
клеток. Кроветворение в эмбриональной печени преимущественно эритроидное.
Эритропоэтическая активность первых гемопоэтических органов (желточного мешка и
печени) связана в первую очередь с обеспечением дыхательной функции растущего
эмбриона.
Число лимфоидных клеток в печени зародыша с 7-й до 13-й недели не
превышает 1 % от всех кроветворных клеток. После 15-й недели содержание их
повышается до 9 %, что, вероятно, является результатом активной деятельности
вилочковой железы и костного мозга.
Дифференцировка Т-лимфоцитов является сложным многоэтапным процессом,
приводящим к образованию разных субпопуляций иммунокомпетентных Т-клеток.
Определяющим моментом считается созревание клеток в вилочковой железе.
Образование Т-лимфоцитов происходит в течение всей жизни человека. Весь путь
дифференцировки Т-клеток обычно делится на 3 основных этапа: дотимическое
развитие лимфоцитов в костном мозге, внутритимическая дифференцировка
лимфоцитов, миграция Т-лимфоцитов из вилочковой железы и заселение ими
периферических лимфоидных органов. Гистологически вилочковая железа формируется
быстро, корковый и мозговой слой хорошо различимы уже на 11-12-й неделе
внутриутробной жизни ребенка. Важно отметить, что, начиная с 20-й недели
внутриутробного периода, к моменту перемещения кроветворения в костный мозг
плод способен к адекватному иммунологическому ответу на антигены, проникающие к
нему через плаценту. Дифференцировка В-клеток, установление разнообразия
В-лимфоцитов, несущих разные классы поверхностных иммуноглобулинов, также
запрограммировано в эмбриогенезе. Уже на 9-й неделе внутриутробного развития в
печени выявляются В-лимфоциты, затем происходит постепенное их перемещение в
селезенку и костный мозг. Пролиферация и дифференцировка предшественников
В-клеток на начальных стадиях индуцируется ИЛ-7 и ФСК. Как только образовались
распознаваемые пре-В- и В-клетки, происходят их дальнейшая дифференцировка и
деление при участии иммуноглобулинового антигенного рецептора и Fc-рецептора,
стимулируемые растворимыми ИЛ-4 и ИЛ-6. После формирования плазматических
клеток, синтезирующих иммуноглобулины, ИЛ-6 и ГМ-КСФ стимулируют дополнительную
пролиферацию и секрецию антител, Пре-Т-клетки подвергаются сложной негативной и
позитивной селекции в тимусе, в процессе которой они «обучаются» распознавать
«свои» и «не свои» - чужеродные - клетки. Возникающие в результате зрелые
Т-клетки являются субъектами антиген- и цитокининдуцированной активности и
экспансии. Стимуляция антигеном в присутствии ИЛ-2 или антигеном в сочетании со
стимуляцией вспомогательными макрофагами либо дендритными клетками, которые
экспрессируют В7, или В7 2, ведет к прямой активации и CD4+, и CD8+ Т-клеток.
Первые макрофаги появляются на 4-й неделе внутриутробного развития в
портальных зонах печени. На 10-й неделе в этих же зонах обнаруживаются первые
гранулоциты, но их количество не превышает 8 % от общего количества клеток
крови. Начиная с 6-й недели в печени обнаруживаются мегакариоциты, но их очень
мало на протяжении всего внутриутробного развития.
В начале 4-го месяца, когда развиваются костная ткань и костный мозг,
возникает костномозговое кроветворение, которое постепенно начинает играть
главную роль. В пренатальном периоде костный мозг является красным, с
3-4-летнего возраста он заменяется на желтый в некоторых костях.
Во внеутробной жизни костный мозг продуцирует эритроциты, гранулированные
лейкоциты, тромбоциты и моноциты; в лимфатических узлах, селезенке, фолликулах,
пейеровых бляшках кишечника и других лимфоидных образованиях продуцируются
лимфоциты.
Для поддержания гемопоэтического самообновления и дифференцировки
стволовых клеток и их потомства они должны находиться в непосредственной
близости от негемопоэтических мезенхимальных клеток, называемых стромальными
клетками: фибробласты, эндотелмальные клетки, остеобласты, адипоциты,
располагающиеся на эндостальной поверхности в костномозговой полости. Для
гемопоэза гемопоэтические клетки нуждаются в растворимых гемопоэтических
факторах роста (колониестимулирующие факторы - КСФ): ИЛ-6, ГМ-КСФ, Г-КСФ, ФСК и
Й1-ЗЦРН-Зb)-лиганд- и мембраносвязанных молекулах присоединения. И тем и другим
их обеспечивают стромальные клетки.
Согласно современной теории кроветворения, различаются 6 классов
кроветворных клеток. (рисунок 1). Первый класс составляют стволовые
полипотентные клетки, способные к самоподдержанию в течение длительного времени
и к дифференцировке по всем листкам кроветворения. Следующим звеном (второй
класс) кроветворения являются ограниченно полипотентные клетки -
предшественники миелопоэза и лимфопоэза. Эти клетки обладают ограниченной
способностью к самоподдержанию. В процессе дальнейшей дифференцировки
образуются унипотентные клетки-предшественники (третий класс), которые также не
способны к длительному самоподдержанию, но способны к пролиферации и
дифференцировке. Основная количественная регуляция кроветворения осуществляется
на данном этапе. К этому классу относятся и две категории клеток -
предшественников лимфоцитов (Т-лимфоциты и В-лимфоциты). Клетки первых трех
классов относятся к бластным, или недифференцированным, формам.
За клетками-предшественниками следует четвертый класс - морфологически
распознаваемые, пролиферирующие клетки, являющиеся родоначальниками отдельных
рядов миелопоэза: гранулоцитопоэза, моноцитопоэза, эритропоэза,
мегалоцитопоэза, лимфопоэза.
Следующий класс (пятый) - это созревающие клетки (переходные формы).
Шестой класс - зрелые клетки с ограниченным жизненным циклом. Интенсивность
формирования клеток того или иного ряда зависит от действия гуморальных
регуляторов-стимуляторов (поэтинов) или ингибиторов. Функцию лей-копоэтинов
выполняют различные колониестимулирующие факторы. Ингибирование гранулопоэза
осуществляют лактоферрин и простагландины. Для эритроцитов стимуляторами
являются эритропоэтин и бурсообразующий фактор, для тромбоцитов - тромбопоэтин,
для Т-лимфоцитов - тимозин и Т-ростковый фактор.
Все фагоциты организма относятся к производным кроветворных клеток и
являются потомством моноцитов.
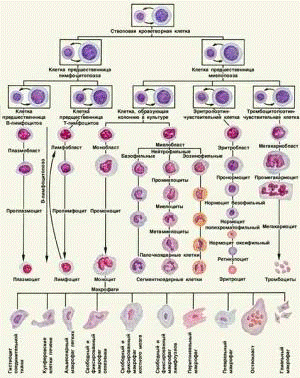
Рисунок 1. Схема кроветворения
Следует знать, что ОЦК у новорожденного с ранним пережатием пуповины
составляет 70 мл/кг, с отсроченным - 95 мл/кг, у недоношенных - 89-105 мл/кг.
Кроме того, ОЦК зависит и от положения новорожденного относительно плаценты, в
котором ребенок рождается и удерживается: выше плаценты в течение 1 мин или
ниже плаценты - соответственно плюс 30 мл или минус 30 мл крови.
Для всей кроветворной системы ребенка характерна крайняя функциональная
неустойчивость (лабильность), легкая ранимость самыми незначительными
экзогенными факторами. Уменьшение количества гемоглобина, эритроцитов,
появление незрелых элементов красной крови, лейкоцитоза с образованием молодых
клеток наблюдаются у детей значительно чаще и развиваются быстрее, чем у взрослых.
Образование очагов экстрамедуллярного кроветворения, а иногда и полный возврат
к эмбриональному типу могут быть обусловлены у детей не только тяжелой анемией
и лейкемией, как у взрослого, но часто происходят под влиянием различных
инфекций, интоксикаций и других вредно действующих факторов (бронхопневмония,
пиелонефрит, отит и др.). Эти патологические изменения гемопоэза, отражающиеся
в периферической крови на качестве и количестве форменных элементов,
встречаются тем чаще и выражены тем резче, чем младше ребенок.
2. Лабораторные показатели и их интерпретация
Эритроциты.
Концентрация Hb и количество
эритроцитов у детей разного возраста представлены в таблице 1-1,1-2.
Осмотическая резистентность эритроцитов в растворе хлорида натрия: минимальная
(начало гемолиза) - 0,36-0,4%. Срений диаметр эритроцитов составляет 7,2-7,5
мкм с вариацией от 4,8 до 9,5 мкм; он увеличивается при макроцитарных анемиях.
Средняя толщина эритроцитов - 1,85 - 2,1 мкм. Важно помнить, что в возрасте 1-6
мес имеет место физиологическое снижение концентрации Hb и количества эритроцитов. Определение концентрации Hb - основной метод установления
анемии, оно проводится при наличии ее клинических признаков или в порядке
обследования детски контингентов на обеспеченность железом.
Таблица 1.1. Содержание эритроцитов в крови в норме 0,5-2
года 3,7-5,2
|
Возраст Женщины, 10|2/л
|
Мужчины, 1012/л
|
|
Кровь из пуповины 3,9-5,5
|
3,9-5,5
|
|
1 -3 дня 4,0-6,6
|
4,0-6,6
|
|
1 нед 3,9-6,3
|
3,9-6,3
|
|
2 » 3,6-6,2
|
3,6-6,2
|
|
1 мес 3,0-5,4
|
3,0-5,4
|
|
2 »> 2,7-4,9
|
2,7-4,9
|
|
3-6» 3,1-4,5
|
3,1-4,5
|
|
3,4-5,0
|
|
|
3-12 лет 3,5-5,0
|
3,9-5,0
|
|
13-16» 3,5-5,0
|
4,1-5,5
|
|
17-19» 3,5-5,0
|
3,9-5,6
|
|
20-29 » 3,5-5,0
|
4,2-5,6
|
|
30-39 » 3,5-5,0
|
4,2-5,6
|
|
40-49 » 3,6-5,1
|
4,0-5,6
|
|
50-59 » 3,6-5,1
|
3,9-5,6
|
|
60-65 » 3,5-5,2
|
3,9-5,3
|
|
>65» 3,4-5,2
|
3,1-5,7
|
Таблица 1.2. Концентрация Hb в крови в норме
|
Возраст
|
Женщины, г/л
|
Мужчины, г/л
|
|
Кровь из пуповины
|
135-200
|
135-200
|
|
1-3 дня
|
145-225
|
145-225
|
|
1 нед
|
135-215
|
135-215
|
|
2 »
|
125-205
|
125-205
|
|
1 мес
|
100-180
|
100-180
|
|
2 »
|
90-140
|
90-140
|
|
3-6 мес
|
95-135
|
95-135
|
|
0,5-2 года
|
106-148
|
114-144
|
|
3-6 лет
|
102-142
|
104-140
|
|
7-12»
|
112-146
|
110-146
|
|
13-16»
|
112-152
|
118-164
|
|
17-19»
|
112-148
|
120-168
|
|
20-29 »
|
110-152
|
130-172
|
|
30-39 »
|
112-150
|
126-172
|
|
40-49 »
|
112-152
|
128-172
|
|
50-59 «
|
112-152
|
124-172
|
|
60-65 »
|
114-154
|
122-168
|
|
>65»
|
110-156
|
122-168
|
Лейкоциты.
Содержание лейкоцитов у детей разного возраста представлено в табл. 1-3.
в настоящее время нормативы содержания лейкоцитов повысились - как за счет
проведения более репрезентативных исследований, так и за счет применения машинных
методов их подсчета. Лейкоцитоз - содержание лейкоцитов выше 12*15 10/9 г/л,
нейтрофилез (у маленьких детей) - содержание нейтрофилов более 9-10*10/9 г/л,
нейтропения - менее 1*10/9 г/л. Лимфоцитоз у детей имеет физиологический
характер, лимфопенией следует считать показатели ниже 0,6*10/9 г/л.
Гемостаз - система, обеспечивающая жидкое состояние крови и, в
необходимых случаях, тромбообразование. Концентрация фибриногена у
новорожденного ниже, чем у старших детей (1,25-3 г/л); протромбина - также на
20 % ниже. Тромбоцитопению констатируют при содержании тромбоцитов менее
100*10/9 г/л, тромбоцитоз - более 400*10/9 г/л.
Таблица 1.3. Содержание лейкоцитов в крови в норме
|
Возраст
|
Величина, -109/л
|
|
Кровь из пуповины
|
9,9-27,6
|
|
24 ч
|
9,4-32,2
|
|
1 мес
|
9,2-13,8
|
|
12 мес-3 года
|
6,0-17,5
|
|
4 года
|
6,1-11,4
|
|
6 лет
|
6,1-11,4
|
|
10"
|
6,1-11,4
|
|
21 год
|
4,5-10,0
|
|
Взрослые
|
4,0-8,8
|
.1 Анемии
Анемия - это снижение содержания эритроцитов и/или концентрации Hb в крови, она может быть связана с их
наследственными дефектами, однако чаще обусловлена дефицитом железа или
гемолизом.
В детском возрасте могут возникнуть или манифестироваться все варианты
анемий, однако, отчетливо преобладают (до 90 %) анемии, связанные с дефицитом
веществ, необходимых для нормального кроветворения, в первую очередь - железа.
В то же время отдельные клинические формы анемий развиваются обычно в
результате разнообразных воздействий и имеют сложный патогенез. В нашей стране
анемия встречается в среднем у 40 % детей до 3 лет, у 1/3 - в пубертатном
возрасте, значительно реже - в другие возрастные периоды.
Это обусловлено высокой интенсивностью роста ребенка первых лет жизни и
подростка, сопровождающейся пропорциональным увеличением количества форменных
элементов и объема крови и высокой активностью эритропоэза.
В процессе кроветворения участвует весь костный мозг ребенка, организму
постоянно требуется большое количество железа, полноценного белка,
микроэлементов, витаминов.
Поэтому даже небольшие нарушения вскармливания, инфекционные воздействия,
применение лекарственных средств, угнетающих функцию костного мозга, легко
приводят к анемизации детей, особенно второго полугодия жизни, когда истощены
неонатальные запасы железа.
Длительно сохраняющаяся сидеропения вызывает глубокие тканевые и органные
изменения развитие гипоксии и расстройств клеточного метаболизма.
При наличии анемии замедляется рост ребенка, нарушается его гармоничное
развитие, более часто наблюдаются интеркуррентные заболевания, формируются
очаги хронической инфекции, отягощается течение других патологических
процессов.
.2 Классификация анемий
Патогенетическая классификация анемий
I. Анемии вследствие кровопотери (постгеморрагические):
а) острая постгеморрагическая анемия;
б) хроническая постгеморрагическая анемия.. Анемии
вследствие нарушения образования эритроцитов и гемоглобина:
а) железодефицитная анемия;
б) мегалобластные анемии, связанные с нарушением синтеза
ДНК;
в) гипопластическая (апластическая) анемия.. Анемия
вследствие усиленного кроворазрушения (гемолитические):
. Наследственные:
а) связанные с нарушением структуры мембраны эритроцитов
(микросфероцитарная анемия Минковского-Шаффара, овалоцитоз, акатоцитоз);
б) связанные с дефицитом ферментов в эритроцитах;
в) связанные с нарушением синтеза гемоглобина
(серповидноклеточная анемия, гемоглобинозы, талассемия).
. Приобретенные.
. Аутоиммунные.. Анемии смешанного генеза.
Морфологическая классификация анемий
I. Макроцитарная анемия (MCV> 100 мкм (фл); диаметр
эритроцитов > 8 мкм) (дефицит витамина В12 и фолиевой кислоты,
болезни печени, предлейкоз).
II. Микроцитарная анемия (MCV<80 мкм (фл), диаметр эритроцитов <
6,5 мкм) (дефицит железа, нарушения синтеза глобина, нарушение синтеза
порфирина и гемма).. Нормоцитарная анемия (MCV 81 -99 мкм (фл), диаметр
эритроцитов 7,2-7,5 мкм) (недавняя кровопотеря, гемолиз эритроцитов, гипо- и
апластическая анемия, миелофиброз).
Классификация анемий по цветовому показателю. Анемия гипохромная,
цветовой показатель < 0,8 (железодефицитная анемия, сидероахрестическая
анемия, талассемии).. Анемия нормохромная, цветовой показатель 0,85-1,05
(анемия при хронической почечной недостаточности, апластическая анемия, анемия
при заболеваниях печени, острая постгеморрагическая анемия).. Анемия
гиперхромная, цветовой показатель > 1,05 (В12-дефицитная анемия,
ахрестическая анемия, фолиеводефицитная анемия).
Классификация анемий в зависимости от способности костного мозга к
регенерации. Регенераторная форма анемии (с достаточной функцией костного
мозга) - ретикулоцитов больше 1% (при гемолитических анемиях, ретикулоцитарном
кризе при лечении витамином В12 пернициозной
анемии, после кровопотерь).. Гипорегенераторная форма анемий (с пониженной
регенераторной функцией костного мозга) - ретикулоцитов меньше 1% (при
железодефицитных анемиях, хронических кровопотерях).. Гипопластическая или
апластическая форма анемии (с резким угнетением процессов эритропоэза) -
ретикулоцитов менее 0,2% (при гипопластических анемиях, панмиелофтизе).
Об эритропоэтической функции костного мозга судят по содержанию в
периферической крови ретикулоцитов. Нормальное содержание ретикулоцитов 0,2-1%.
3.1 Железодефицитная анемия
.1.1 Этиология
Недостаток поступления железа в организм особенно часто наблюдают у детей
до 3 лет. Концентрация сывороточного железа у новорожденного 5-19 мкмоль/л, у
более старших - 10-30 мкмоль/л. Железодефицитная анемия также может быть
обусловлена кровопотерей, вскармливанием коровьим молоком, особенно парным
(термолабильный, повышающий проницаемость капилляров, фактор обуславливает
потерю крови до 7 мл/сут), нарушениях всасывания, авитаминозе С и др. По
критериям ВОЗ, при концентрации Hb
120-130 г/л диагностируют дефицит железа, 100-110 г/л - легкую анемию,70-100
г/л - выраженную, менее 70 г/л - тяжелую. Количество эритроцитов снижается в
меньшей степени, за счет чего уменьшается цветовой показатель.
Различные виды кровопотерь, приводящие к развитию постгеморрагической
железодефицитной анемии, по частоте распределяются следующим образом: на первом
месте находятся маточные кровотечения, затем кровотечения из пищеварительного
канала. Редко сидеропения может развиться после повторных носовых, легочных,
почечных, травматологических кровотечений, кровотечений после экстракции зубов
и других видах кровопотерь. В отдельных случаях к дефициту железа, особенно у
женщин, могут приводить частые кроводачи у доноров, лечебные кровопускания при
гипертонической болезни и эритремии.
Встречаются железодефицитные анемии, развивающиеся вследствие
кровотечений в закрытые полости с отсутствием последующей реутилизации железа
(гемосидероз легких, эктопический эндометриоз, гломические опухоли).
По статистическим данным, у 20 - 30 % женщин детородного возраста
наблюдается скрытый дефицит железа, у 8 - 10 % обнаруживается железодефицитная
анемия. Основной причиной возникновения гипосидероза у женщин, кроме
беременности, являются патологическая менструация и маточные кровотечения.
Полименорея может быть причиной уменьшения запасов железа в организме и
развития скрытого дефицита железа, а затем и железодефицитной анемии. Маточные
кровотечения в наибольшей мере увеличивают объем кровопотери у женщин и
способствуют возникновению железодефицитных состояний. Существует мнение о том,
что фибромиома матки, даже при отсутствии менструальных кровотечений, может
привести к развитию дефицита железа. Но чаще причиной анемии при фибромиоме
является повышенная кровопотеря.
Второе место по частоте среди факторов, вызывающих развитие
постгеморрагической железодефицитной анемии, занимают кровопотери из
пищеварительного канала, которые часто имеют скрытый характер и трудно диагностируются.
У мужчин это вообще основная причина возникновения сидеропении. Такие
кровопотери могут быть обусловлены заболеваниями органов пищеварения и
болезнями других органов.
Нарушения баланса железа могут сопровождать повторные острые эрозивные или
геморрагические эзофагиты и гастриты, язвенную болезнь желудка и
двенадцатиперстной кишки с повторными кровотечениями, хронические инфекционные
и воспалительные заболевания пищеварительного канала. При гигантском
гипертрофическом гастрите (болезни Менетрие) и полипозном гастрите слизистая
оболочка легко ранима и часто кровоточит. Частой причиной скрытых
труднодиагностируемых кровопотерь является грыжа пищевого отверстия диафрагмы,
варикозное расширение вен пищевода и прямой кишки при портальной гипертензии,
геморрой, дивертикулы пищевода, желудка, кишок, протока Меккеля, опухоли.
Легочные кровотечения - редкая причина развития дефицита железа. К развитию
дефицита железа иногда могут приводить кровотечения из почек и мочевых путей.
Очень часто сопровождаются гематурией гипернефромы.
В некоторых случаях кровопотери различной локализации, являющиеся
причиной железодефицитной анемии, связаны с гематологическими заболеваниями
(коагулопатиями, тромбоцитопениями и тромбоцитопатиями), а также с поражением
сосудов при васкулитах, коллагенозах, болезни Рандю - Вебера - Ослера,
гематомах.
Иногда железодефицитная анемия, обусловленная кровопотерей, развивается у
новорожденных и грудных детей. Дети в значительно большей степени чувствительны
к кровопотере, чем взрослые. У новорожденных потеря крови может быть следствием
кровотечения, наблюдавшегося при предлежании плаценты, ее повреждении при
кесаревом сечении. Другие труднодиагностируемые причины кровопотери в период
новорожденности и грудном возрасте: кровотечения из пищеварительного канала при
инфекционных заболеваниях кишок, инвагинации, из дивертикула Меккеля.
Значительно реже дефицит железа может возникать при недостаточном его
поступление в организм.
Дефицит железа алиментарного происхождения может развиться у детей и
взрослых при недостаточном его содержании в пищевом рационе, что наблюдается
при хроническом недоедании и голодании, при ограничении питания с лечебной
целью, при однообразной пище с преимущественным содержанием жиров и сахаров. У
детей может наблюдаться недостаточное поступление железа из организма матери
как следствие железодефицитной анемии во время беременности, преждевременных
родов, при многоплодности и недоношенности, преждевременной перевязке пуповины
до прекращения пульсации.
Длительное время считали основной причиной развития дефицита железа
отсутствие хлористоводородной кислоты в желудочном соке. Соответственно
выделяли гастрогенную или ахлоргидрическую железодефицитную анемию. В настоящее
время установлено, что ахилия может иметь только дополнительное значение в
нарушении всасывания железа в условиях повышенной потребности в нем организма.
Атрофический гастрит с ахилией возникает вследствие дефицита железа,
обусловленного снижением активности ферментов и клеточного дыхания в слизистой
оболочке желудка.
К нарушению всасывания железа могут приводить воспалительные, рубцовые
или атрофические процессы в тонкой кишке, резекция тонкой кишки.
Существует ряд физиологических состояний, при которых потребность в
железе резко увеличивается.
К ним относятся беременность и лактация, а также периоды усиленного роста
у детей. Во время беременности расходование железа резко повышается на
потребности плода и плаценты, кровопотерю при родах и лактацию.
Баланс железа в этот период находится на грани дефицита, и различные
факторы, уменьшающие поступление или увеличивающие расход железа, могут
приводить к развитию железодефицитной анемии.
В жизни ребенка существует два периода, когда наблюдается повышенная
потребность в железе.
Первый период - это первый - второй год жизни, когда ребенок быстро
растет.
Второй период - это период полового созревания, когда снова наступает
быстрое развитие организма, у девочек появляется дополнительный расход железа
вследствие менструальных кровотечений.
Причины анемии у новорожденных:
транзиторные возрастные особенности гемопоэза и внутриклеточного гемолиза
- так называемая физиологическая анемия доношенных и недоношенных детей
подавление функции костного мозга (врожденные и приобретенные)
наследственные гемолитические анемии
приобретенные гемолитические анемии, в т.ч. ГБН
алиментарная анемия
постгеморрагическая анемия
Железодефицитная анемия иногда, особенно в грудном и пожилом возрасте,
развивается при инфекционных и воспалительных заболеваниях, ожогах, опухолях,
вследствие нарушения обмена железа при сохраненном его общем количестве.
.1.2 Патогенез
Патогенез железодефицитной анемии связан с физиологической ролью железа в
организме и его участием в процессах тканевого дыхания. Оно входит в состав
гема - соединения, способного обратимо связывать кислород. Гем представляет
собой простетическую часть молекулы гемоглобина и миоглобина, который связывает
кислород, что необходимо для сократительных процессов в мышцах. Кроме того, гем
является составной частью тканевых окислительных энзимов - цитохромов, каталазы
и пероксидазы. В депонировании железа в организме основное значение имеет
ферритин и гемосидерин. Транспорт железа в организме осуществляет белок
трансферрин (сидерофилин).
Организм только в незначительной степени может регулировать поступление
железа из пищи и не контролирует его расходование. При отрицательном балансе
обмена железа вначале расходуется железо из депо (латентный дефицит железа),
затем возникает тканевый дефицит железа, проявляющийся нарушением ферментативной
активности и дыхательной функции в тканях, и только позже развивается
железодефицитная анемия.
.1.3 Клиника
Для длительно существующего дефицита железа при уровне
гемоглобина ниже 80 г/л характерны "эпителиальный",
астеноневротический, сердечно-сосудистый, гепатолиенальный и иммунодефицитный
синдромы, проявляющиеся изолированно или сочетающиеся между собой.
"Эпителиальный" синдром
Характеризуется бледностью кожи, ушных раковин и слизистых оболочек;
сухостью и шелушением вплоть до ихтиоза пигментацией кожи; дистрофией волос и
ногтей, бессимптомным кариесом зубов; анорексией, извращением обоняния и вкуса
(рiса сhlоrоtiса); ангулярным стоматитом, атрофическим глосситом, гастритом,
дуоденитом, расстройствами переваривания и всасывания; срыгиванием, тошнотой, рвотой,
неустойчивым стулом; нередко скрытыми кишечными кровотечениями.
При исследовании слизистой оболочки пищевода могут наблюдаться участки
ороговения, атрофического изменения в слизистой и мышечной оболочке
пищевода,что может проявиться сидеропенической дисфагией (симптом Пламмера -
Винсона - Бехтерева, проявляющийся затруднением при глотании сухой и плотной
пищи).
Астеноневротический синдром
Проявляется повышением возбудимости, раздражительностью, эмоциональной
неустойчивостью; постепенным отставанием в психомоторном, речевом и физическом
развитии; вялостью, апатией, утомляемостью, в тяжелых случаях негативизмом; у
детей старшего возраста отмечаются головные боли, головокружения.
Сердечно-сосудистый синдром
Сопровождается одышкой, сердцебиениями, тенденцией к
гипотонии, тахикардией, приглушением тонов, функционального характера
систолическим шумом, увеличением показателей выброса и гипертрофией левого
желудочка. На ЭКГ выявляются признаки гипоксических трофических изменений в
миокарде. Конечности постоянно холодные.
Гепатолиенальный синдром
Разной степени выраженности наблюдается у большинства
больных, особенно при сопутствующих дефицитах белка, витаминов и активном
рахите.
Синдром снижения местной иммунной защиты
Обусловлен поражением регенерирующих барьерных тканей, проявляется
частыми ОРВИ, пневмониями, кишечными инфекциями (в 2,5 - 3 раза чаще, чем у
здоровых) и ранним возникновением хронических инфекционных очагов. При легкой
степени анемии и преходящей сидеропении все указанные клинические синдромы могут
отсутствовать. В то же время поздняя диагностика и лечение приводят к
углублению дефицита железа и более тяжелым функциональным и метаболическим
расстройствам. В связи с этим большое значение в диагностике железодефицитных
анемий приобретают данные лабораторных исследований.
Обнаружение признаков анемии, сопровождающейся геморрагическими
проявлениями и температурной реакцией, связанной с нейтропенией и
тромбоцитопенией, заставляет заподозрить фолиево-дефицитную или приобретенную
апластическую анемию.
Тщательное выяснение анамнеза помогает выявить ряд врожденных и
наследственных анемий. Наличие у родственников больного снижения гемоглобина,
сопровождающегося желтухой и спленомегалией, позволяет заподозрить один из
вариантов гемолитической анемии или гемоглобинопатии. Более глубокое
гематологическое обследование позволяет выявить и дифференцировать редкие виды
анемии - наследственные апластические (типа Фанкони) или врожденные
(Даймонда-Блекфена), а также дизэритропоэтические и сидеробластные анемии.
Осмотр больного с проявлениями анемии также дает большую информацию.
Прежде всего, следует обращать внимание на поведение ребенка. При быстром
снижении гемоглобина или объема циркулирующей крови могут появиться признаки
анемической комы или гиповолемического шока - вялость, сонливость, потливость,
падение артериального давления, малый частый пульс и т.д.
При постепенном, длительном снижении гемоглобина дети адаптируются к
гипоксии и чувствуют себя удовлетворительно, не предъявляют жалоб.
При осмотре кожных покровов (желательно проводить при естественном
освещении) следует обращать внимание на их цвет. Для анемии характерна не
столько бледность, сколько желтушный, восковой оттенок кожи, особенно ушных
раковин. Если причина снижения гемоглобина - гемолиз, цвет кожных покровов,
слизистых оболочек, склер будет желтушным. Цвет слизистых оболочек в основном
соответствует окраске кожи. Следует иметь в виду, что бледность кожи и
слизистых оболочек может быть не только при снижении гемоглобина в крови, но и
при других патологических состояниях, в том числе некоторых видах врожденных
пороков сердца. Выявление желтушного окрашивания кожи и слизистых оболочек
требует специального обследования.
Критерии анемии у новорожденных: на 1-2 неделе жизни - снижение уровня
гемоглобина ниже 150 г/л (в капиллярной крови) и числа эритроцитов ниже
4,5Х10/12 г/л, гематокритного числа - ниже 0,4; на 3-4 неделе - снижение уровня
гемоглобина ниже 120 г/л.
"Ранняя" анемия недоношенных
Занимает особое место среди дефицитных анемий грудного возраста и имеет
сложный патогенез. Она развивается на 1 - 2 месяце жизни более чем у половины
недоношенных, а изредка и у доношенных детей ("физиологическая"
доброкачественная анемия), особенно при наличии неблагоприятного преморбидного
фона (внутричерепная родовая травма, пренатальная дистрофия, инфекция).
Отчетливые клинические проявления обычно отсутствуют. Отмечается только
бледность при снижении уровня гемоглобина ниже 80 г/л. При исследовании
периферической крови обнаруживают нормо- или гиперхромную, норморегенераторную
анемию, часто достигающую тяжелой степени. Основными причинами развития
"ранней" анемии считают усиленный "физиологический" гемолиз
эритроцитов, содержащих фетальный гемоглобин, и недостаточную функциональную и
морфологическую зрелость костного мозга, обусловленную преждевременным
появлением на свет или индивидуальными особенностями (у доношенных). Большое
значение придается также снижению продукции тканевых эритропоэтинов вследствие
гипероксии, возникающей при рождении ребенка. Однако в генезе этой анемии
немаловажную роль играют и дефициты многих необходимых для кроветворения
веществ, откладывающихся в депо только в последние 2 месяца беременности:
белка, витаминов С, Е, группы В, меди, кобальта, обеспечивающих всасывание,
транспорт, обмен и фиксацию железа в молекуле гема, а также стабильность
оболочек и мембран эритроцитов. Имеет значение и дефицит железа в депо,
завуалированный текущим гемолизом, но четко выявляемый микроцитозом и
гипохромией части эритроцитов, снижением уровня сывороточного железа и числа
сидероцитов в пунктате костного мозга. Как только иссякнут неонатальные запасы
железа, увеличивающиеся за счет массивного гемолиза, "ранняя" анемия
переходит в "позднюю" анемию недоношенных или алиментарно-инфекционую
анемию доношенных.
"Поздняя" анемия недоношенных (конституциональная)
Развивается на 3 - 4 месяце жизни в результате истощения неонатальных
запасов железа в депо. Клинические проявления ее обычно незначительны,
лабораторные данные свидетельствуют о преимущественном дефиците железа.
Алиментарная и алиментарно-инфекционная анемия наблюдается во втором полугодии
жизни у доношенных детей. Наряду с истощением депо железа в ее происхождении
играют роль нарушения вскармливания, одновременно вызывающие и дистрофию.
Инфекционные заболевания, чаще всего ОРВИ и отиты, способствуют более тяжелому
ее течению. Клинические и лабораторные проявления свидетельствуют о смешанной
природе анемии с преобладанием дефицита железа.
Врожденная гипопластическая анемия (Даймонда - Блекфана)
При рождении или в первые две недели жизни проявляется только у 15%
больных этим заболеванием. Отмечается бледность, вялость, апатичность, дети
плохо сосут, возможно, увеличение печени и селезенки, бывают врожденные
аномалии: трехфаланговые большие пальцы кистей, двухцветные волосы на голове,
вздернутый нос, широкая переносица, толстая верхняя губа и др.
Хлороз
Редкое заболевание у девочек в периоде полового созревания. Развивается
на фоне нарушения режима и эндокринной дисфункции. Проявляется слабостью,
утомляемостью, анорексией, извращением вкуса (рiса chloroticа),
головокружением, иногда обмороками, сердцебиениями, болями в эпигастрии,
тошнотой, рвотой, запорами. Характерны "алебастровая", в некоторых
случаях с зеленоватым оттенком, бледность кожи, нарушения менструального цикла
(олиго- или аменорея). Выздоровление часто самопроизвольное, возможны рецидивы.
Лабораторные исследования свидетельствуют о преимущественном дефиците железа.
Проявлением дефицита железа иногда является лихорадка, температура обычно
не превышает 37,5 °С и исчезает после лечения железом. Железодефицитная анемия
имеет хроническое течение с периодическими обострениями и ремиссиями. При
отсутствии правильной патогенетической терапии ремиссии неполные и
сопровождаются постоянным тканевым дефицитом железа.
.1.4 Диагностика
При постановке диагноза ЖДА решающее значение имеют данные лабораторных
исследований крови, костного мозга и обмена железа.
Картина крови характеризуется наличием признаков гипохромной
микроцитарной анемии. Обнаруживается снижение концентрации гемоглобина.
Количество эритроцитов вначале может быть нормальным. При значительном
дефиците железа оно также снижается, но в меньшей степени, чем уровень
гемоглобина. Отмечается низкий цветовой показатель (0,7-0,5) и уменьшение
средней концентрации гемоглобина в эритроцитах. Уменьшаются размер эритроцитов
и их насыщенность гемоглобином. В мазках крови преобладают небольшие
гипохромные эритроциты, аннулоциты (эритроциты отсутствием гемоглобина в
центре, в виде колец), эритроциты неодинакового размера и формы (анизоцитоз,
пойкилоцитоз). При тяжелых анемиях могут появляться отдельные эритробласты.
Количество ретикулоцитов не изменено. Только при анемии, развившейся
непоредственно после кровотечения количество ретикулоцитов повышается, что является
важным признаком кровотечения. Осмотическим резистентность эритроцитов мало
изменена или несколько повышена. Количество лейкоцитов имеет нерезко выраженную
тендецию к снижению. Лейкоцитарная формула мало изменена. Количество
тромбоцитов остается нормальным, а при кровотечениях несколько повышено.
В костном мозге при ЖДА можно обнаружить эритробластическую реакцию с
задержкой созревания и гемоглобинизации эритробластов. Костный мозг в
большинстве случаев гиперпластичен. Увеличивается соотношение клеток белого и
кранного ряда, количество последних преобладает. Лейкопоэз характеризуется
некоторым увеличением количества незрелых гранулоцитов.
Стадии развития болезни основаны на лабораторных исследованиях.
Регенераторная стадия: снижено количество гемоглобина, а количество
эритроцитов - в пределах нормы. Цветной показатель будет низким. Содержание
лейкоцитов, тромбоцитов - в пределах нормы. Отмечается микроцитоз, гипохромия
эритроцитов, незначительный ретикулоцитоз.
Гипогегенераторная стадия: снижено количество гемоглобина и эритроцитов.
Цветной показатель в пределах нормы. Содержание лейкоцитов, тромбоцитов
несколько уменьшено, ретикулоцитоза нет. Микро - и макроцитоз эритроцитов,
анизохромия. Костный мозг клеточный, но не активный, снижено количество эритробластов,
пойкилоцитоз, анизоцитоз.
Лабораторные критерии ЖДА:
. Снижение уровня гемоглобина (ниже 110 г/л)
. Снижение уровня эритроцитов (ниже 4 на 10*9 г/л)
. Снижение цветного показателя (ниже 0,85)
. Количество железа в сыворотке крови (негемоглобиновое железо). В норме
12-3- мкмоль в час. Определяется методом комплексования железа с
бета-фенантронином.
. Общая железосвязывающая способность сыворотки: измеряется количеством
железа, которое может связать 100 мл или 1 л сыворотки крови, в норме она
равняется 30-80 мкмоль на литр.
. В норме свободный сидероферрин составляет 2/3 - ¾ абсолютной способности сыворотки
связывать железо.
Главными критериями ЖДА являются снижение количества железа в сыворотке
крови и повышение общей железосвязывающей способности сыворотки.
После установления по клиническим и лабораторным данным железодефицитного
характера анемии, необходимо определить причину малокровия.
Дифференциальная диагностика
Дифференциальная диагностика причин ЖДА у новорожденных и грудных детей
требует учета всех факторов, которые могут привести к развитию дефицита железа
в этом возрасте (ЖДА у матери, недоношенность, многоплодная беременность,
небольшая масса тела при рождении, ранняя перевязка пуповины, кровопотеря у
ребенка во время родов, характер питания, возможные нарушения всасывания,
инфекции).
Дифференциальная диагностика по лабораторным показателям представлена в
таблице 2.
Таблица 2. Основные дифференциально-диагностические признаки гипохромных
анемий
|
Показатели
|
ЖДА
|
Сидероахрестические анемии
|
Талассемии
|
Железоперераспреде-лительные анемии
|
|
Сывороточное железо
|
↓
|
↑ / N (редко)
|
↑ / N
|
N / ↓
|
|
ОЖСС
|
↑
|
↓ / N
|
↓
|
N / ↓
|
|
Сывороточный ферритин
|
↓
|
↑ / N
|
↑
|
↑
|
|
Количество ретикулоцитов
|
N
|
N / ↑
|
↑
|
N / ↑
|
|
Мишеневидность эритроцитов
|
может быть
|
может быть
|
часто выражена
|
может быть
|
|
Базофильная пунктация эритроцитов
|
нет
|
есть
|
есть
|
нет
|
|
Содержание протопорфирина в эритроцитах
|
↑
|
↓ / ↑*
|
↑ / N
|
↑ / N
|
|
Количество сидеробластов и сидероцитов
|
↓
|
↑
|
↑
|
↑
|
|
Непрямой билирубин
|
N
|
N
|
↑
|
N
|
|
Проба с десфералом
|
"-"
|
"+"
|
"+"
|
"+"
|
|
Признаки гипосидероза
|
есть
|
нет
|
нет
|
нет
|
|
Эффект от препаратов железа
|
есть
|
нет**
|
нет**
|
нет
|
|
Примечание: ↑ - выше нормы; N - норма; ↓ - ниже
нормы * При наследственных формах содержание протопорфирина в эритроцитах
снижено, а для свинцовой интоксикации характерно повышение содержания
протопорфирина. ** Препараты железа категорически противопоказаны!
|
3.1.5 Лечение
Цель лечения - получение полной клинико-гематологической ремиссии,
которая достигается путем возмещения дефицита железа в крови и тканях;
восстановления метаболизма эритроцитов и других клеток; коррекции причин
(заболеваний), лежащих в основе ДЖ; коррекции висцеральных поражений ЖКТ, ССС,
гепатобилиарной систем.
Принципы лечения:
1. ЖДА может быть излечена только при использовании препаратов
железа. Никакие продукты питания неспособны вылечить ЖДА.
2. Препарат железа необходимо приниматьстрого в предписанной
терапевтической дозе.
. Лечение препаратами железа необходимо проводить не менее 2-3
месяцев. Только такой срок лечения позволяет восполнить насущную потребность в
железе и создать в организме необходимый резерв.
Диета показана в зависимости от степени тяжести анемии: при легкой и
среднетяжелой степенях и удовлетворительном аппетите - разнообразное,
соответствующее возрасту ребенка питание с включением в рацион продуктов,
богатых железом, белком, витаминами, микроэлементами. В первом полугодии -
более раннее введение тертого яблока, овощного пюре, яичного желтка, овсяной и
гречневой каш, во втором - мясного суфле, пюре из печени. Можно использовать
гомогенизированные консервированные овощи (пюре) добавлением мясных продуктов.
При тяжелой анемии, сопровождающейся обычно анорексией и дистрофией, вначале
выясняют порог толерантности к пище, назначая постепенно возрастающие
количества грудного молока или смесей. Недостаточный объем восполняют соками,
овощными отварами, у старший детей - минеральной водой. По достижении должного
суточного объема пищи постепенно меняют ее качественный состав, обогащая
необходимыми для кроветворения веществами. Ограничивают злаковые продукты и
коровье молоко, так как при их употреблении образуются нерастворимые фитаты и
фосфаты железа.
Патогенетическую
терапию осуществляют лекарственными препаратами железа (ферроцерон, резоферон,
конферон, актиферрин, ферроплекс, орферон) и витаминов. Железо чаще всего
назначают внутрь в виде закисных солей, преимущественно сульфата железа,
который всасывается и усваивается наиболее полно. Применяют также хлорид,
лактат, аскорбинат, глюконат и сахарат железа. Лекарственные препараты
изготавливают из солей железа в сочетании с органическими веществами
(аминокислотами, яблочной, янтарной, аскорбиновой, лимонной кислотами,
диоктилсульфосукцинатом натрия и т.д.), которые в кислой среде желудка
способствуют образованию легкорастворимых комплексных соединений железа -
хелатов и более полному его усвоению. Принимать железо рекомендуется между
кормлениями или за 1 час до еды, так как некоторые ингредиенты пищи могут
образовывать с ним нерастворимые соединения. Заливают препараты фруктовыми и
овощными соками, особенно полезны соки цитрусовых. Детям раннего возраста
средняя лечебная доза назначается из расчета 4 - 6 мг элементарного железа на 1
кг массы в сутки в 3 приема. Большая часть препаратов содержит 20 %
элементарного железа, поэтому расчетную дозу обычно увеличивают в 5 раз.
Индивидуальную дозу на курс лечения рассчитывают в миллиграммах по следующей
формуле:
Fe = Р х (78 -
0,35 х Hb),
где
Р - масса тела, кг; Hb - фактический уровень гемоглобина у ребенка, г/л.
Курс лечения обычно длительный, полная доза назначается до достижения
стабильного нормального содержания гемоглобина, а в течение последующих 2 - 4
месяцев (до 6 месяцев при тяжелой анемии доношенных и до 2 лет жизни у
недоношенных) дается профилактическая доза (1/2 лечебной 1 раз в день) для
накопления железа в депо и предупреждения рецидивов заболевания. При плохой
переносимости железа лечение начинают с малых доз, постепенно увеличивая их,
сменяют препараты. Эффективность лечения определяется по нарастанию гемоглобина
на (на 10 г/л, или 4 - 6 ед. в неделю), уменьшению микроцитоза,
ретикулоцитарному кризу на 7 - 10 день применения препаратов железа, повышению
содержания железа в сыворотке до 17 мкмоль/л и более, а коэффициента насыщения
трансферрина - до 30 %. Парентерально препараты железа назначают с
осторожностью при тяжелой форме анемии, непереносимости препаратов железа при
приеме внутрь, язвенной болезни, нарушениях всасывания, отсутствии эффекта от
энтерального применения, так как у детей возможно развитие гемосидероза.
Курсовую дозу рассчитывают по следующим формулам:
Fe (мг) = (масса
тела (кг) х [1000 - Fe (мкг/л)]) / 20
Или
Fe (мг) = Рх (78 - 0,35 Hb),
где
Fe (мкг/л) - содержание железа в сыворотке больного; Hb -
уровень гемоглобина периферической крови. Максимальная ежедневная разовая доза препаратов
парентерального железа при массе тела до 5 кг - 0,5 мл, до 10 кг - 1 мл, после
1 года - 2 мл, взрослым - 4 мл. Наиболее часто употребляют сахарат железа,
эффективно лечение фербитолом (сорбитол железа), ферковеном (2 % сахарат железа
с глюконатом кобальта в растворе углеводов). Препараты железа внутрь назначают
одновременно с пищеварительными ферментами с целью нормализации кислотности
внутренней среды, ее стабилизации. Для лучшего усвоения и всасывания назначают
соляную кислоту с пепсином панкреатин с кальцием, фестал. Кроме того, показаны
большие дозы аскорбиновой кислоты и другие витамины в возрастной дозировке
внутрь. Переливание цельной крови и эритроцитной массы производится только по
витальным показаниям (содержание гемоглобина ниже 60 г/л), так как оно лишь на
короткое время создает иллюзию выздоровления. В последнее время показано, что
гемотрансфузии подавляют активность синтез, гемоглобина в нормобластах, а в
некоторых случаях даже вызывают редукцию эритропоэза .
Содержание
железа в различных препаратах представлено в таблице 3.
Современные
препараты железа представлены в таблице 4. Препараты железа, применяемые у
детей представлены в таблице 5.
Таблица 3. Содержание железа в современных препаратах
|
Препарат
|
Содержание железа
|
|
Железа хлорид (усвоение 6%) («Гемофер») Железо
восстановленное, усвоение 1,5%
|
1,5 мг в 1 капле
|
|
Сульфат железа (усвоение 15%)
|
|
Железа сульфат + аскорбиновая кислота «Ферроплекс») Железа
сульфат + фолиевая кислота + цианокобаламин («Ферро-фольгамма») Железа
сульфат + аскорбиновая кислота («Тардиферон») Железа сульфат + аскорбиновая
кислота Сорбифер»)
|
10 мг в 1 таблетке 34,5-45 мг в 1 капсуле, 1 таблетке, 5
мл сиропа 80 мг в 1 таблетке 100-105 мг в 1 таблетке
|
|
Фумарат железа (усвоение 5-35%)
|
|
Железа фурамат + фолиевая кислота («Ферретаб»)
|
50-65 мг в 1 таб
|
|
Глюконат железа
|
|
Глюконат железа + марганца глюконат + меди глюконат
(«Тотема»)
|
|
Железа полимальтозат
|
|
Железа(3) гидроксид полимальтозат («Феррум Лек»)
|
50 мг в 5 мл сиропа , 100 мг в 1 таб, 100 мг в 2 мл
|
Таблица 4. Современные препараты Ре для лечения и профилактики ЖДА.
|
Препараты железа (II)
|
Препараты железа (III)
|
|
Сульфат Ре (II) • Актиферрин • Гемофер пролонгатум •
Тардиферон • Ферроплекс Хлорид Ре (II) • Гемофер Глюконат Ре (II) • Тотема
Фумарат Ре (II) • Ферронал
|
Ре (Ш) - гидроксид полимальтозный комплекс • Мальтофер •
Мальтофер Фол • Феррум Лек Ре (III) - гидроксид полимальтозный комплекс •
Феррум Лек (р-р для в/м введения) Ре (III) - гидроксид сахарозный комплекс •
Венофер (р-р для в/в введения)
|
Таблица 5. Препараты железа, применяемые у детей.
|
Препарат
|
Кол-во активного железа в препарате
|
|
Ранний возраст • Гемофер, капли • Феррум Лек, сироп •
Мальтолфер, капли • Актиферрин, капли Дошкольный возраст • Феррум Лек, сироп
• Мальтофер, сироп • Актиферрин, сироп • Тотема, р-р для приема внутрь •
Ферронат, р-р для приема внутрь • Ферроплекс Пубертатный возраст • Феррум
Лек, жев.таб. • Мальтофер, жев.таб. • Актиферрин • Гемофер пролонгатум •
Тардиферон • Тотема, р-р для приема внутрь • Ферроплекс
|
В 1 к.-1 мг В 1 мл-10 мг В 1 к.-2,5мг В 1 к. - 0,53г В 1
мл-10 мг В 1 мл- 10 мг В 1 мл-6,8мг В 1 мл-5мг В 1 мл-10 мг В 1 т. - 100 мг В
1 т.-100 мг В 1 кап.-34, 5мг В 1 т. - 105 мг В 1 т. -80 мг В 1 мл-5мг В 1
д.-10 мг В 1 д. - 10 мг
|
Об эффективности терапии железодефицитной анемии у детей можно судить уже
через 10-12 дней по увеличению ретикулоцитов в 2 раза по сравнению с исходным
количеством (так называемый ретикулоцитарный криз). Также оценивается прирост
гемоглобина, который должен составлять +10 г/л и более через месяц от начала
приема. Соответственно, достижение целевого уровня гемоглобина наблюдается в
среднем через 6-8 нед от начала терапии в зависимости от тяжести анемии. Однако
лечение препаратами железа должно проводиться в достаточных дозах и длительно
(не менее 3 мес) даже после нормализации уровня гемоглобина, с тем чтобы
пополнить запасы железа в депо.
Если же в течение 4 нед. не наблюдается значимого улучшения показателей
гемоглобина, то необходимо выяснить, почему лечение оказалось неэффективным.
Наиболее часто речь идет: о неадекватной дозе препарата железа; продолжающейся
или неустановленной кровопотере; наличии хронических воспалительных заболеваний
или новообразований; сопутствующем дефиците витамина В12; неверном диагнозе; глистной
инвазии и других паразитарных инфекциях.
.2 В12-дефицитная анемия
Впервые эту разновидность дефицитных анемий описал Аддисон в 1849 г., а
затем в 1872 г. - Бирмер, назвавший ее "прогрессирующей пернициозной"
(гибельной, злокачественной) анемией. Причины, вызывающие развитие анемий
указанного вида, могут быть разделены на две группы:
· недостаточное поступление витамина В12 в организм
с продуктами питания
· нарушение усвоения витамина В12 в организме
у детей обычно развивается вследствие недостатка фолатов - при
вскармливании козьим молоком (в женском и коровьем молоке их достаточно),
мальабсорбции, инвазии широким лентецом, при лечении сульфаниламидами,
метотрексатом.
Анемии, возникающие по этой причине, протекают тяжело, трудно поддаются
лечению, именно в связи с этим указанные формы мегалобластических дефицитных
анемий называют пернициозными или анемиями Аддисона - Бирмера. Витамин В12
(цианокобаламин) содержится в животных продуктах - мясе, яйцах, сыре, печени,
молоке, почках. В этих тканях он связан с белком. При кулинарной обработке, а
также в желудке цианокобаламин освобождается от белка (в последнем случае - под
влиянием протеолитических ферментов). В свободном состоянии витамин В12
образует комплекс с синтезирующимся в желудке гликопротеином и в таком виде
всасывается в кровь. Недостаток витамина В12 в указанных продуктах,
голодание или отказ от употребления пищи животного происхождения
(вегетарианство) нередко обусловливают развитие витамин В12 -
дефицитной анемии. Витамин В12 , поступающий в организм с пищей, по
предложению Кастла (1930) называют "внешним фактором" развития
анемии. Париетальные клетки желудка синтезируют термолабильный щелочеустойчивый
фактор (его обозначают как "внутренний фактор" Кастла), представляющий
собой гликопротеин с молекулярной массой 50 000 - 60 000. Комплекс витамина и
гликопротеина связывается со специфическими рецепторами клеток слизистой
оболочки средней и нижней части подвздошной кишки и далее поступает в кровь.
Незначительное количество витамина В12 (около 1 %) всасывается в желудке без
участия внутреннего фактора. Запасы витамина В12 в организме
достаточно велики (около 2 - 5 мг). В основном он депонируется в печени. Из
организма ежедневно выводится с экскрементами около 2-5 мкг. В связи с этим
дефицит витамина при значительном снижении его поступления и (или) усвоения
развивается лишь через 3 - 6 лет. Недостаток витамина В12 в
результате нарушения и (или) снижения его всасывания может быть следствием
уменьшения или прекращения синтеза внутреннего фактора Кастла; нарушения
всасывания комплекса "витамин В12 + гликопротеин" в
подвздошной кишке; повышенного расходования витамина; "конкурентного"
использования витамина В12 в кишечнике паразитами или
микроорганизмами.
3.2.1 Этиология
Мегалобластные анемии возникают при недостаточном поступлении в организм
витаминов В12 и/или фолиевой кислоты. Дефицит этих витаминов приводит к
нарушению в клетках синтеза ДНК и РНК, что вызывает нарушения созревания и
насыщения гемоглобином эритроцитов. В костном мозге появляются крупные клетки -
мегалобласты, а в периферической крови - крупные эритроциты (мегалоциты и
макроциты). Процесс кроворазрушения преобладает над кроветворением.
Неполноценные эритроциты менее устойчивы, чем нормальные, и гибнут быстрее.
.2.2 Патогенез
Недостаток в организме витамина В12 любого происхождения
обусловливает нарушение синтеза нуклеиновых кислот в эритрокариоцитах, а также
обмена жирных кислот в них и клетках других тканей. Витамин В12
имеет две коферментные формы: метилкобаламин и 5 - дезоксиаденозилкобаламин.
Метилкобаламин участвует в обеспечении нормального, эритробластического,
кроветворения. Тетрагидрофолиевая кислота, образующаяся при участии
метилкобаламина, необходима для синтеза 5, 10 - метилтетрагидрофолиевой кислоты
(коферментная форма фолиевой кислоты), участвующей в образовании
тимидинфосфата. Последний включается в ДНК эритрокариоцитов и других интенсивно
делящихся клеток. Недостаток тимидинфосфата, сочетающийся с нарушением
включения в ДНК уридина и оротовой кислоты, обусловливает нарушение синтеза и
структуры ДНК, что ведет к расстройству процессов деления и созревания
эритроцитов. Они увеличиваются в размерах (мегалобласты и мегалоциты), в связи
с чем напоминают эритрокариоциты и мегалоциты у эмбриона. Однако это сходство
только внешнее. Эритроциты эмбриона полноценно обеспечивают
кислородтранспортную функцию. Эритроциты же, образующиеся в условиях дефицита
витамина В12 , являются результатом патологического
мегалобластического эритропоэза. Они характеризуются малой митотической активностью
и низкой резистентностью, короткой продолжительностью жизни. Большая часть их
(до 50 %, в норме около 20 %) разрушается в костном мозге. В связи с этим
существенно снижается число эритроцитов и в периферической крови.
.2.3 Клиника
В12-дефицитная анемия развивается относительно медленно и может быть
малосимптомной. Клинические признаки анемии неспецифичны: слабость, быстрая
утомляемость, одышка, головокружение, сердцебиение. Больные бледны,
субиктеричны. Есть признаки глоссита - с участками воспаления и атрофии
сосочков, лакированный язык, может быть увеличение селезенки и печени.
Желудочная секреция резко снижения. При фиброгастроскопии выявляется атрофия
слизистой оболочки желудка, которая подтверждается и гистологически.
Наблюдаются и симптомы поражения нервной системы (фуникулярный миелоз), которые
не всегда коррелируют с вырженностью анемии. В основне неврологических
проявлений лежит демиелинизация нервных волокон. Отмечается дистальные
парестезии, периферическая полиневропатия, расстройства чувствительности,
повышение сухожильных рефлексов.
Таким образом, для В12-дефицитной анемии характерна триада:
поражение крови;
поражение ЖКТ;
поражение нервной системы.
В
костном мозге обнаруживают в большем или меньшем количестве мегалобласты
диаметром более (15 мкм), а также мегалокариоциты. Мегалобласты характеризуются
десинхронизацией созревания ядра и цитоплазмы. Быстрое образование гемоглобина
(уже в мегалобластах) сочетается с замедленной дифференциацией ядра. Указанные
изменения в клетках эритрона сочетаются с нарушением дифференцировки и других
клеток миелоидного ряда: мегакариобласты, миелоциты, метамиелоциты, палочко- и
сегментоядерные лейкоциты также увеличены в размерах, ядра их имеют более
нежную, чем в норме, структуру хроматина. В периферической крови значительно
снижено число эритроцитов, иногда до 0,7 - 0,8 x 1012
/л. Они большого размера - до 10 - 12 мкм, часто овальной формы, без
центрального просветления. Как правило, встречаются мегалобласты. Во многих
эритроцитах обнаруживаются остатки ядерного вещества (тельца Жолли) и
нуклеолеммы (кольца Кебота). Характерны анизоцитоз (преобладают макро- и
мегалоциты), пойкилоцитоз, полихроматофилия, базофильная пунктация цитоплазмы
эритроцитов. Эритроциты избыточно насыщены гемоглобином. Цветовой показатель
обычно более 1,1 - 1,3. Однако общее содержание гемоглобина в крови существенно
снижено в связи со значительным уменьшением числа эритроцитов. Количество
ретикулоцитов обычно понижено, реже - нормальное. Как правило, наблюдаются
лейкопения (за счет нейтрофилов), сочетающаяся с наличием полисегментированных
гигантских нейтрофилов, а также тромбоцитопения. В связи с повышенным гемолизом
эритроцитов (в основном в костном мозге) развивается билирубинемия. В12
- дефицитная анемия обычно сопровождается и другими признаками авитаминоза:
изменениями в желудочно-кишечном тракте связи с нарушением деления (при этом
выявляются признаки атипичного митоза) и созревания клеток (наличие
мегалоцитов), особенно в слизистой оболочке. Наблюдается глоссит, формирование "полированного"
языка (в связи с атрофией его сосочков); стоматит; гастроэнтероколит, что
усугубляет течение анемии в связи с нарушением всасывания витамина В12;
неврологический синдром, развивающимся вследствие изменений в нейронах. Эти
отклонения в основном являются следствием нарушения обмена высших жирных
кислот. Последнее связано с тем, что другая метаболически активная форма
витамина В12 - 5 - дезоксиаденозилкобаламин (помимо метилкобаламина) регулирует
синтез жирных кислот, катализируя образование янтарной кислоты из
метилмалоновой. Дефицит 5 - дезоксиаденозилкобаламина обусловливает нарушение
образования миелина, оказывает прямое повреждающее действие на нейроны
головного и спинного мозга (особенно задних и боковых его столбов), что
проявляется психическими расстройствами (бред, галлюцинации), признаками
фуникулярного миелоза (шаткая походка, парестезии, болевые ощущения, онемение
конечностей и др.).
Данной
разновидности мегалобластических анемий заключается в нарушении образования
соединений, участвующих в биосинтезе ДНК, в частности тимидинфосфата,
уридинфосфата, оротовой кислоты. В результате этого нарушаются структура ДНК и
заключенная в ней информация по синтезу полипептидов, что ведет к трансформации
нормобластического типа эритропоэза в мегалобластический. Проявления указанных
анемий в большинстве своем такие же, как при витамин В12 - дефицитной анемии.
Развитие мегалобластических анемий возможно не только по причине дефицита
витамина В12 и (или) фолиевой кислоты, но также в результате
нарушения синтеза пуриновых или пиримидиновых оснований, необходимых для
синтеза нуклеиновых кислот. Причиной этих анемий обычно является наследуемое
(как правило, рецессивно) нарушение активности ферментов, необходимых для
синтеза фолиевой, оротовой, адениловой, гуаниловой и, возможно, некоторых
других кислот.
.2.4 Диагностика
Диагностика В12-дефицитной анемии:
. Клинический анализ крови
снижение количества эритроцитов
снижение гемоглобина
повышение цветного показателя (выше 1.05)
макроцитоз (относится к группе макроцитарных анемий)
базофильная пунктация эритроцитов, наличие в них телец Жолл и
колец Кебота
появление ортохромных мегалобластов
снижение ретикулоцитов
лейкопения
тромбоцитопения
снижение моноцитов
анэозинфилия
. В окрашенных мазках - типичная картина: наряду с
характерными овальными макроцитами встречаются эритроциты нормального размера,
микроциты и шизоциты - пойкило- и анизоцитоз.
. Уровень билирубина в сыворотке повышен за счет непрямой
фракции
4. Обязательна пункция костного мозга так как такая картина на периферии
может быть при лейкозе, гемолитической анемии, апластических и гипопластических
состояниях (однако, необходимо отметить, что гиперхромия характерна именно для
В12-дефицитной анемии). Костный мозг клеточный, число ядросодержащих
эритроидных элементов увеличено в 2-3 раза противо нормы, однако эритропоэз
неэффективный, о чем свидетельствует снижение числа ретикулоцитов и эритроцитов
на периферии и укорочение их продолжительности жизни (в норме эритроцит живет
120-140 дней). Находят типичные мегалобласты - главный критерий постановки
диагноза В12-дефицитная анемия. Это клетки с "ядерно-цитоплазматической
диссоциацией" (при зрелой гемоглобинизированной цитоплазме нежное,
сетчатого строения ядро с нуклеолами); также обнаруживаются клетки гранулоцитарного
ряда большого размера и гигантские мегакариоциты.
.2.5 Лечение
Комплекс лечебных мероприятии при В12 - дефицитной анемии
следует проводить с учетом этиологии, выраженности анемии и наличия
неврологических нарушений. При лечении следует ориентироваться на следующие
положения:
· непременным условием
лечения В12 - дефицитной анемии при глистной инвазии является
дегельминтизация (для изгнания широкого лентеца назначают фенасал по
определенной схеме или экстракт мужского папоротника).
· при органических заболеваниях
кишечника и поносах следует применять ферментные препараты (панзинорм, фестал,
панкреатин), а также закрепляющие средства (карбонат кальция в сочетании с
дерматолом).
· нормализация кишечной
флоры достигается приемом ферментных препаратов (панзинорм, фестал,
панкреатин), а также подбором диеты, способствующей ликвидации синдромов
гнилостной или бродильной диспепсии.
· сбалансированное питание
с достаточным содержанием витаминов, белка, безусловным запрещением алкоголя -
непременное условие лечения В12 и фолиеводефицитной анемии.
· патогенетическая терапия осуществляется с помощью
парентерального введения витамина В12 (цианкобаламин
<#"516246.files/image002.gif">
Проведя анализ данных учетной формы № 030, определено, что по
заболеваемость распределена следующим образом:
Патология органов дыхания - 98 чел (30,5%)
Заболевания ССС - 54 чел (16,8 %);
ЖКТ - 47 чел (14,6 %);
МВП - 34 чел (10,5%);
патологии развития нервной системы - 20 чел (6,2%);
болезни органов кроветворения - 16 чел (4,9 %);
прочие - 52 чел (16,1%).
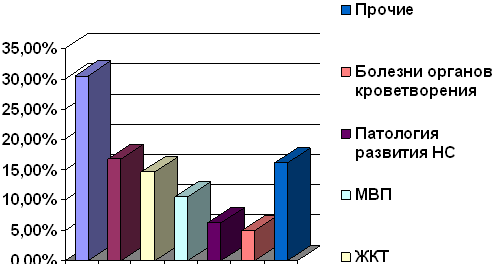
На основании полученных данных определено, что болезни органов
кроветворения занимают 6 место в общей структуре заболеваемости детей.
Далее проводился анализ данных ф № 1124 с целью определения факторов,
влияющих на развитие анемии у детей, по следующим параметрам:
состояние здоровья матерей детей, состоящих на «Д» учете по анемии, по
критериям:
). ЖДА - 9 (33,3%)
). ХУГИ - 7 (25,7%)
) патология ССС - 6 (22,2%)
). патология почек - 5 (18,5%)

Выявлено, что ни одна женщина в период беременности не была абсолютно
здорова. Анемия занимает первое место по количеству встречающихся случаев среди
всех патологией.
Родоразрешение детей в 43,5% (7) случаев произошло оперативным путем.
Все дети в исследуемой группе рождены со II группой здоровья, т.к. имели различную патологию в
интернатальном периоде. Общее количество случаев патологии - 19.
В состоянии асфиксии родилось 7 детей (36,8%); ВУИ - 6 (31,5 %); в/у
гипотрофии - 4 (21%); крупным плодом - 2 (10,6%).
Вывод: внутриутробно и в постнатальном периоде 36,8% детей перенесли
гипоксию, что является одним из факторов развития анемии.
Исследуя влияние длительности грудного вскармливания на частоту
заболеваний на частоту заболеваемости, было выявлено, что ни один ребенок не
имел полноценного грудного вскармливания до 12 месяцев. А это является
подтверждением положительного влияния полноценного грудного вскармливания на
состояние здоровья, профилактику анемии.
Грудное вскармливание 1). до 7 мес - 1 чел (6,25%)
). до 6 мес - 2 чел (12,5%)
). менее 6 мес - 13 чел (81,25%)
Смешанное вскармливание: 1). до 8 мес - 3 чел (18,7%)
). до 7 мес - 3 чел (18,7%)
). до 6 мес. и менее - 10 чел (62,5%)
Искусственное вскармливание: 1). до 8 мес. - 1 чел (6,25%)
). до 6 мес. - 1 чел (6,25%)
). до 4 мес. и менее - 14 чел (87,5%)
Также был проведен анализ структуры заболеваемости детей, состоящих на
учете с анемией, за весь период жизни. Общее количество случаев заболеваемости
- 67. На первом месте число респираторных заболеваний (67,1%)
Респираторные заболевания - 43 (67,1%)
ПЭП - 2 (2,9%)
Гипотрофия - 4 (5,9%)
Аллергозы -3 (4,7%)
Прочие - 15 (22,3%)
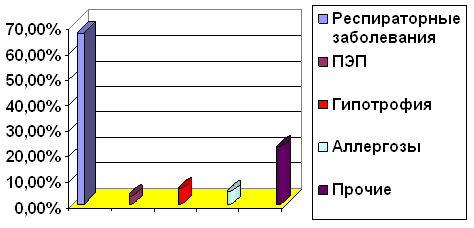
На основе этих данных можно сделать вывод о том, что состояние анемии
является одним из основополагающих факторов, снижающих защитные силы организма
и приводящим к возникновению различных заболеваний.
6. Заключение
Анемия (малокровие) - уменьшение количества эритроцитов и (или) снижение
содержания гемоглобина в единице объема крови. Анемия может быть как
самостоятельным заболеванием, так и синдромом, сопровождающим течение другого
патологического процесса.
Из статистических данных наглядно видно, что число заболеваемости
анемиями у детей младшего и среднего школьного возраста с каждым годом растет.
Это связано с неосведомленностью родителей о правильном рациональном питании
ребенка и позднем обращении их в лечебные учреждения, а также с
неблагоприятными условиями как окружающей, так и социальной среды.
Проведя анализ статистических данных, было определено, что
).болезни органов кроветворения занимают 6 место в общей структуре
заболеваемости детей;
).ни одна женщина в период беременности не была абсолютно здорова.
).анемия занимает первое место по количеству встречающихся случаев среди
всех патологий у беременных;
).исследуя влияние длительности грудного вскармливания на частоту
заболеваний на частоту заболеваемости, было выявлено, что ни один ребенок не
имел полноценного грудного вскармливания до 12 месяцев;
).все дети в исследуемой группе рождены со II группой здоровья, т.к. имели различную патологию в
интернатальном периоде;
). внутриутробно и в постнатальном периоде 36,8% детей перенесли
гипоксию, что является одним из факторов развития анемии.
Также были выделены группы риска, факторы и причины развития данной
патологии:
Группу риска составляют:
все недоношенные дети
дети, рожденные от многоплодной беременности и при отягощенном протекании
второй половины беременности (гестозы, фетоплацентарная недостаточность,
осложнения хронических заболеваний)
дети с дисбактериозами кишечника, пищевой аллергией
дети, которые находятся на искусственном вскармливании
дети, которые растут с опережением общепринятых стандартов физического
развития
дети, рожденные от матерей с анемией
Факторы риска по развитию анемии у детей:
- нарушение маточно-плацентарного кровообращения, плацентарная
недостаточность (токсикозы, угрозы прерывания, перенашивание беременности,
гипоксия, обострение соматических и инфекционных заболеваний);
фетоматеринские и фетоплацентарные кровотечения;
многоплодная беременность;
геморрагический синдром в периоде новорожденности;
гемолитическая болезнь новорожденного
недоношенность
многоплодие;
глубокий и длительный дефицит железа в организме беременной;
преждевременная или поздняя перевязка пуповины;
интранатальные кровотечения;
крупные дети;
дети с аномалиями конституции;
синдром мальабсорбции, хронические заболевания кишечника
Причины возникновения ЖДА у детей:
- недостаточный уровень железа в организме (нарушения маточно-
плацентарного кровообращения, фетоматеринские и фетоплацентарные кровотечения,
синдром фетальной трансфузии при многоплодной беременности, внутриутробная
мелена, недоношенность, многоплодие, глубокий и долговременный дефицит железа в
организме беременной, преждевременная или поздняя перевязка пуповины,
интранатальное кровотечение вследствие травматических акушерских вмешательств
или аномалии развития плаценты и сосудов пуповины)
повышенная потребность в железе (недоношенные, дети с большой массой тела
при рождении, с лимфатическим типом конституции, дети второго полугодия жизни).
недостаточное количество железа в еде (раннее искусственное вскармливание
коровьим или козьим молоком, мучной, молочной или молочно-вегетарианской едой,
несбалансированная диета, в которой нет достаточного содержания молочных
продуктов)
повышенные потери железа вследствие кровотечений различной этиологии,
нарушения кишечного всасывания (хронические заболевания кишечника, синдром
мальабсорбции), а так же значительные и длительные геморрагические маточные
кровотечения у девочек.
нарушения обмена железа в организме (пре и пубертатный гормональный
дисбаланс)
нарушения транспорта и утилизации железа (гипо и атрансферинемия,
энзимопатии, аутоиммунные процессы)
недостаточная резорбция железа в пищеварительном тракте (пострезекционные
и агастральные состояния).
Основная роль в раннем выявлении, наблюдении, лечении, профилактике
анемии у детей отведена первичному звену. Фельдшер участка берет на учет
беременных, проводит дородовые патронажи, дает рекомендации по профилактике
анемии (рациональному питанию, приему пре правильному режиму дня, гимнастике).
Всем детям проводится скриннинг в 5 месяцев, что является одним из факторов
выявления анемии, с ежемесячным контролем развития - проводится исследование
общего анализа крови, при выявлении анемии проводится постановка на «Д» учет.
В обязанности фельдшера, при постановке на учет с диагнозом анемии детей,
входит также организация плана наблюдения:
педиатр до 3 месяцев 2 раза в месяц
общий анализ крови в 1,3,6,12 мес.; в более ранние сроки - по показаниям
исследование сывороточного железа, общей железосвязывающей способности
сыворотки (ОЖСС)
консультации узких специалистов (кардиолог, гастроэнтеролог) по
показаниям
раннее введение прикорма (овощное и фруктовое пюре, мясной фарш,
обогащенные железом каши промышленного производства)
при искусственном вскармливании - адаптированные смеси, содержащие железо
назначение ферротерапии после подтверждения железодефицита
Дальнейшее ведение детей с анемией проводится фельдшером участка в
соответствии с Протоколом.
Протокол ведения детей с анемией
Железодефицитная анемия у детей пубертатного возраста (ювенильный
хлороз). Дефицит железа в период быстрого роста является следствием
некомпенсированного в первые годы жизни сниженного запаса железа.
Скачкообразное увеличение расходов железа быстрорастущим организмом, появление
менструальных кровопотерь формируют относительный дефицит. Поэтому в
пубертатный период желательно использовать диетопрофилактику дефицита железа, а
при появлении признаков гипосидероза - назначать препараты железа.
Железодефицитная анемия у женщин в период беременности и лактации. С
целью профилактики анемии в этой группе пациентов часто используются
комбинированные препараты с относительно невысоким содержанием железа (30-50
мг), включающие витамины, в том числе фолиевую кислоту и витамин В12.
ХАРАКТЕРИСТИКА ТРЕБОВАНИЙ
1. Модель пациента
Нозологическая форма: железодефицитная анемия
Стадия: любая
Фаза: любая
Осложнение: вне зависимости от осложнений
Код по МКБ-10: D50.0
Критерии и признаки, определяющие модель пациента
Обязательно сочетание всех признаков:
• снижение уровня гемоглобина ниже 120 г/л;
• снижение уровня эритроцитов ниже 4,2 x 1012/л;
• гипохромия эритроцитов;
• снижение одного из показателей насыщения эритроцитов гемоглобином
(цветовой показатель (ЦП) ниже 0,85, среднее корпускулярное содержание
гемоглобина (MCH) ниже 24 пг, средняя концентрация гемоглобина в эритроцитах
(МСНС) ниже 30-38 г/дцл);
• снижение уровня сывороточного железа ниже 13 мкмоль/л у мужчин и ниже
12 мкмоль/л у женщин.
2. Порядок включения пациента в протокол
Пациент включается в протокол в том случае, если состояние больного
(анамнез, клинические и лабораторные данные) удовлетворяет критериям и
признакам, определяющим модель пациента.
3. Требования к диагностике амбулаторно-поликлинической
Код Наименование Кратность выполнения
.05.001 Сбор анамнеза и жалоб при болезнях органов кроветворения и крови
1
.05.002 Визуальное исследование при болезнях органов кроветворения и
крови 1
.05.003 Пальпация при болезнях органов кроветворения и крови 1
.05.004 Перкуссия при болезнях органов кроветворения и крови 1
.31.012 Аускультация общетерапевтическая 1
.05.003 Исследование уровня эритроцитов в крови 1
.05.004 Исследование уровня лейкоцитов в крови 1
.05.005 Исследование уровня тромбоцитов в крови 1
.05.006 Соотношение лейкоцитов в крови (формула крови) 1
.05.007 Просмотр мазка крови для анализа аномалий морфологии эритроцитов,
тромбоцитов и лейкоцитов 1
.05.008 Исследование уровня ретикулоцитов в крови 1
.05.009 Определение цветового показателя 1
.05.003 Исследование уровня общего гемоглобина в крови 1
.05.007 Исследование уровня железа сыворотки крови 1
.12.009 Взятие крови из периферической вены 1
.05.001 Взятие крови из пальца 1
.05.010 Определение среднего содержания и средней концентрации
гемоглобина в эритроцитах (по потребности)
.05.001 Цитологическое исследование мазка костного мозга (подсчет формулы
костного мозга) (по потребности)
.05.002 Гистологическое исследование препаратов костного мозга (по
потребности)
.05.002 Оценка гематокрита (по потребности)
.05.008 Исследование уровня трансферрина сыворотки крови (по потребности)
.05.077 Исследование уровня ферритина в крови (по потребности)
.05.003 Получение цитологического препарата костного мозга путем пункции
(по потребности)
.05.004 Получение гистологического препарата костного мозга (по
потребности)
.05.031 Определение сидеробластов и сидероцитов (по потребности)
.05.002 Исследование осмотической резистентности эритроцитов (по
потребности)
.05.003 Исследование кислотной резистентности эритроцитов (по
потребности)
.05.011 Исследование железосвязывающей способности сыворотки (по
потребности)
.05.020 Десфераловый тест (по потребности)
.05.001 Определение объема кровопотери через желудочно-кишечный тракт с
помощью радиоактивного хрома (по потребности)
4. Характеристика алгоритмов и особенностей выполнения
немедикаментозной помощи
Диагностика при железодефицитной анемии:
-й этап - определение (подтверждение) железодефицитного характера анемии;
-й этап - определение причины дефицита железа.
Определение железодефицитного характера анемии
Сбор анамнеза и жалоб при болезнях органов кроветворения и крови
Объективное исследование при болезнях органов кроветворения и крови -
направлено на выявление у больного признаков, характеризующих гипосидероз, и
определение заболеваний (состояний) с повышенным расходом железа.
Исследование уровня эритроцитов, лейкоцитов, тромбоцитов, ретикулоцитов
цветового показателя. Соотношение лейкоцитов в крови (формула крови).
Исследование уровня общего гемоглобина.
Результаты всех исследований анализируются врачом в совокупности, ни один
признак в отдельности не является специфичным для дефицита железа.
Просмотр мазка крови для анализа аномалий морфологии эритроцитов,
тромбоцитов и лейкоцитов. Наиболее точным методом определения содержания
гемоглобина в эритроцитах остается морфологическое исследование эритроцитов.
При железодефицитной анемии выявляется отчетливая гипохромия.
Исследование уровня железа сыворотки - является обязательным
диагностическим тестом для постановки диагноза железодефицитной анемии.
Определение среднего содержания гемоглобина в эритроцитах
Методика, применяемая в автоматических анализаторах.
Исследование уровня трансферрина, ферритина сыворотки
Определение причины дефицита железа
-й этап - определение причины дефицита железа выполняется в соответствии
с требованиями, предусмотренными иными протоколами ведения больных (язва
желудка, лейомиома матки и др.).
5. Требования к лечению амбулаторно-поликлиническому
Код/ Наименование/Кратность выполнения
.05.001 Сбор анамнеза и жалоб при болезнях органов кроветворения и крови
/2
.05.002 Визуальное исследование при болезнях органов кроветворения и
крови/2
.05.008 Исследование уровня ретикулоцитов в крови /1
.05.009 Определение цветового показателя/2
.05.003 Исследование уровня общего гемоглобина в крови/2
.05.001 Взятие крови из пальца/2
.05.003 Пальпация при болезнях органов кроветворения и крови /По
потребности
.05.004 Перкуссия при болезнях органов кроветворения и крови /По
потребности
.31.012 Аускультация общетерапевтическая /По потребности
.05.010 Определение среднего содержания гемоглобина в эритроцитах/ По
потребности
.05.002 Оценка гематокрита /По потребности
.05.007 Исследование уровня железа сыворотки крови /По потребности
.05.077 Исследование уровня ферритина в крови /По потребности
.05.008 Исследование уровня трансферрина сыворотки крови /По потребности
.12.009 Взятие крови из периферической вены /По потребности
.05.011 Исследование железосвязывающей способности сыворотки /По
потребности
6. Характеристика алгоритмов и особенностей выполнения
немедикаментозной помощи
Сбор анамнеза и жалоб при болезнях органов кроветворения и крови,
физикальное обследование
Сбор жалоб и физикальное обследование проводятся двухкратно для оценки
динамики в общем состоянии (самочувствии) пациентов. «Малые признаки»
эффективности очень важны с точки зрения ранней оценки эффективности терапии.
Исследование уровня ретикулоцитов крови
Исследование уровня эритроцитов крови, общего гемоглобина
Повышение уровня гемоглобина, числа эритроцитов отмечается обычно на 3-й
неделе терапии, позже исчезают гипохромия и микроцитоз. К 21-22 дню лечения
обычно нормализуется гемоглобин (при адекватных дозах), однако насыщение депо
не происходит.
Проверить насыщение депо можно только с помощью комплексного
биохимического исследования. Таким образом, контроль эффективности терапии
является обязательным компонентом рационального применения железосодержащих
препаратов.
7. Требования к лекарственной помощи
Наименование группы Кратность (продолжительность) лечения
Противоанемические средства Согласно алгоритму
8. Характеристика алгоритмов и особенностей применения
медикаментов
Заместительная терапия дефицита железа проводится препаратами железа. В
настоящее время используются две группы препаратов железа - содержащие
двухвалентное и трехвалентное железо, в подавляющем большинстве случаев
применяемые внутрь.
Некоторые препараты выпускаются в виде сиропов и суспензий, что облегчает
их назначение детям. Однако и здесь пересчет суточной дозы должен производиться
с учетом содержания железа в единице объема.
Препараты железа назначаются на протяжении 3-х недель, после получения
эффекта, доза препарата снижается в 2 раза и назначается еще на 3 недели.
Терапия железодефицитной анемии у детей
Необходимо, чтобы ребенок получал не менее 6 мг железа в сутки
(нормальная суточная потребность), при наличии дефицита нужно увеличивать это
количество в 5-10 раз.
Для восполнения дефицита железа можно использовать специальные молочные
смеси, обогащенные железом, но обязательно добавлять железосодержащие сиропы
или растворы, рассчитав предварительно необходимый объем. Кроме того, мать,
имеющая доказанный дефицит железа даже в отсутствие анемии, должна получать
препараты железа как во время беременности, так и во время лактации, что будет
являться в первом случае фактором профилактики дефицита железа у
новорожденного, во втором - дополнительным фактором терапии.
дети кроветворение анемия диагностика лечение
Список литературы
1. Анемии у
детей: диагностика и лечение. Практическое пособие для врачей /Под ред. А.Г.
Румянцева, Ю.Н. Токарева. М: МАКС-Пресс, 2007.
2. Волкова
С. Анемия и другие болезни крови. Профилактика и методы лечения. Изд.:
Центрполиграф. 2005 - 162 с.
3. Гогин
Е. Протокол ведения больных. «Железодефицитная анемия». Изд.: Ньюдиамед. 2005
г. - 76 с.
. Иванов
В. Железодефицитная анемия беременных. Учебное пособие. Изд. Н-Л. 2008 г. - 16
с.
. Казюкова
Т.В. Калашникова Г.В., Фаллух А. и др. Новые возможности ферро-терапии
железодефицитных анемий// Клиническая фармакология и терапия. 2006. № 9 (2). С.
88-92.
. Калиничева
В.Н. Анемии у детей. М.: Медицина, 2003.
. Калманова
В.П. Показатели эритропоэтической активности и обмена железа при гемолитической
болезни плода и новорожденного и внутриутробных трансфузиях эритроцитов: Дис...
канд. мед. наук. М., 2005.
. Коровина
Н.А., Заплатников А.Л., Захарова И.Н. Железодефицитные анемии у детей. М.,
2009.
. Мирошникова
К. Анемия. Лечение народными средствами. Изд.: ФЕИКС. 2007 г. - 256 с.
10. Михайлова
Г. Болезни детей от 7 до 17 лет. Гастрит, анемия, грипп, аппендицит,
вегетососудистая дистония, невроз и др. Изд.: ВЕСЬ. 2005 г. - 128 с.
11. Эллард
К. Анемия. Причины и лечение. Изд.: Норинт. 2002 г. - 64 с.
Приложения
Приложение 1. Диета при анемии
Первым лечебным мероприятием при алиментарной анемии у ребенка является
правильная организация питания в соответствии с возрастом ребенка. Пища должна
быть богата белком животного происхождения, солями железа, меди, магния,
кобальта, цинка, витаминами, прежде всего фолиевой кислотой и В12.
Если ребенок находится на искусственном вскармливании, показано
применение лечебных смесей - «Энпитов». Лечебные (диетические) молочные смеси
представлены выпускаемыми отечественной промышленностью сухими диетическими
молочными продуктами энпитами ("Энпит белковый", "Энпит
жировой", "Энпит обезжиренный" и "Энпит
противоанемический"), низколактозной молочной смесью "Малютка" и
низколактозным молоком. Эти продукты характеризуются оптимальным содержанием
полноценных легкоусвояемых белков, обогащены незаменимыми жирными кислотами,
витаминами, препаратами железа. Вырабатываются диетические молочные продукты с
использованием препарата сухого растворимого молочного белка - казецита, а также
сливок, сахара, рафинированного растительного масла с добавлением широкого
комплекса витаминов - A, D2, С, Е, В1, В2, В6, РР и других, цитратов натрия и
калия, солей железа. "Энпит белковый" содержит 47, 2% белка,
"Энпит жировой" - 39% жира. Особенностью "Энпита
противоанемического" является высокое содержание железа (146 мг/100 г
продукта).
Если ребенок находится на исключительно грудном вскармливании - показано
более раннее введение прикорма. Необходимы овощные пюре и каши. Особенно богаты
железом белокочанная и цветная капуста, морковь, редис, редька, свекла, томаты,
зеленый горошек. В редисе, свекле, а также в картофеле, баклажанах содержится
значительное количество меди. Детям после года рекомендуется готовить овощные
салаты из сырых овощей, поскольку при термической обработке значительная часть
минеральных солей и витаминов разрушается. В этом возрасте обязательно давайте
детям зелень (петрушку, укроп, шпинат), в которой минеральных солей еще больше,
чем в овощах. Среди каш отдавайте предпочтение овсяной и гречневой - они
превосходят все остальные по содержанию железа и меди.
Также грудничкам с анемией уже с пяти месяцев нужно ввести в рацион мясо,
поскольку животный белок необходим для образования гемоглобина. Следует
использовать нежирное мясо кур, цыплят, индеек, телятину, говядину. Мясо птицы
обладает высокой пищевой ценностью: в составе его белка имеются все незаменимые
аминокислоты, а жир богат полиненасыщенными жирными кислотами, которые по
биологической ценности можно сравнить с витаминами.
Особенно полезна при анемии говяжья и телячья печень. Но для детей
первого года жизни ее необходимо дважды пропустить через мясорубку с мелкой
решеткой или протереть через сито.
Высокую пищевую ценность для страдающего малокровием ребенка имеет желток
куриного яйца. Он содержит полноценные высокоусвояемые белки, а также
значительное количество железа, меди, кобальта, марганца.
Продукты, содержащие железо:
Продукт/ Размер порции/ Кол-во железа(mg)
говяжая печень 85гр 7.5
печень цыпленка 3 небольшие шт. 7.4
отруби 1/2 стакана 6.2
пшенная каша 1/2 стакана 6.0
моллюски 85гр 5.2
устрицы (сырые) 85гр 4.8
курага 85 гр 4.0
свиная отбивная 85гр 3.3
бифштекс (из постного мяса) 85гр 3.0
печеные бобы 1/2 стакана 3.0
Примерный рацион ребенка 7 месяцев, больного анемией
ч
Молоко грудное
(детская смесь - 200 мл, сок фруктовый - 30 мл.
ч
Каша гречневая 10%-ная - 150 г (с 4 г сливочного масла),
творог - 40 г,
пюре фруктовое - 30 г.
ч
Молоко грудное (детская смесь) ,- 200 мл, пюре фруктовое - 30 г.
ч
Суп овощной на мясном бульоне (20 мл) с сухариком,
пюре овощное - 150 г (с 1/2 яичного желтка и 1 чайной ложкой
растительного масла),
пюре мясное - 40 г,
сок фруктовый - 30 мл.
ч
Молоко грудное
(детская смесь) - 200 мл.
Приложение 2. Фитотерапия при анемии
При железодефицитной анемии можно рекомендовать больным некоторые
лекарственные травы. В растениях биологически активные вещества находятся в
оптимальном соотношении. Целесообразно использование крапивы двудомной (рисунок
1) , череды трехраздельной (рисунок 2). Настой плодов шиповника и земляники
лесной (плодов и листьев) по ¼ - 1/2 стакана З раза в день. Отвар
листьев земляники лесной принимают по 1 стакану в день. Они богаты железом,
медью, марганцем, кобальтом, аскорбиновой кислотой, рибофлавином, органическими
кислотами, что обеспечивает их гемостимулирующее действие. для приготовления
настоя 1 ст. л. сбора из указанных трав и плодов (предварительно измельченных)
заливают стаканом кипятка, настаивают в течение 2 - З часов, процеживают. Плоды
абрикоса следует употреблять по нескольку штук в день, сок - З раза в день.
Хорошо применять настой листьев медуницы лекарственной (рисунок 3), шпината
огородного, одуванчика. Лекарственные растения широко используются для
остановки кровотечений.
При мено- и метроррагиях назначают настои крапивы двудомной по 1/2
стакана 2 раза в день; настой пастушьей сумки по 1/2 стакана З раза в день;
отвар корневищ кровохлебки по 1 ст. л. З - 4раза в день. При атонических
маточных кровотечениях применяют настойку из листьев барбариса амурского по 25
- 30 капель З раза в день в течение 2 - З недель. Настой водяного перца
назначают при маточных и геморроидальных кровотечениях по 1 ст. л. 2 - 4раза в
день. С кровоостанавливающей целью рекомендуется также хвощ полевой. Отвар
принимают по 1 ст. л. З - 4раза в день. Стальник пашенный в виде настойки из
корней или отвара у больных геморроем облегчает стул, останавливает
кровотечение и уменьшает отек. Настойку стальника назначают внутрь по 40 - 50
капель на прием З раза в день в течение 2 - З недель. Отвар стальника принимают
по 2 - З ст. л. З раза в день перед едой в течение 2 - 4 недель.
В качестве вспомогательных средств и для проведения поддерживающей
терапии при анемиях рекомендуют богатые аскорбиновой кислотой ягоды черной
смородины, рябины обыкновенной, шиповника, земляники. Из ягод и листьев этих
растений готовят витаминный чай.
Чай витаминный:
плоды рябины - 25 г;
плоды шиповника - 25 г.
Принимают по одному стакану в день.
Настой:
плоды шиповника - 25 г;
ягоды черной смородины - 25 г.
Принимают по 1/2 стакана 3 - 4раза в день.

Рисунок 2. Крапива двудомная

Рисунок 3. Череда трехраздельная

Рисунок 4. Медуница лекарственная
Приложение 3. Характеристика наиболее употребляемых препаратов
железа
Мальтофер Фол.
Жевательные таблетки со вкусом шоколада. 100 мг железа в каждой таблетке.
Лечение клинически выраженного дефицита железа: 1-2 таблетки в день до
достижения нормального уровня гемоглобина в крови, затем по 1 таблетке в день в
течение 4 недель.
Лечение и профилактика латентного дефицита железа: 1 таблетка в день в
течение 4 недель.
Ферроцитон.
Натриевая соль орто-карбоксибензоилферроцена.
Кристаллический темно-оранжевый порошок без запаха, горький на вкус.
Таблетки темно-оранжевого цвета по 0,3 г и таблетки, покрытые оболочкой
розового цвета, по 0,1 г в упаковке по 30, 60 и 100 штук.
Лечение гипохромных ЖДА различного происхождения. Легко всасывается
слизистой оболочкой ЖКТ. Стимулирует процессы кроветворения.
Назначают внутрь в виде таблеток взрослым по 0,3 г 3 раза в день после еды.
Детям до 2 лет назначают по 0,1 г 1-2 раза в день, 2-4 лет - по 0,1 г 2 раза в
день, 4-6 лет - по 0,1 г 3 раза в день, 6-14 лет - по 0,2 г 3 раза в день курс
лечения 30 дней.
Феррамид.
Дихлородикотинамид железа. Комплексное соединение железа с никотинамодом.
Мелкокристаллический порошок бледно-желтого цвета, металлического вкуса.
Таблетки светло-желтого по 0,1 в стеклянных банках по 100 шт.
Лечение постгеморрагической анемии и ЖДА анемиях различного
происхождения.
Назначают внутрь (после еды) взрослым по 0,1 г 3 раза в день. Курс
лечения 3-4 недели.
Ферроплекс.
Драже белого и цвета, содержащие по 50 мг сульфата железа II и 30 мг аскорбиновой кислоты.
Лечение ЖДА различного генеза: гипохромная анемия; хронический гастрит;
хронические кровотечения; язвенная болезнь желудка и двенадцатиперстной кишки.
Профилактика ЖДА у беременных женщин, гипохромной анемии и снижения
сопротивляемости к инфекциям у недонощенных детей; ЖДА у новорожденных.
Детям 4-12 лет- по 1-2 драже 3 раза в сутки, новорожденным - по 1 драже 3
раза в сутки.
Сорбифер.
Таблетки, покрытые оболочкой, содержащие по 320 мг сульфата железа (100
мг двухвалентного железа) и 60 мг аскорбиновой кислоты.
Лечение ЖДА алиментарного происхождения, повышение физиологической
потребности в железе, хронической кровопотери.
Профилактика ЖДА у беременных женщин, в послеродовом периоде и лактации.
Взрослым и подросткам старше 12 лет по 1 таблетке 2 раза в день. После
нормализации показателей гемоглобина крови лечение должно проводиться еще
примерно 2 месяца до полного насыщения депо железа в организме. В среднем
продолжительность курса лечения составляет 3-6 месяцев.
Приложение 4. Диета беременных
Для того чтобы кровь была здоровой, организму необходимо получать много
различных витаминов и минералов. При беременности потребность в них возрастает,
ведь в это время мама является единственным источником питательных веществ для
ребенка, да и свои потребности ей тоже нужно удовлетворять: в материнском
организме увеличивается объем циркулирующей крови, а значит - эритроцитов и
гемоглобина. Непременное условие профилактики анемии - это полноценное
РАЗНООБРАЗНОЕ питание, поскольку к анемии может привести дефицит железа,
белков, витаминов группы В, фолиевой кислоты, аскорбиновой кислоты, меди,
кобальта и т.д.
Необходимое количество минеральных веществ для беременных
женщин в сутки:
Кальций - 1500-2000 мг
Магний - 300-500 мг
Фосфор - 1-1,5 г
Калий - 3-5 г
Медь - 4-6 г
Железо - 18 мг
Самой частой причиной анемии у беременных является дефицит железа.
Железо, получаемое с пищей, принято делить на два вида (в зависимости от типа
соединения, в которое оно входит): неорганическое, содержащееся в продуктах
растительного происхождения, и гемовое, содержащееся в животных продуктах.
Гемовое железо усваивается значительно лучше неорганического. Поэтому для
профилактики железодефицитной анемии нужно ежедневно есть мясо (говядину,
свинину) либо такие продукты, как птица, рыба или печень. Железо содержится
также в крупах (например в гречке), фруктах, овощах, ягодах, но из продуктов
растительного происхождения усваивается только 5-7% железа.
В первой половине беременности наиболее физиологично 4-разовое питание.
Первый завтрак должен содержать около 30 % энергоценности суточного рациона,
второй завтрак - 15%, обед - 40%, ужин - 10%, в 21 час стакан кефира - 5%.
Во второй половине беременности рекомендуется 5-6-разовое питание.
Женщина должна получать в сутки:
хлеба пшеничного - 100-150 г, ржаного - 150-200 г,
мяса или рыбы - 200 г,
масла сливочного - 40 г,
масла растительного - 30 г,
1 яйцо, молока - 500 г,
творога - 150 г,
кефира - 200 г,
сметаны - 30 г,
мучных изделий - 100 г, макаронных изделий - 60 г ,
крупы - 50 г,
картофеля - 400 г,
капусты - 100 г,
лука репчатого - 35 г,
моркови - 100 г,
томатов - 200 г,
чай, какао (от кофе и острых приправ следует отказаться),
Из этих же продуктов можно предложить меню беременной, в котором
предусмотрен 4-разовый прием пищи:
первый завтрак в 7-8 ч утра,
второй завтрак в 11-12 ч,
обед в 14-15 ч,
ужин в 18-19 ч.
Это расписание приема пищи может меняться в зависимости от распорядка
беременной, ее занятий и т.д. Следует распределить продукты таким образом,
чтобы мясо, рыба, крупа, крупы входили в завтрак и обед. На ужин рекомендуется
преимущественно молочно-растительная пища. Последний прием должен производиться
за 2-3 часа до сна.
Помимо железосодержащих продуктов, для удовлетворения потребности в
железе необходимы вещества, помогающие организму усваивать этот элемент. Лучший
«друг» железа - витамин С (также помогает в усвоении фолиевой кислоты). Для
адекватного усвоения железа ежедневно необходимо 75 мг витамина С. Такое
количество этого витамина содержатся в чайной чашке одного из следующих
продуктов: капуста брокколи, брюссельская, цветная капуста, клюквенный,
апельсиновый, грейпфрутовый или ананасный сок, папайя (кусочки), свежая
клубника.
Нередко причиной анемии оказывается дефицит витамина В12. Для
профилактики В12-дефицитной анемии необходимо включать в рацион продукты
животного происхождения: молочные продукты, яйца, мясо.
Фолиевая кислота также нужна для построения гемоглобина. Она содержится
главным образом в свежих фруктах и овощах, которые обязательно должны
присутствовать в ежедневном рационе беременной женщины.