Ациклические непредельные углеводороды (алкены)
«Уфимский Государственный Нефтяной Технический Университет»
Кафедра: «Физическая и органическая химия»
Реферат
Ациклические
непредельные углеводороды
(алкены)
Ст.гр.БТП-09-01
Антипин А.
Доцент
Калашников С.М.
Уфа 2010
Содержание
1.
Алкены
2.
Цис-транс-изомерия в ряду алкенов
3.
Получение алкенов
4.
Физические свойства алкенов
5.
Химические свойства алкенов
6.
Применение алкенов
7.
Номенклатура
1. Алкены
АЛКЕНЫ (ОЛЕФИНЫ)
(от лат. oleum-масло) (этиленовые углеводороды), ненасыщенные ациклические углеводороды, содержащие одну двойную связь С=С; общая формула СnН2n. Атомы углерода при двойной связи имеют sp2-гибридизацию и образуют s-
и p-связи. Последняя состоит из двух базисных орбиталей-связывающей и
разрыхляющей, образующихся за счет р-орбиталей атомов С. Энергия
связи ~615 кДж/моль. Простейший
олефин - этилен, валентные углы которого практически равны 120°. Для олефинов,
начиная с С4Н8, наряду с изомерией углеродного скелета и разл. положения двойной связи, возможна геометрическая (цис-, транс-) изомерия, обусловленная большим барьером вращения вокруг двойной связи.
2. Цис-транс-изомерия в ряду алкенов
“Наряду с изомерией,
связанной со строением углеродного скелета и положением двойной связи, в ряду
алкенов имеет место геометрическая или цис-транс-изомерия. Ее существование
обусловлено отсутствием свободного вращения атомов, связанных двойной связью.
|
CH3
\
|
|
CH3
/
|
|
CH3
\
|
|
H
/
|
|
C=C
|
|
|
|
C=C
|
|
|
/
H
|
|
\
H
|
|
/
H
|
|
\
CH3
|
цис-изомер транс-изомер
Метильные группы в
приведенных примерах могут располагаться как по одну сторону двойной связи
(такой изомер называется цис-изомером), так и по разные стороны (такой изомер
называется транс-изомером). Названия упомянутых изомеров происходят от
латинского cis - на этой стороне и trans- через, на другой стороне. Превращение
изомеров друг в друга невозможно без разрыва двойной связи”.
3. Получение алкенов
1) Основным
промышленным источником получения первых четырех членов ряда алкенов (этилена,
пропилена, бутиленов и пентиленов ) являются газы крекинга и пиролиза
нефтепродуктов, а также газы коксования угля (этилен, пропилен). Газы крекинга
и пиролиза нефтепродуктов содержат от 15 до 30% олефинов. Так, крекинг бутана
при 600С приводит к смеси водорода, метана, этана и олефинов – этилена,
пропилена, псевдобутилена (бутена -2) с соотношением олефинов ≈ 3,5 : 5 :
1,5 соответственно.
2) Все более
значительные количества алкенов получают дегидрогенизацией алканов при
повышенной температуре с катализатором.
|
CH3–CH2–CH2–CH3 ––300C,Cr2O3–
|
|
|
|
CH2=CH–CH2–CH3(бутен-1) + H2
CH3–CH=CH–CH3(бутен-2) + H2
|
3) В лабораторной
практике наиболее распространенным способом получения алкенов является
дегидратация (отщепление воды) спиртов при нагревании с водоотнимающими
средствами (концентрированная серная или фосфорная кислоты) или при пропускании
паров спирта над катализатором (окись алюминия).
CH3–CH2–OH(этанол)
––t,Al2O3
CH2=CH2 + H2O
Порядок дегидратации вторичных и третичных спиртов
определяется правилом А.М.Зайцева: при образовании воды атом водорода
отщепляется от наименее гидрогенизированного соседнего атома углерода, т.е. с
наименьшим количеством водородных атомов.
|
CH3–
|
CH–C
I I
|
H–CH3(бутанол-2) CH3–CH=CH–CH3(бутен-2) +
H2O
|
|
OH H
|
|
4) Часто алкены
получают реакцией дегидрогалогенирования (отщепление галогеноводорода) из
галогенопроизводных при действии спиртового раствора щелочи. Направление данной
реакции также соответствует правилу Зайцева.
|
CH3–CH–CH2–CH3(2-бромбутан) + NaOH(спирт p-p)
CH3–CH=CH–CH3 + NaBr + H2O
I
Br
|
5) Реакция
дегалогенирования (отщепление двух атомов галогена от соседних атомов углерода)
при нагревании дигалогенидов с активными металлами также приводит к алкенам.
|
CH2–CH –CH3(1,2-дибромпропан)
+ Mg
CH2=CH–CH3(пропен) + MgBr2
I I
Br Br
|
4.
Физические свойства алкенов
5.
Химические свойства алкенов
Углеродные атомы в молекуле этилена
находятся в состоянии sp2- гибридизации, т.е. в гибридизации
участвуют одна s- и две p -орбитали.
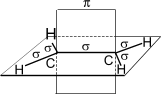
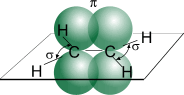
Схематическое изображение строения
молекулы этилена
В результате каждый
атом углерода обладает тремя гибридными sp2 -орбиталями, оси которых
находятся в одной плоскости под углом 120º друг к другу, и одной
негибридной гантелеобразной p-орбиталью, ось которой расположена под прямым
углом к плоскости осей трех sp2 -орбиталей. Одна из трех гибридных
орбиталей атома углерода перекрывается с подобной орбиталью другого атома
углерода, образуя - связь. Каждая оставшаяся гибридная орбиталь атомов
углерода перекрывается с s- орбиталью атомов водорода, приводя к образованию в
той же плоскости четырех - связей C–H. Две негибридные p- орбитали
атомов углерода взаимно перекрываются и образуют - связь, максимальная
плотность которой расположена перпендикулярно плоскости - связей.
Следовательно, двойная связь алкенов представляет собой сочетание - и -
связей.
- Связь менее
прочна, чем - связь, так как p- орбитали с параллельными осями
перекрываются значительно меньше, чем при образовании теми же p- орбиталями и
s- орбиталями - связи (перекрывание осуществляется по оси орбиталей). В
связи с этим, - связь легко разрывается и переходит в две новые -
связи посредством присоединения по месту двойной связи двух атомов или групп
атомов реагирующих веществ.
Иными словами, для
алкенов наиболее типичными являются реакции присоединения.
В реакциях
присоединения двойная связь выступает как донор электронов, поэтому для алкенов
характерны реакции электрофильного присоединения.
1) Галогенирование.
Алкены при обычных условиях присоединяют галогены, приводя к
дигалогенопроизводным алканов, содержащим атомы галогена у соседних углеродных
атомов.
H2C=CH2 + Br2
BrCH2–CH2Br(1,2-дибромэтан)
Приведенная реакция -
обесцвечивание алкеном бромной воды является качественной реакцией на двойную
связь.
2) Гидрирование.
Алкены легко присоединяют водород в присутствии катализаторов (Pt, Pd, Ni),
образуя предельные углеводороды.
CH3–CH=CH2 +
H2 ––Ni
CH3–CH2–CH3(пропан)
3) Гидрогалогенирование.
Этилен и его гомологи присоединяют галогеноводороды, приводя к
галогенопроизводным углеводородов.
H2C=CH2
+ HBr CH3–CH2Br(бромистый этил)
Присоединение
галогеноводородов к пропилену и другим алкенам происходит в соответствии с
правилом В.В.Марковникова (водород присоединяется к наиболее
гидрогенизированному атому углерода при двойной связи).
CH3−CH=CH2 +
HCl CH3−
|
CH−CH3(2-хлорпропан)
I
Cl
|
4) Гидратация. В
присутствии минеральных кислот олефины присоединяют воду, образуя спирты.
|
|
OH
I
|
|
CH3−
|
C=CH2(2-метилпропен-1)
+ H2O ––H+ CH3−
|
C−CH3(2-метилпропанол-2)
|
|
I
CH3
|
I
CH3
|
5) Сульфатация (O-
сульфирование). Взаимодействие алкенов с серной кислотой приводит к кислым
эфирам серной кислоты.
|
CH2=CH−CH3
+ HO−SO2−OH
CH3−
|
CH−O−SO2−OH(изопропилсерная
кислота)
I
CH3
|
Как видно, направление реакций гидратации и сульфирования
также определяется правилом Марковникова.
6) Окисление.
Алкены легко окисляются. В зависимости от условий проведения реакции образуются
различные продукты.
a) При сжигании на
воздухе олефины дают углекислый газ и воду.
H2C=CH2
+ 3O2 2CO2 + 2H2O
b) При окислении
алкенов разбавленным раствором перманганата калия образуются двухатомные спирты
– гликоли (реакция Е.Е.Вагнера). Реакция протекает на холоде.
|
3H2C=CH2 + 2KMnO4 + 4H2O 3
|
CH2−CH2(этиленгликоль) + 2MnO2 + 2KOH
I I
OH OH
|
В результате реакции
наблюдается обесцвечивание раствора перманганата калия. Реакция Вагнера служит
качественной пробой на двойную связь.
c) При жестком
окислении алкенов кипящим раствором перманганата калия в кислой среде
происходит полный разрыв двойной связи и образование кислот или кетонов.
|
O
II
|
O
II
|
|
CH3−CH=CH−CH2−CH3(пентен-2) –[O] CH3−
|
C (уксусная кислота) +
|
C−CH2−CH3(пропионовая кислота)
|
|
I
OH
|
I
OH
|
|
|
|
O
II
|
|
CH3−
|
C=CH−CH3(2-метилбутен-2) –[O] CH3−
|
C=O(пропанон-2) +
|
C−CH3(уксусная кислота)
|
|
I
CH3
|
I
CH3
|
I
OH
|
6.
Применение алкенов
Алкены широко
используются в промышленности в качестве исходных веществ для получения
растворителей (спирты, дихлорэтан, эфиры гликолей и пр.), полимеров (полиэтилен,
поливинилхлорид, полиизобутилен и др.), а также многих других важнейших
продуктов.
Номенклатура
В алкенах с неразветвленной
углеродной цепью нумерацию начинают с того конца, ближе к которому находится
двойная связь. В названии соответствующего алкана окончание -ан заменяется на
-ен. В разветвленных алкенах выбирают главную цепь так, чтобы она содержала
двойную связь, даже если она при этом и не будет самой длинной. Перед названием
главной цепи указывают номер атома углерода, при котором находится заместитель,
и название этого заместителя. Номер после названия главной цепи указывает положение
двойной связи, например:
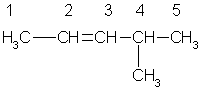
4-метил-2-пентен