Железо в почвах. Методы определения железа
МИНИСТЕРСТВО
ОБРАЗОВАНИЯ И НАУКИ
РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ АГЕТСТВО
ПО ОБРАЗОВАНИЮ
Реферат
Железо в почвах
Методы определения железа
Выполнила:
Проверила:
Содержание
Введение
Глава 1. Железо в почвах
Глава 2. Методы
определения железа в почвах
2.1 Атомно-абсорбционный
метод
2.2
Комплексонометрическое определение железа в почвах
2.2.1 Методика
комплексонометрического определения валового содержания железа в почвах
2.3 Фотометрические
методы определения железа
2.3.1 Методика определения общего содержания железа сульфосалицинатным
методом
2.4 Методика определения подвижных форм железа с помощью
роданида аммония
Список литературы
Введение
Железо — элемент, абсолютно необходимый для жизни растений,
без железа не образуется хлорофилла. В почвах железо встречается в составе
минералов группы ферросиликатов, в виде гидроокислов, окислов, простых солей, а
также ферро- и ферриорганических комплексных солей.
В результате выветривания минералов, содержащих железо,
освобождается гидроокись железа — малоподвижное соединение, выпадающее в виде
аморфного геля Fe2O3*nH2O и, переходящее при кристаллизации в
гетит Fe2O3*Н2O и гидрогетит Fe2O3*ЗН2O. [1]
Только в сильнокислой среде (рН<3) подвижность гидроокиси железа
увеличивается и в почвенном растворе появляются ионы железа (Fe3+).
В восстановительных условиях окисное железо переходит в закисное с образованием
растворимых соединений FeCO3, Fe(HCO3)2, FeSO4, доступных
растениям. Повышенная растворимость соединений железа угнетает растения. На
почвах нейтральных и щелочных с ярко выраженными окислительными условиями
растения могут испытывать недостаток железа, что внешне проявляется как хлороз.
Гидроокись железа, так же как и гидроокись алюминия, может образовывать
с органическими кислотами подвижные формы комплексных соединений, способных
перемещаться по профилю почвы.
Глава 1. Железо в почвах
Среднее содержание железа в почвах составляет 3,8%. В составе
почв в зависимости от кислотно-основных и окислительно-восстановительных
условий железо может присутствовать в степени окисления +3 и +2. Принципиально
возможно определение количества Fe(III) и количества Fe(II) в почвах, но, как
правило, при проведении валового анализа определяют общее содержание железа в
почвах. А.А. Роде (1971) считал существенным недостатком исследований
элементного состава почв отсутствие сведений о содержании Fe(III) и Fe(II) в
почвах. Введение в практику валового анализа почв определения Fe(II) позволило
бы выявить и количественно оценить особенности гидроморфного почвообразования.[3]
Этот элемент присутствует в почве в составе как первичных,
так и вторичных минералов, являясь компонентом магнетика, гематита,
титаномагнетита, глауконита, роговых обманок, пироксенов, биотитов, хлоритов,
глинистых минералов, минералов группы оксида железа. Много в почвах содержится
и аморфных соединений железа, особенно разнообразных гидроксилов (гетит,
гидрогетит и др.). Общее содержание в почве Fe2O3 колеблется в очень широких пределах (в %): от 0,5 –
1,0 в кварцево-песчаных почвах и 3 – 5 в почвах на лессах, до 8 – 10 в почвах
на элювии плотных ферромагнезиальных пород и до 20 – 50 в ферраллитных почвах и
латеритах тропиков. В почвах также часто наблюдаются железистые конкреции и
прослои.[2]
Согласно С. В. Зонну, соединения железа в почвах представлены
следующими формами, соотношение которых показано в таблице 1: 1)силикатное
железо, входящее в состав кристаллических решеток: а) первичных минералов; б) вторичных
(глинистых) минералов; 2) несиликатное (свободное) железо: а)
окристаллизованное (слабо или сильно) оксидов и гидроксидов; б) аморфных
соединений (железистых и гумус-железистых); в) подвижных соединений (обменных и
водно-растворимых).
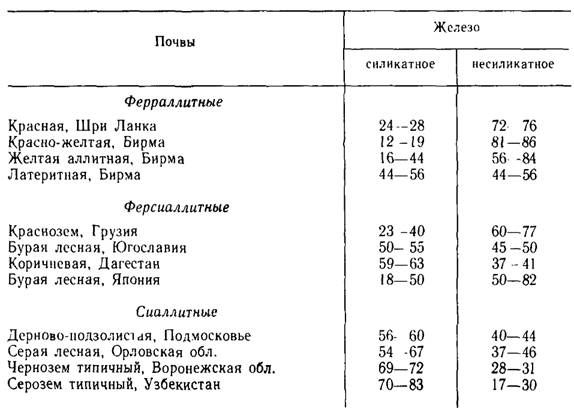
Таблица 1. Соотношение групп соединений железа в различных
почвах, % от валового
Глава 2. Методы определения железа в почвах
2.1 Атомно-абсорбционный метод
Для количественного определения общего содержания железа в
растворах, полученных при разложении почв, могут быть использованы разнообразные
методы. Широко применяют атомно-абсорбционную спектроскопию, фотометрические
методы и комплексонометрическое титрование.
Атомно-абсорбционный метод используют для определения
валового содержания железа и оценки содержания отдельных групп его соединений в
почвах. Железо атомно-абсорбционным методом может быть определено
непосредственно в пламени воздух—ацетилен и воздух—пропан—бутан, если его
концентрация близка или выше 1 мг/л. Растворы с более низкой концентрацией
железа рекомендуется анализировать после концентрирования или непламенным
вариантом атомно-абсорбционного метода с использованием графитовой кюветы.
Определение валового содержания железа проводят пламенным
вариантом метода. При этом, как правило, приходится в десятки раз разбавлять
растворы, полученные при разложении почвы. Атомно-абсорбционным методом железо
обычно определяют при длине волны 248,3 нм.
2.2 Комплексонометрическое определение железа в почвах
Определение общего содержания железа в почвах
комплексонометрическим методом проводят титруя ионы трехвалентного железа.
Комплексонат трехвалентного железа более устойчив, чем железа двухвалентного.
Поэтому перед титрованием Fe(II) окисляют азотной кислотой при нагревании.
В связи с тем что Fe(III) легко гидролизуется, его
комплексонометрическое титрование можно проводить лишь в сильно-кислой среде.
Трехвалентное железо может быть оттитровано даже при рН 1, константа
устойчивости комплексоната трехвалентного железа в этом случае равна 107'1
(1gКэффуст = 25,1
— 18,0). При титровании в сильнокислой среде устраняется мешающее влияние
многих сопутствующих элементов, которые в этих условиях либо вовсе не образуют
комплексонатов (Ва, Mg, Ca), либо комплексонаты образуются, но они
малоустойчивы (Си и др.). Относительно устойчивые комплексонаты в сильно кислой
среде образуют Bi3+, V3+, но их содержание в почвах
невелико и влиянием этих элементов на результаты определения железа в почвах
пренебрегают. Титан при высоких содержаниях в почвах может влиять на результаты
определения валового содержания железа.[3]
В связи с тем что железо медленно реагирует с комплексном
III, титруют подогретые растворы. В качестве индикатора используют
сульфосалициловую кислоту. Интервал рН, в котором развивается красно-фиолетовая
окраска сульфосалицилатного комплекса железа, не велик. Поэтому нужно очень
строго соблюдать предписанные методикой условия проведения анализа. В противном
случае окрашенное соединение может не образоваться. Часто раствор не
приобретает красно-фиолетовой окраски в связи с тем, что имеет более кислую,
чем необходимо, реакцию. В этом случае в анализируемую систему нужно добавить
раствор аммиака, а не сульфосалициловой кислоты.
В конечной точке титрования сульфосалицилат железа разрушается
вследствие образования более устойчивого комплексоната железа и лиловая окраска
исчезает, переходя в лимонно- желтую, обусловленную комплексонатом железа. Как
уже отмечалось, молярный коэффициент поглощения сульфосалицилата железа
невелик, поэтому переход окраски при комплексонометрическом титровании железа
нерезкий.
2.2.1 Методика комплексонометрического определения валового
содержания железа в почвах
Прежде чем проводить анализ на конических колбах вместимостью
250 мл, делают отметку на уровне, соответствующем объему 50 мл. В колбу
помещают 25 мл фильтрата, полученного после отделения кремниевой кислоты,
добавляют 5—7 капель концентрированной HN03 и нагревают до кипения
окисляя Fe(II).
Затем в колбу добавляют 10—15 капель 25%-ного раствора
аммиака, помещают кусочек индикаторной бумаги конго-рот и добавляют по каплям
сначала 25%-ный раствор аммиака, а затем 10%-ный до перехода синей окраски
индикаторной бумаги в бурую. Если при этом выпадет осадок, его растворяют
несколькими каплями 1 н. НСl. В
колбу приливают 5 мл 1 н. НСl, и
объем жидкости дистиллированной водой доводят до отметки, соответствующей 50
мл. Содержимое колбы нагревают до 50-60°, добавляют 1-3 капли 10%-ного раствора
сульфосалициловой кислоты и титруют 0,01 М раствором комплексона III до перехода лиловой окраски сульфосалицилата железа в бледно-желтую комплексоната
железа. Скорость реакции невелика, поэтому последние порции титранта добавляют
медленно
Реагенты:
1. 0,01 Мраствор комплексона III. См. раздел 5.6.2.1.
2. 25%-ный раствор аммиака.
3. 1 н. раствор НС1. 8,2 мл конц. НС1 разбавляют водой до 1 л.
4. 10%-ный раствор сульфосалициловой кислоты.
2.3 Фотометрические методы определения железа
В связи с тем что и Fe2+ и Fe3+
обладают хромофорными свойствами (электронная конфигурация атома железа — 1s2
2s2 2р6 3s2 Зр6 3d6 4s2),
для фотометрического определения железа используют различные типы химических
реакций, которые приводят к образованию окрашенных соединений.
Для определения общего содержания железа в почвах разработаны
фотометрические методы, основанные на образовании окрашенных соединений как
двух-, так и трехвалентного железа. В России наиболее широко используют
фотометрический сульфосалицилатный метод определения Fe(III).
Сульфосалициловая кислота в зависимости от рН раствора образует
с Fe(III) три различно окрашенных комплекса. При рН 2-3 образуется
красно-фиолетовый комплекс [FeSsal]+, при рН 4-8 коричневато-оранжевый комплекс
[Fe(Ssal)2]- и при рН 8—10 в аммиачном растворе
образуется устойчивый желтый комплекс [Fe(Ssal)3]3-.
Красно-фиолетовый комплекс, образующийся в кислой среде,
может быть использован для селективного определения Fe(III) в присутствии
Fe(II); вариант метода малочувствительный, молярный коэффициент поглощения при
длине волны 490 нм равен 2,6-103. Этот комплекс используют при комплексонометрическом
определении железа в почвах, предварительно переведя Fe(II) в Fe(III).
Для фотометрического определения валового содержания железа в
почвах используют комплекс желтого цвета, устойчивый в щелочной среде. Этот
вариант метода позволяет определить общее содержание железа в почвах, так как в
условиях эксперимента Fe(II) легко окисляется до Fe(III). Максимум светопоглощения
находится в области длин волн 420-430 нм, молярный коэффициент поглощения равен
5,8-103. Кривые светопоглощения сульфосалицилатных комплексов железа приведены
на рис. 1.
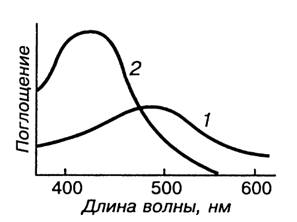
Рисунок 1. Кривые свстопоглощения сульфосалицилатных
комплексов железа при рН 2 (1) и рН 9 (2) молярный коэффициент поглощения
Сульфосалициловая кислота образует устойчивые комплексные соединения
со многими металлами. При проведении анализа добавляют избыток реагента, чтобы
предотвратить осаждение алюминия, магния, кальция при подщелачивании раствора.
Комплексы этих элементов с сульфосалициловой кислотой бесцветны. Окрашенные
комплексы сульфосалициловая кислота образует с металлами, обладающими хромофорными
свойствами.[3]
Для предотвращения выпадения в осадок гидроксида Mn(IV) при
подщелачивании в раствор предварительно добавляют гидроксиламин.
Валовое содержание железа может быть определено по окрашенному
комплексу двухвалентного железа с бртофенантролином (Methods of soil analysis, 1982). В этом случае железо восстанавливают
гидроксиламином до двухвалентного состояния. Затем в раствор добавляют ортофенантролин,
с которым Fe(II) образует устойчивый, имеющий красноватую окраску, комплекс —
Fe(C12H10N2)2+3. Эта
цветная реакция специфична для Fe2+. Присутствующие в почвах химические
элементы, как правило, не влияют на результаты анализа.
Ортофенантролин может быть использован для раздельного определения
Fe(II) и Fe(III). В этом случае анализируют две аликвоты исследуемого раствора.
В одной из них определяют суммарное содержание Fe(II) и Fe(III) после
предварительного восстановления трехвалентного железа, в другой — Fe(II). Определение
Fe(II) рекомендуется проводить в темноте или при слабом красном свете, чтобы
предотвратить фоторедукцию комплекса Fe(III) с ортофенантролином.
Окрашенный комплекс Fe(II) с ортофенантролином образуется
сразу после добавления реагента и устойчив в течение нескольких суток. Окраска
развивается в интервале значений рН от 2 до 9. Однако при проведении анализа
почв оптическую плотность измеряют при рН 3—5, так как при высоком содержании
кальция и фосфора в условиях меньшей кислотности может произойти образование
труднорастворимого фосфата кальция.
2.3.1 Методика
определения общего содержания железа сульфосалицинатным методом
В мерную колбу
вместимостью 100 мл помещают 10-25 мл фильтрата, полученного после отделения
кремниевой кислоты. В колбу добавляют 0,5 г гидроксиламина, приливают 5—10 мл 25%-ного раствора сульфосалициловой кислоты. Раствор в колбе перемешивают и
приливают аммиак до появления слабого запаха. Раствор снова перемешивают и
добавляют еще 2 мл аммиака. Объем жидкости в колбе доводят водой до метки,
раствор тщательно перемешивают и через 10 мин измеряют оптическую плотность.
Для построения
калибровочного графика в мерные колбы вместимостью 100 мл помещают 1, 2, 4, 5,
7 мл стандартного раствора с содержанием Fe 0,1 мг/мл. В колбы приливают 25 мл
воды и проводят анализ, как указано выше, для испытуемых растворов.
Строят график зависимости
оптической плотности от концентрации Fe2O3 и находят содержание железа в почве.
Реагенты:
1. 25%-ный раствор
сульфосалициловой кислоты. Навеску сульфосалициловой кислоты массой 25 г растворяют в 100 мл дистиллированной воды. Раствор хранят в темной склянке с притертой пробкой.
3. Гидроксиламин
солянокислый NH2OH HCl.
4. Стандартный раствор
железа. Навеску [(NH4)2SO4 Fe2(SO4)3*24
Н2O] массой 0,8637 г растворяют в 1 л 5%-ного раствора H2S04 и тщательно перемешивают. Полученный раствор должен
содержать в 1 мл 0,1 мг железа. Концентрацию железа в растворе проверяют
гравиметрическим методом.
Стандартный раствор
железа может быть получен растворением 0,1000 г металлического железа в 5%-ном растворе серной кислоты. Если для полного растворения железа необходимо, раствор
подогревают.
2.4 Методика
определения подвижных форм железа с помощью роданида аммония
Навеску воздушно-сухой
почвы 5 г, просеянной через сито с отверстиями 1 мм, помещают в колбу и приливают 250 мл 0,2 Н раствора HCL, перемешивают и настаивают в течение суток.
Суспензии фильтруют,
пипеткой отбирают 5 мл фильтрата в колбу на 100 мл и приливают 5 мл HNO3, затем перемешивают и по каплям добавляют раствор KMnO4 с м.д. 0,3% до образования неисчезающей слабо-розовой
окраски от одной капли, затем добавляют 80-90 мл дистиллированной воды и 5 мл
аммония роданистого. Доводят водой до метки и колориметруют.
Из рабочего раствора соли
Мора готовят эталонные растворы. Для этого в колбы на 100 мл наливают
количество раствора по таблице 2, доливают дистиллированной воды около 80 мл,
приливают 5 мл аммония роданистого, доводят водой до метки, перемешивают
колориметрируют сразу в течение 15 – 30 мин.
|
№ колбы
|
Объем раствора соли
Мора, мл
|
Масса Fe в 100 мл
эталонного раствора, мг
|
|
1
|
1
|
0,1
|
|
2
|
2
|
0,2
|
|
3
|
4
|
0,4
|
|
4
|
8
|
0,8
|
|
5
|
16
|
0,16
|
|
6
|
24
|
0,24
|
|
7
|
32
|
0,32
|
Таблица 2. Таблица
эталонных растворов для проведения анализа
По результатам
фотометрирования эталонных растворов строят градуировачный график. По оси
абсцисс откладывают массу железа в миллиграммах, соответствующую объему соли
Мора в эталонных растворах, а по оси ординат – соответствующие им показания
прибора. Пользуюсь градуировачным графиком, по результатам анализа определяют
массу железа в анализируемых пробах.
Для вычисления массы
подвижных форм железа при натуральной влаге используют следующие уравнение:
Fe % = m*250*100/V*m1
где m – масса Fe по градуировачному графику; 250 – объем HCL, приливаемый к навеске; V – объем вытяжки, взятый на
определение, в мл; m1 – масса навески, в г.
Для вычисления массы
подвижных форм железа в пересчете на оксид железа при натуральной влаге
используют следующие уравнение:
Fe % =
m*250*1,43*100/V*m1
где 1,43 – коэффициент
пересчета на оксид железа.
Список литературы
1. Почвоведение: учебник для
сельскохозяйственных вузов: допущено Главным управлением высшего и среднего
сельскохозяйственного образования Минестерства сельского хозяйства СССР/
Кауричева И. С., Гречина И. П. – Москва: «Колос», 1969. – 542 с.
2. Почвоведение: учебник для
университетов. В 2 ч./ Под ред. В. А. Ковды, Б. Г. Розанова. Ч. 1. Почва и
почвообразование / Богатырев Л. Г., Васильевская В. Д., Владыченский А. С. и
др. – Москва: Издательство Высшая школа, 1988. – 368 с.
3. Химический анализ почв: учебник
для студентов высших учебных заведений, обучающихся по направлению и
специальности «Почвоведение»: рекомендовано
Министерством общего и профессионального образования Российской
Федерации/Воробьева Людмила Андреевна. – Москва: Издательство Московского
университета, 1998. – 271 с.
4. Материалы сайта http://www.pochva.com/