|

|

|
|

|
|
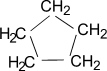
Циклопропан
|
Циклобутан
|
Циклопентан
|
Циклогексан
|
По своему
строению молекулы органическогих соединений различают на соединения с открытой
цепью и циклические. Циклы могут быть построены либо только из атомов углерода
(карбоциклы), либо могут включать в себя атомы других элементов (гетероциклы).
В свою очередь, циклические соединения бывают предельными, непредельными и
ароматическими.
Молекулы
циклоалканов имеют скелет, построенный в виде цикла из только sp3-гибридных
атомов углерода. Для образования названия циклоалканов необходимо к названию
соответствующего предельного углеводорода добавить приставку «цикло». Так,
наименьший из возможных циклоалканов – циклопропан, за ним следует циклобутан,
затем циклопентан и т.д.
Положения
заместителей указывают, нумеруя атомы цикла, причем атому с наиболее старшим
заместителем присваивается номер 1. В дизамещенных циклоалканах заместители
могут располагаться по одну (цис-) или по разные стороны плоскости кольца
(транс-).
Молекулы
циклоалканов могут состоять из двух и более циклов. Бициклические углеводороды
следует различать по способу соединения (аннелирования) циклов. Если два цикла
имеют лишь один общий атом углерода, соединения называют спироциклическими.
Названия таких бициклов образуют, добавляя приставку «спиро» к названию соответствующему
гомолога алкана. После приставки в квадратных скобках указывают две цифры,
обозначающие число атомов углерода, расположенных по каждую сторону от узлового
С-атома. Нумерацию атомов начинают с меньшего цикла, последним номером
обозначают узловой атом.
В другом
способе аннелирования циклы имеют два общих атома углерода. Это – так
называемые мостиковые циклоалканы. Названия таких соединений начинается с
указания количества циклов приставками бицикло-, трицикло-, затем указываются
три цифры, обозначающие число углеродных атомов каждого мостика, связанного с
узловыми атомами. В конце пишется название соответствующего алкана. Нумеруют
атомы, начиная с одного узлового и передвигаясь по большему (главному) циклу к
другому узловому С-атому. Иногда указывают дополнительные координаты мостика.
Получение
1.
Циклоалканы содержатся в значительных количествах в нефтях некоторых
месторождений (отсюда произошло одно из их названий – нафтены). При
переработке нефти выделяют главным образом циклоалканы С5 Н10
– С7 Н14

(вместо металлического натрия
используется также порошкообразный цинк).
Строение образующегося циклоалкана
определяется структурой исходного дигалогеналкана. Этим путем можно получать
циклоалканы заданного строения. Например, для синтеза 1,3-диметилциклопентана
следует использовать 1,5-дигалоген – 2,4-диметилпентан:
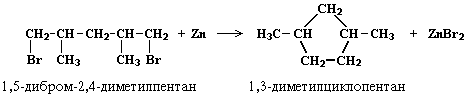
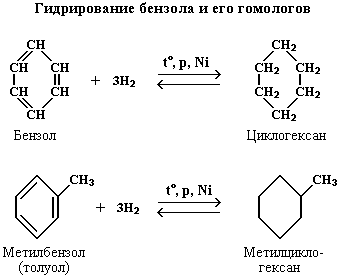
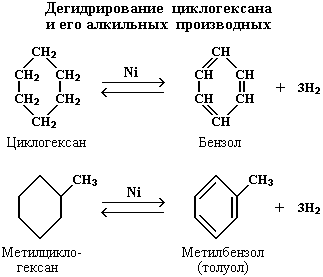
Существуют и другие методы получения
циклоалканов. Так, например, циклогексан и его алкильные производные получают
гидрированием бензола и его гомологов, являющихся продуктами нефтепереработки.
Изомерия
Для
циклопарафинов, начиная с C4H8, характерны некоторые виды
структурной изомерии, связанные:
a) с числом
углеродных атомов в кольце – например, 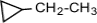 (этилциклопропан),
(этилциклопропан), 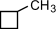 (метилциклобутан);
(метилциклобутан);
b) с числом
углеродных атомов в заместителях – 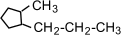 (1-метил-2-пропилциклопентан),
(1-метил-2-пропилциклопентан), 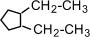 (1,2-диэтилциклопентан)
(1,2-диэтилциклопентан)
c) с
положением заместителя в кольце – 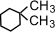 (1,1-диметилциклогексан),
(1,1-диметилциклогексан), 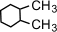 (1,2-диметилциклогексан)
(1,2-диметилциклогексан)
Для
циклоалканов характерна также межклассовая изомерия с алкенами.
При наличии
двух заместителей в кольце у разных углеродных атомов возможна геометрическая
цис-транс-изомерия, начиная с C5H10, и оптическая
изомерия. Оптическая изомерия проявляется в том случае, если молекула не имеет
плоскости симметрии.
Цис-транс-изомерия
в циклических соединениях
При наличии
двух заместителей в циклических соединениях также возможна цис-транс-изомерия.
Метильные группы в приведенных примерах могут располагаться по одну сторону
плоскости кольца (такой изомер называется цис-изомером) и по разные стороны
(такой изомер называется транс-изомером).
Естественно,
что при наложении друг на друга моделей цис- и транс- изомеров они не
совмещаются. Взаимные изомеризации требуют разрыва цикла с последующим его
замыканием или разрыва связи заместителя с углеродным атомом цикла и
образованием новой связи с другой стороны цикла.
Следует
отметить, что в циклических соединениях возможно возникновение не только
цис-транс-, но и зеркальной изомерии. При наложении модели молекулы цис-изомера
с одинаковыми заместителями и ее зеркального отражения они совмещаются, в то
время как таковое невозможно для цис-изомера с различными заместителями. Для
транс-изомеров совмещение модели молекулы и ее зеркального отражения невозможно
как при одинаковых, так и различающихся заместителях.
Циклобутан,
циклопентан и их конформации
Циклические
соединения – это такие органические соединения, в которых углеродные атомы
составляют замкнутые цепи, т.е. циклы. Простейшими представителями таких
соединений являются циклопарафины или циклоалканы.
Прочность
связей в циклических соединениях зависит от числа атомов, участвующих в
образовании цикла. Она определяется степенью его напряженности, обусловленной
изменением валентных углов атомов цикла и отклонением этих атомов от
нормального направления.
Чем больше
отклонение валентного угла от нормального, тем более напряжены и,
следовательно, непрочны циклы. Однако в отличие от циклопропана циклобутан и
циклопентан имеют неплоские циклы. Один из атомов углерода непрерывно выходит
из плоскости. Циклобутан существует в виде неплоских «сложенных» конформаций.
Циклопентан характеризуется конформацией «конверт». Таким образом, обсуждаемые
циклы находятся в колебательном движении, приводящем к уменьшению «заслоненности»
атомов водорода у соседних углеродных атомов и снижению напряжения.
Циклогексан
и его конформации
Для
циклогексана, как правильного шестиугольника, межъядерные углы составляют 120º.
Если бы молекула циклогексана имела плоское строение, то отклонение от
нормального валентного угла атома углерода составляло: 109,5º-120º =
10,5º.
Однако
циклогексан и большие циклы имеют неплоское строение. В рассматриваемой
молекуле циклогексана сохраняются обычные валентные углы при условии его
существования в двух конформациях «кресла» и «ванны». Конформация «кресла» менее
напряжена, поэтому циклогексан существует преимущественно в виде конформеров I
и III, причем цикл претерпевает непрерывную инверсию (inversio – с латинского
переворачивание, перестановка) с промежуточным образованием конформера II:

ось симметрии
II III I
Двенадцать
связей C–H, которые имеются у циклогексана в конформации «кресла», делятся на
два типа. Шесть связей направлены радиально от кольца к периферии молекулы и
называются экваториальными связями (e – связи), остальные шесть связей
направлены параллельно друг другу и оси симметрии и называются аксиальными (a –
связи). Три аксиальные связи направлены в одну сторону от плоскости цикла, а
три – в другую (имеется чередование: вверх-вниз).
Свойства
циклоалканов
Физические
свойства
циклоалканов закономерно изменяются с ростом их молекулярной массы. Пpи
ноpмальных условиях циклопpопан и циклобутан – газы, циклоалканы С5Н10 – С16Н32 – жидкости, начиная с С17Н34, – твердые вещества.
Температуры кипения циклоалканов выше, чем у соответвующих алканов. Это связано
с более плотной упаковкой и более сильными межмолекулярными взаимодействиями
циклических структур.
Химические
свойства
циклоалканов сильно зависят от размера цикла, определяющего его устойчивость.
Трех- и четырехчленные циклы (малые циклы), являясь насыщенными, тем не
менее, резко отличаются от всех остальных предельных углеводородов. Валентные
углы в циклопропане и циклобутане значительно меньше нормального
тетраэдрического угла 10928’, свойственного sp3-гибридизованному атому
углерода.
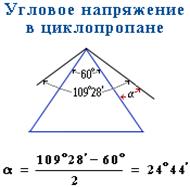
Это приводит
к большой напряженности таких циклов и их стремлению к раскрытию под действием
реагентов. Поэтому циклопропан, циклобутан и их производные вступают в реакции
присоединения, проявляя характер ненасыщенных соединений. Легкость реакций
присоединения уменьшается с уменьшением напряженности цикла в ряду:
циклопропан > циклобутан >> циклопентан.
Наиболее
устойчивыми являются 6-членные циклы, в которых отсутствуют угловое и другие
виды напряжения.
Малые
циклы (С3Н6 – С4Н8) довольно легко вступают
в реакции гидрирования:
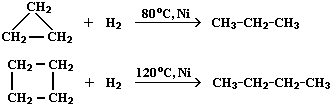
Циклопропан и
его производные присоединяют галогены и галогеноводороды:
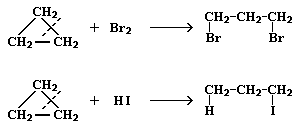
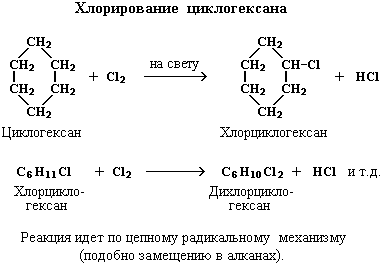
В других
циклах (начиная с С5) угловое напряжение снимается благодаря
неплоскому строению молекул. Поэтому для циклоалканов (С5 и выше)
вследствие их устойчивости характерны реакции, в которых сохраняется циклическая
структура, т.е. реакции замещения.
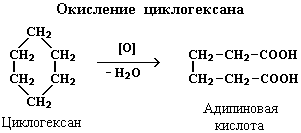
Столь резкое
отличие в свойствах циклоалканов в зависимости от размеров цикла приводит к
необходимости рассматривать не общий гомологический ряд циклоалканов, а
отдельные их ряды по размерам цикла. Например, в гомологический ряд циклопропана
входят: циклопропан С3Н6, метилциклопропан С4Н8,
этилциклопропан С5Н10 и т.д.
Наибольшее
практическое значение имеют циклогексан, этилциклогексан. Циклогексан
используется для получения циклогексанола, циклогексанона, адипиновой кислоты,
капролактама, а также в качестве растворителя. Циклопропан используется в
медицинской практике в качестве ингаляционного анестезирующего средства.
Список использованной литературы
1. Химия: Органическая
химия: Учебное издание для 10 кл. сред. шк. – Москва, Просвещение, 1993
2. Глинка Н.Л. Общая
химия. -25-е изд., испр. – Л.: Химия
3. Артеменко А.И. Органическая
химия: учеб. для строит. спец. вузов. – М.: Высшая школа, 2000.
4. Березин Б.Д., Березин Д.Б. Курс
современной органической химии. Учебное пособие для вузов. – М.: Высшая школа,
1999.
5. ХИМИЯ. Справочник
школьника, – М., 1995.
6. ХИМИЯ. Энциклопедия
для детей. АВАНТА, 2000.
7. Хомченко Г.П. Химия
для поступающих в ВУЗы. – М., 1995 г.
8. «Органическая химия».,
Просвещение, 1991