Жидкокристаллические полиэфиры, содержащие фрагменты камфорной кислоты
ЖИДКОКРИСТАЛЛИЧЕСКИЕ ПОЛИЭФИРЫ, СОДЕРЖАЩИЕ ФРАГМЕНТЫ КАМФОРНОЙ КИСЛОТЫ
В последние
годы проявляется особый интерес к введению в ЖК-по-лимеры с мезогенными
группами в основной цепи различных алифатических циклов [1], что позволяет
значительно улучшить их растворимость и удобных растворителях и понизить
температуры фазовых переходов. В эти циклы могут быть включены хиральные
центры. Тогда появится возможность получения оптически активных полимеров,
холестериков или хиральных смектиков.
Продолжая
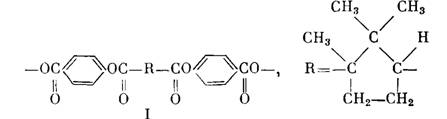
ранее начатые нами исследования мезогенных свойств фрагмента типа I [2],
содержащего варьируемое центральное ядро R и боковые
4-оксибензоатные группы, мы решили в качестве центрального ядра ввести остаток
камфорной кислоты
Ранее было
показано, что использование как мономеров дихлорангид-ридов, структура которых
соответствует структуре мезогенного фрагмента, позволяет получать методом
высокотемпературной безакцепторной поликонденсации широкий набор ЖК-полиэфиров
высокой ММ [2]
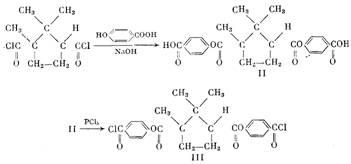
Условия
синтеза полимеров отрабатывали на рацемических производ-ных. Дихлорангидрид III
был получен в условиях, аналогичных условиям получения камфороилхлорида [3].
Поликонденсацией III с гексамети-ленгликолем-1,6, декаметиленгликолем-1,10,
хлоргидрохиноном и гидрохиноном были получены соответствующие полиэфиры IVa-r. За
исключением поли(га-фенилен-камфороил-бкс-4-оксибензоата) IVr, который не
плавится до температуры деструкции, все они имеют низкие температуры размягчения
и не обладают ЖК-свойствами (табл. 1).
Поликонденсация
камфороилхлорида с хлоргидрохиноном, гидрохиноном и 4,4'-диоксидифенилом также
привела к получению полимеров V— VII, не обладающего ЖК-свойствами (табл. 1).
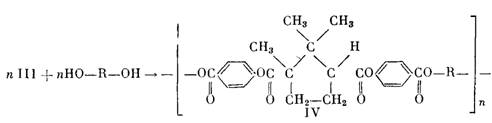
То
обстоятельство, что на основе 4,4'-диоксидифенила и различных алифатических
кислот Кригбаум с сотр. получил широкий набор ЖК-по-лиэфиров [4], позволяло
надеяться получить ЖК-сополиэфиры сополиконденсацией 4,4'-диоксидифенила,
камфороилхлорида и соответствующего алифатического дихлорангидрида. Нами был
выбран дихлорангидрид пимелиновой кислоты, так как было известно, что его
гомополимер с 4,4'-диоксидифенилом образует нематический тип мезофазы.
Следовательно, при введении хиральной добавки можно было получить холестерический
тип мезофазы [5].
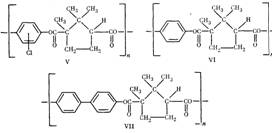

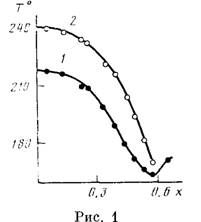
Рис. 1. Зависимость температур фазовых переходов от состава сополиэфиров VIII: 1
и 2 — температуры
плавления и изотропизации
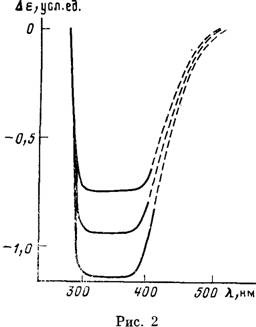
Рис. 2. Спектр кругового дихроизма пленки сополиэфира VIH-10 использован L-камфороилхлорид
и в результате получен набор ЖК-со полимеров VIII (рис. 1).

Все
сополиэфиры VIII, обладающие ЖК-свойствами, при охлаждении из изотропного
расплава образуют планарную текстуру, которую удается «заморозить» в пленке при
быстром охлаждении. Планарная текстура сополиэфиров VIII с х>0,5 отражает свет в видимой области (голубой), что часто
наблюдается у низкомолекулярных холестеринов [6]. Нами были сняты спектры
кругового дихроизма (КД) полученных пленок (рис. 2). Эти спектры по форме
аналогичны полученным Кригбаумом и Ватапабе для пленок сополиэфиров
4,4'-диоксидифенила, 3-метиладипи-новой кислоты и алифатических дикарбоновых
кислот [7].
Мы полагаем,
однако, что следует с осторожностью связывать наблюдаемый спектр только с
круговым дихроизмом, вызванным (закрученной) холестерической структурой пленок,
так как сама планарная текстура является двулучепреломляющей и обладает
свойствами двуосного кристалла. Об этом свидетельствует изменение кругового
дихроизма при повторном снятии спектра одной и той же пленки. В то же время
постоянство длины волны максимума спектра КД свидетельствует о том, что основной вклад в явление кругового дихроизма вносит планарная
холестерическая текстура.
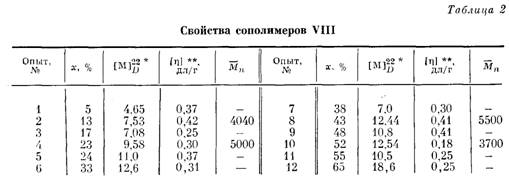
Рис. 3. Спектры поглощения и кругового ди- [в].рад.смг/дМОль хроизма растворов полимеров VII (1), VIII-1, (2), VI1I-10 (3) и VIII-4 (4) в хлороформе (о) и диоксане (б)
Рис. 4. Спектры кругового дихроизма полимера VIII-10 в различных растворителях:
1 — 100%-ный хлороформ; 2 — 50% хлороформа+ + 50% диоксана; 3 — 22%
хлороформа+ 78% диокеана; 4 — 100% диоксана
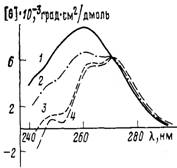
Рис. 4. Спектры кругового дихроизма полимера VIII-10 в различных растворителях:
1 — 100%-ный хлороформ; 2 — 50% хлороформа+ + 50% диоксана; 3 — 22%
хлороформа+ 78% диокеана; 4 — 100% диоксана
Нами были исследованы хироптические свойства сополиэфиров VIII в
растворе (табл. 2). Нелинейная зависимость величины мольного оптического
вращения от состава, вероятно, определяется различной ММ этих сополиэфиров [8].
Спектры КД растворов сополиэфиров VIII приведены на рис. 3. Обращает на себя
внимание сильное влияние растворителя. Для подобных алкиленароматических
полиэфиров хлороформ — более хороший растворитель, чем диоксан [9]. В то же
время фрагмент камфорной кислоты, как об этом можно судить на основании величин
характеристической вязкости и ММ (табл. 2), является более «гибкой» развязкой,
чем фрагмент пимелиновой кислоты. Величина КД в случае сополимеров VIII с
большим содержанием фрагментов камфорной кислоты (55%) не зависит от
растворителя и прямо пропорциональна содержанию этих фрагментов. Вероятно, она
определяется в основном дисимметричным окружением бифенильного хромофора.
Резкое изменение величины КД происходит при переходе от хлороформа к диоксану
для сополимера VII-10 с £=0,52, что, вероятно, обусловлено изменением конформации
полимера, вызванного ухудшением качества растворителя. Эти изменения происходят
в широком диапазоне соотношений хлороформ — диоксан (рис. 4) и отражают
усредненное влияние растворителя на конформацию макромолекул. Сополимер,
содержащий 23% камфорной кислоты, растворяется в диоксане настолько плохо, что
нам не удалось получить его истинный спектр КД (опалесцирующие растворы этого
полимера проявляют аномальный КД, характерный для агрегирующих систем [10]).
Таким образом, конформация макромолекулы с мезогенными группами в
основной цепи определяется соотношением качества растворителя и «гибкости»
развязки и может изменяться от статического клубка [11] до конформации упорядоченной [ 12].
Вязкость полученных полимеров измеряли на вискозиметре типа Уббелоде. Мп находили методом ИТЭК на приборе «Hitachi—Perkin—Elmer» модели 115 в
хлороформе. Температуры фазовых переходов определяли на столике для определения
температуры плавления «Боэтиус» с поляризационным микроскопом. Спектры ПМР
снимали на приборах «JEOL C60L» (60 МГц) и «Tesla BS-497» (100 МГц). Оптическое вращение определяли на спектрополяриметре «Pepol-бО»
(Великобритания) для растворов концентрацией 0,1-0,5 мг/мл в CF3COOH. Спектры УФ и КД
записывали на приборах «Specord UV-VIS» и «Магк III» (Франция) для растворов с концентрацией 0,01—0,05 мг/мл
в диоксане.
Камфороил-бис-4-оксибензойную кислоту (II) получали следующим образом. К
раствору 72,5 г (0,53 моля) α-оксибензойной кислоты в 600 мл 1 н. NaOH в течение 30 мин
при перемешивании прикапывали раствор 60 г (0,25 моля) камфороил хлорида в 200
мл четыреххлористого углерода. Затем при комнатной температуре раствор
перемешивали еще 5 ч, следя за тем, чтобы рН не опускался ниже 8. Затем раствор
подкисляли НС1 до рН 5 и отфильтровывали выпавший осадок. Его дважды
перекристаллизовывали из воды и высушивали. Полученный продукт представлял собой
кристаллогидрат II с одной молекулой воды. Выход 12,5 г (11%); Гпл=177-178°.
Спектр ПМР (100 МГц) в ацетоне-de. б, м. д.: а
- 8,06 (4Н); б - 7,18 (4Н); в -1,19-1,09 (6Н); г-0,76 (ЗН);
9-3,15-1,0 (5Н).
Вычислено, %: С 63,43; Н 4,88. С24Н22 09.
Найдено, %: С 63,37; Н 4,82.
Дихлорангидрид камфороил-бис-4-оксибензойной кислоты (III) получали
следующим образом. 12,5 г (0,027 моля), 11,8 г (0,20 моля) РС15 в 50
мл абс. петролейного эфира нагревали при 40° 3 ч до прекращения выделения газа.
Затем отгоняли эфир в хлорокись фосфора. Оставшаяся прозрачная желтовая
жидкость представляла собой искомый продукт. Выход 10,4 г (81%). Спектр ПМР
(100 МГц) в CDCU 8 (м.д.): о-8,08 (ЗН); 6-7,20 (4Н); в - 1,19; 1,09 (6Н); г - 0,86 (ЗН); д - 3,15-1,0 (5Н).
Для поликонденсации в пробирку помещали эквимольные количества диола и
дихлорангидрида (по 0,002 моля) в 4 мл дифенилоксида, в течение 15 мин
продували аргоном, помещали в масляную баню, нагретую до 160°, и в токе аргона
нагревали в течение 2,5 ч. Затем полимер высаждали в толуол, фильтровали и
дважды переосаждали из хлороформа или смеси CF3COOH: СНС1з (1:1 по
объему) в метанол. Выход полимеров 95-98%.
ЛИТЕРАТУРА
1.Polk М., Nandu М. Ц J. Polymer
Sci. Polymer. Chem. Ed. 1986. V. 24. №
8. P. 1923.
2.Bilibin A.Yu., Zuev V.V., Skorokhodov
S.S. // Makromolek. Chem. Rapid Commun.
1985. B. 6. № 9. S. 601.
3.Bredt J./JBer. 1912. B. 45. № 1. S. 1419.
4.Krigbaum W.R., Watanabe J., Ishikawa T. // Macromolecules. 1983. V. 16. № 8. P. 1271.
5.Shibaeu V.P., Plate N.Л.//Advances
Polymer Sci. 1984. V. 60/61. P. 173.
6.Беляков В.А., Сонин А.С. // Оптика холестерических жидких кристаллов. М., 1982. С. 360.
7.Watanabe J., Krigbaum W.R. // J. Polymer Sci. Polymer
Phys. Ed. 1985. V. 23. №3. P. 565.
9.Lenz R. W. //Recent Advances in Liquid Crystalline Polymers/Ed. by
Chapoy L. L. L.; N. Y., 1985. P. 3.
10.Keller D., Bustamante C. // J.
Chem. Phys. 1986. V. 84. № 6. P. 2981.
11.Blumstein A., Maret G., Vilasugar S. // Macromolecules. 1984. V. 14. № 8. P. 1543.
12.Chiellini E., Galli G. // Faraday Disc. Chem. Soc. 1985. V. 79. № 16. P. 1.