Анализ почвы
ФЕДЕРАЛЬНОЕ
АГЕНСТВО ПО ОБРАЗОВАНИЮ
ГОСУДАРСТВЕННОЕ
ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО
ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«ЛИПЕЦКИЙ
ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙЦ УНИВЕРСИТЕТ»
Кафедра
химии
Зачетная задача по предмету:
«Аналитические
методы анализа в мониторинге объектов окружающей среды»
на тему:«Анализ почвы»
Выполнил:
студент ХМФ гр. АХ-06-1
Ирхина Э.Е.
Проверил:
Дергунова Елена
Сергеевна
Липецк 2010
г.
Введение
Почва - особое природное
образование, сформировавшееся в результате длительного преобразования
поверхностных слоев литосферы под совместным взаимообусловленным
взаимодействием гидросферы, атмосферы, живых и мертвых организмов. Почва
состоит из органических, минеральных, органоминеральных комплексных соединений,
почвенной влаги, воздуха и живых существ, населяющих ее.
Почва является одним из элементов
биосферы, которые обеспечивают циркуляцию химических веществ в системе
окружающая среда - человек. Причем это относится не только к эндогенным
химическим веществам, но и к экзогенным химическим веществам, поступающим в
почву с выбросами промышленных предприятий, сточными водами, выбросами авто- и
авиатранспорта, при обработке сельскохозяйственных земель
Почва является местом сбора и
хранения большого числа загрязнителей, куда они попадают в результате
техногенной деятельности человека и выбросов загрязнителей из природных
источников. Она не обладает свойством подвижности, характерным для других
природных сред, и наиболее подвержена загрязнению. Кроме того, многие
соединения, попадая в почву, вследствие химических и микробиологических
превращений могут стать более токсичными, чем исходные. Из почвы может
происходить загрязнение воды, воздуха, пищевых продуктов и других элементов
биосферы канцерогенными и радиоактивными веществами.
Вследствие этого необходимо
регулярно проводить мониторинг почв в различных раонах города и области.
В данной зачетной задаче проводился
общий анализ почвы, отобранной в Усманском районе, Липецкой области.
1 Мониторинг
почв
Мониторинг состояния почв предназначен для
регулярных наблюдений за химическим загрязнением почв, их состоянием;
обеспечивает сбор, передачу и обработку полученной информации в целях
своевременного выявления негативных процессов, прогнозирования их развития,
предотвращения вредных последствий и определения степени эффективности
осуществляемых природоохранных мероприятий.
В отличие от воды и атмосферного воздуха,
которые являются лишь миграционными средами, почва является наиболее
объективным и стабильным индикатором техногенного загрязнения. Она четко
отражает эмиссию загрязняющих веществ и их фактического распределения в
компонентах городской территории. Наиболее крупные промышленные города образуя
обширные зоны загрязнений, постепенно превращаются в сплошные техногенные
территории, представляющие серьезную опасность для здоровья проживающего на них
населения.
В этой связи, постоянное наблюдение за
содержанием промышленных токсикантов в почвах и тенденцией их содержанием
является наиболее актуальным.
Одним из наиболее мощным факторов, приводящим к
загрязнению окружающей среды, является промышленность.
Зона существенного загрязнения почв химическими
элементами в окрестностях промышленных предприятий занимает площадь радиусом 10
км с гораздо большей протяженность (до 30 км и более) в направлении господствующих
ветров, а также в направлении стока поверхностных и грунтовых вод.
Источниками загрязнения почвы являются:
· выбросы вредных веществ в
атмосферный воздух от стационарных и передвижных источников загрязнения;
· полигоны промышленных и бытовых
отходов;
· несанкционированные свалки
промышленных и бытовых отходов;
· средства химической защиты растений
и минеральные удобрения.
На загрязнение почвы значительное влияние
оказывают проливы нефтепродуктов, неорганизованные сбросы ливневых и талых вод,
а также санитарное состояние городской территории.
Классификкация почв
Основной единицей классификации почв
является тип почв. Понятие «тип почв». Под типом почв понимают почвы,
образованные в одинаковых условиях и обладающие сходными строением и свойствами.
К одному типу почв относятся почвы:
· 1) со сходными процессами
превращения и миграции веществ;
· 2) со сходным характером
водно-теплового режима;
· 3) с однотипным строением почвенного
профиля по генетическим горизонтам;
· 4) со сходным уровнем природного
плодородия;
· 5) с экологически сходным типом
растительности.
Широко известны такие типы почв, как
подзолистые, черноземы, красноземы, солонцы, солончаки и др.
Каждый тип почв последовательно подразделяется
на подтипы, роды, виды, разновидности и разряды.
Подтипы почв представляют собой группы почв,
различающиеся между собой по проявлению основного и сопутствующего процессов
почвообразования и являющиеся переходными ступенями между типами. Например, при
развитии в почве наряду с подзолистым процессом дернового процесса формируется
подтип дерново-подзолистой почвы. При сочетании подзолистого процесса с глеевым
процессом в верхней части почвенного профиля формируется подтип глееподзолистой
почвы.
Подтиповые особенности почв отражаются в особых чертах
их почвенного профиля. При выделении подтипов почв учитываются процессы и
признаки, обусловленные как широтнозональными, так и фациальными особенностями
природных условий. Среди последних первостепенную роль играют термические
условия и степень континентальности климата.
В пределах подтипов выделяются роды и виды почв.
Роды почв выделяются внутри подтипа по особенностям почвообразования, связанным
прежде всего со свойствами материнских пород, а также свойствами,
обусловленными химизмом грунтовых вод, или со свойствами и признаками,
приобретенными в прошлых фазах почвообразования (так называемые реликтовые
признаки).
Роды почв выделяются в каждом типе и подтипе
почв. Самые распространенные из них:
· 1) обычный род, т. е. отвечающий по
своему характеру подтипу почв; при определении почв название рода «обычный»
опускается;
· 2) солонцеватые (особенности почв
определяются химизмом грунтовых вод);
· 3) остаточно-солонцеватые
(особенности почв определяются засоленностью пород, которая постепенно
снимается);
· 4) солончаковатые;
· 5) остаточно-карбонатные;
· 6) почвы на кварцево-песчаных
породах;
· 7) почвы контактно-глеевые
(формируются на двучленных породах, когда супесчаные или песчаные толщи
подстилаются суглинистыми или глинистыми отложениями; на контакте смены наносов
образуется осветленная полоса, образующаяся за счет периодического
переувлажнения);
· 8) остаточно-аридные.
Виды почв выделяются в пределах рода по степени
выраженности основного почвообразовательного процесса, свойственного определенному
почвенному типу.
Для наименования видов используют генетические
термины, указывающие на степень развития этого процесса. Так, для подзолистых
почв - степень подзолистости и глубина оподзоливания; для черноземов - мощность
гумусового горизонта, содержание гумуса, степень выщелоченности; для солончаков
- характер распределения солей по профилю, морфология поверхностного горизонта
(пухлые, отакыренные, выцветные).
Внутри видов определяются разновидности почв.
Это почвы одного и того же вида, но обладающие различным механическим составом
(например, песчаные, супесчаные, суглинистые, глинистые). Почвы же одного вида
и одного механического состава, но развитые на материнских породах разного
происхождения и разного петрографического состава, выделяются как почвенные
разряды.
Дерново-подзолистые почвы - отличаются невысоким
содержанием гумуса (0,5-2,5%) и небольшим гумусовым слоем (10-20 см), в связи с
этим - невысоким естественным плодородием и, как правило, кислой реакцией
(рН=4-5). В большинстве случаев они пере увлажнены.
Нуждаются в дренажных и других осушительных
работах, увеличении гумусового горизонта, а также регулярном известковании и
внесении повышенных доз органических удобрений или землевании.
Дерново-карбонатные почвы. В отличие от
дерново-подзолистых почв обладают более высокой продуктивностью (гумус - 2-4%),
меньшей кислотностью рН=6 и более благоприятными физико-механическими
показателями. Для получения высоких урожаев нуждаются только в повышенных дозах
органических и минеральных удобрений.
Серые лесные почвы. По многим
показателям близки к дерново-карбонатным почвам (только несколько выше
кислотность (рН-5,5-6,5). Они склонны к замыванию и переуплотнению. Нуждаются в
периодическом известковании, углублении пахотного горизонта, а также в удобрении
фосфором и азотом.
Торфяно-болотные почвы.
Характеризуются высоким естественным плодородием и большим содержанием азота
(2-4%), низким содержанием фосфора, высокой кислотностью (рН=3,5-5) и низкими
физико-механическими свойствами. Нуждаются в регулировании водного режима
(осушение-орошение), внесении фосфорно-калийных удобрений, регулярном
известковании и внесении микроэлементов.
Черноземные почвы. Лучшие из почв по
всем показателям (уровню плодородия, глубине гумусового горизонта (если не
эродированы), содержанию макро- и микроэлементов и физико-механическим
параметрам почвы). Оподзоленные черноземы склонны к заиливанию и
переуплотнению, а карбонатные черноземы бедны железом : в доступной для
растений форме (провоцируется хлороз винограда и плодовых).
2 Методика определения
гигроскопической влаги почвы
Навеску почвы 2-5 г берут на
аналитических весах в предварительно высушенных при температуре 100-105 0С
и взвешенных стеклянных бюксах (бюксы взвешивают с крышками). Бюксы с почвой в
течение 5 ч выдерживают в сушильном шкафу при температуре 100-1050С.
С помощью щипцов с резиновыми наконечниками бюксы вынимают из сушильного шкафа,
закрывают крышками, охлаждают в эксикаторе и взвешивают. Условились считать,
что выдерживание почвы в течение 5 ч при температуре 100-1050С
приводит к полной потере гигроскопической влаги. Если необходимо проверить
полноту удаления гигроскопической влаги, бюксы с почвой снова ставят в
сушильный шкаф на 1,5-3 ч и взвешивают. Высушивание прекращают, если масса
равна или больше результата предыдущего взвешивания (увеличение массы может
произойти за счет окисления некоторых компонентов почв). Расчет массовой доли
гигроскопической влаги (%) проводят по уравнению:
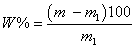
Где m - масса воздушно-сухой
почвы, г; m1 - масса высушенной почвы, г.
2.1 Определение C и органических соединений по Тюрину
Приборы и реактивы:Аналитические весы, Колба коническая
термостойкая на 100 мл.,воронка стеклянная диаметром 3см,бюретка на 25
мл.,пипетка медицинская,фильтровальная бумага, хромовая смесь 0,4н,соль Мора
0,2 н, ФАК 0,2%,KMnO4.
Ход работы:
Взять мелкодисперсную навеску 0,5 г,Поместить в колбу емкостью 100
мл. Затем в колбочки пипеткой прилить по каплям 10 мл 0,4 н р-ра K2Cr2O7
в H2SO4.Осторжно взболтать и поставить на эл.
плитку.Кипятят 5 минут,одновременно проводят холостое кипячение без почвы,
только 10 мл K2Cr2O7.
После кипячения колбы охлаждают. Смывают капли хромовой смеси
дистиллированной водой в колбочку и, добавив 4-5 капель 0,2% р-ра ФАК, титруют
0,2 н соли Мора.Переход окраски из вишнево-фиолетовой в зеленую. Одновременно
проводят холостое титрование. По объему соли Мора, пошедшего на
титрование,определяют колличество хромовой смеси, не израсходованной на
окисление органического вещ-ва почвы. При титровании солью Мора избытка K2Cr2O7
происходит реакция:
6FeO4 (NH4) 2SO4+K2Cr2O7+7H2 SO4=Cr2(SO4)3+3Fe2(SO4)3+6(NH4)2SO4+ K2SO4+7H2O
Содержание углерода вычисляют по формуле:
C%=((Vхол-Vраб)*N*0.003*100)/a ,
Где Vхол-объем соли Мора(мл) пошедший на титрование 10
мл K2Cr2O7.
2.2 Определение фенола в почве
Приборы и реактивы: п-нитроаналин,NaNo2(1н), Н2SО4(разбавл),
Na2CO3(2н), смесь: уксуская кислота- бутанол- вода
(3:5:2)
Ход работы:
Растворяют 5г фенола в дистиллированной воде , разбавляют до
1л.Отбирают 1мл этого раствора , содержащий 5 мл фенола , вносим в делительную
воронку, прибавляем 1 мл H2SО4, 25 мл Na2СО3,
2,5 мл п-нитроаналина. Затем прибавляем еще 50 мл H2SО4 и
экстрагируют краситель 50 мл хлорбензола. Бензольный экстракт фильтруют в 50 мл
колбу и доводят до метки чистым хлорбензолом (0,1 мл фенола содержит).
Далее вносим на покрытое смесью стекло, следующие концентрации:
5,0; 10,0; 20,0; 70,0; и Х мкг. Помещаем пластинку в хроматографическую камеру.
Пятна фенола (розово-сиреневого цвета) появляются на расстоянии 1-15 см от
стартовой линии.(Rf=0.1).
Каждое пятно экстрагируют изопропанольной смесью и измеряют
оптическую плотность экстрактов при λ=540нм.
По градуировочному графику находят содержание фенола.
2.3 Определение общей щелочности и щелочности, обусловленной
карбонат-ионами
Навеску почвы массой 40,0 г помещают в сухую колбу или другую
емкость вместимостью 250 мл. К почве с помощью мерного цилиндра приливают 100
мл. 1 М раствора KCl. Содержимое
колбы взбалтывают 1 час и фильтруют через складчатый фильтр в сухую коническую
колбу. Чтобы получить прозрачные фильтраты, на фильтр переносят как можно
больше почвы. Первые порции фильтрата могут опалесцировать, их
перефильтровывают. Вытяжка должна быть прозрачной.
В полученной 1 М KCl-вытяжке
определяют концентрацию карбонат-ионов. Для этого из мерной колбы в коническую
колбу для титрования вместимостью 100 мл прибавляют 25 мл аликвоты раствора и
несколько капель фенолфталеина. Титруют 0,01 М раствором H2SO4
до обесцвечивания розовой окраски раствора. Записывают объем титранта V1, пошедший на титрование.
Далее определяют общую щелочность. Для этого из мерной колбы в
коническую колбу для титрования вместимостью 100 мл прибавляют 25 мл аликвоты
раствора и несколько капель метилового-оранжевого. Титруют 0,01 М раствором H2SO4
до изменения окраски раствора из желтой в оранжевую. Записывают объем титранта V2, пошедший на титрование.
Концентрацию карбонат-ионов и общую щелочность вычисляют по
формулам:
= ;
;
где н - нормальность кислоты; Vа
- объем аликвоты, мл; V0
- объем, добавленный к навеске почвы, мл; m
- навеска почвы, г.
2.4 Методика комплексонометрического определения валового
содержания железа в почвах
На конических колбах вместимостью 250 мл делают отметку на уровне,
соответствующем объему 50 мл. В колбу помещают 25 мл фильтрата, полученного
после отделения кремниевой кислоты, добавляют 5-7 капель концентрированной
азотной кислоты и нагревают до кипения, окисляя Fe(II).
Затем в колбу добавляют 10-15 капель 25%-ного раствора аммиака,
помещают кусочек индикаторной бумаги Конго-рот и добавляют по каплям сначала
25%-ный раствор аммиака, а затем 10%-ный до перехода синей окраски индикаторной
бумаги в бурую. Если при этом выпадет осадок, его растворяют несколькими
каплями 1 н. HCl. В колбу приливают 5 мл 1 н. HCl,
и объем жидкости дистиллированной водой доводят до отметки, соответствующей 50
мл. Содержимое колбы нагревают до 50-60 °С, добавляют 1-3 капли 10%-ного
раствора сульфосалициловой кислоты и титруют 0,01 М раствором комплексона III до перехода лиловой окраски сульфосалицилата железа в
бледно-желтую комплексоната железа. Скорость реакции невелика, поэтому
последние порции титранта добавляют медленно. Если в этой же порции
анализируемого раствора будет определяться алюминий, нельзя добавлять избытка
титранта.
2.5 Определение кальция и магния при совместном присутствии
Константы устойчивости этилендиаминтетраацетатов кальция и магния
различаются на 2 порядка. Поэтому эти ионы нельзя оттитровать раздельно,
используя только различие в константах устойчивости комплексонатов. При pHопт ~ 10 в качестве металлоиндикаторов используют эриохромовый черный
Т. При этих условиях определяют сумму кальция и магния. В другой аликвотной
части создают pH > 12, вводя NaOH,
при этом магний осаждается в виде гидроксида, его не отфильтровывают, и в
растворе определяют комплексонометрический кальций в присутствии мурексида,
флуорексона или кальциона, являющихся металлоиндикаторами на кальций. Магний
определяют по разности.
Выполнение определения.
1.
Определение суммы кальция и магния.
Отбирают пипеткой 10 мл
анализируемого раствора (водной вытяжки почвы) из мерной колбы вместимостью 100
мл в коническую колбу для титрования вместимостью 100 мл, прибавляют 2-3 мл
буферного раствора с pH 10, 15 мл воды, перемешивают и прибавляют на кончике шпателя
20-30 мг смеси эриохромового черного Т и хлорида натрия. Перемешивают до
полного растворения индикаторной смеси и титруют раствором ЭДТА до изменения
окраски раствора из винно-красной в голубую.
2.
Определение кальция.
Отбирают пипеткой 10 мл
анализируемого раствора (водной вытяжки почвы) в коническую колбу для
титрования вместимостью 100 мл, прибавляют 2-3 мл раствора NaOH или KOH, разбавляют водой
примерно до 25 мл, вводят 20-30 мг индикаторной смеси мурексида, флуорексона,
или кальциона с хлоридом натрия и титруют раствором ЭДТА до изменения окраски
раствора от одной капли раствора ЭДТА.
Изменение окраски в конечной точке
титрования зависит от выбранного металлоиндикатора. При использовании мурексида
окраска изменяется из розовой в фиолетовую; при использовании флуорексона - из
желтой с зеленой флуоресценцией в бесцветную или розовую с резким уменьшением
интенсивности флуоресценции; при использовании кальциона - из бледно-желтой в
оранжевую. В последнем случае щелочную среду создают только 2 М раствором KOH.
3.
Определение магния. Объем титранта, израсходованный на титрование
магния, вычисляют по разности объемов ЭДТА, пошедшей на титрование при pH 10 и при pH 12.
2.6 Методика определения
обменной кислотности
Навеску почвы, пропущенной через
сито с отверстиями диаметром 1-2 мм, массой 40 г помещают в колбу вместимостью
250 мл. В колбу приливают 100 мл 1М раствора KCl и взбалтывают в течение
1 ч. Часовое взбалтывание суспензии может быть заменено трехминутным
взбалтыванием с последующим суточным настаиванием. Содержимое колбы фильтруют в
сухую коническую колбу или другую емкость. Первые 10 мл фильтрата выбрасывают.
После того, как суспензия будет
профильтрована полностью, 50 мл фильтрата помещают в коническую колбу
вместимостью 250 мл, добавляют 2-3 капли фенолфталеина и титруют 0,02-0,1М
раствором NaOH до появления розовой окраски, не исчезающей в течение 1 мин.
Обменную кислотность (Ноб)
рассчитывают по уравнению:
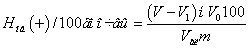
Где V и V1 - объем NaOH,
пошедший на титрование соответственно аликвоты вытяжки и контрольной пробы; н -
молярная концентрация NaOH,
ммоль/мл; Vал и V0
- объем аликвоты вытяжки и общий объем добавленного к почве 1М KCl, мл; m - навеска почвы, г.
Реагенты:
1М раствор KCl
растворяют в 300-400 мл дистиллированной воды, раствор фильтруют и объем
доводят до 1 л. Значение рН раствора соответствует 5,6-6,0 (рН дистиллированной
воды, находящейся в равновесии с СО2 атмосферного воздуха, имеет рН
около 5,6).
2.7 Методика определения гидролитической кислотности
В сухую колбу вместимостью 250 мл помещают навеску почвы,
пропущенной через сито с отверстиями диаметром 1 мм, массой 40,0 г. В колбу
приливают 100 мл 1М раствора СН3СООNa
и взбалтывают в течение часа. Часовое взбалтывание может быть заменено 3
минутным с последующим 18-20 часовым настаиванием с периодическим (4-5 раз)
взбалтыванием суспензии. Суспензию взбалтывают круговыми движениями и фильтруют
через сухой складчатый фильтр. Первые порции (около 10 мл) фильтрата
выбрасывают. Если затем при фильтровании получают мутный раствор, его
перефильтровывают. Аликвоту фильтрата 50 мл помещают в коническую колбу
вместимостью 250 мл, добавляют 2-3 капли фенолфталеина и титруют 0,02-0,1 н
раствором NaOH до слабо-розовой окраски, не исчезающей в течение 1 мин.
Гидролитическую кислотность рассчитывают по уравнению:
Нг моль(+)/100 г почвы = [VнV0100]/[Vалm],
Где V и н - объем и
концентрация раствора NaOH,
ммоль/мл; Vал - объем аликвоты вытяжки, мл; V0
- объем добавленного к навеске почвы раствора ацетата натрия, мл; m - навеска почвы, г. Если полученный результат умножают на 1,75
для компенсации неполного извлечения из почв кислотных компонентов при
однократной обработке почвы экстрагирующим раствором, в комментарии к
результатам анализа делают соответствующую оговорку.
Реагенты:
1М раствор СН3СООNa
с рН 8,3. Навеску ацетата натрия 82,0 г СН3СООNa или 136,0 г СН3СООNax3Н2О
растворяют в дистиллированной воде ,(если необходимо, фильтруют), доводят объем
до 1 л и измеряют рН. Величину рН доводят до 8,3 растворами СН3СООNa или NaOH с массовой долей
10%. Контроль рН раствора может быть осуществлен с помощью фенолфталеина.
Раствор ацетата натрия при добавлении фенолфталеина должен иметь слабо-розовую
окраску.
2.8 Методика определения концентрации фосфатов в 0,03 н. K2SO4-вытяжках
(по Карпинскому - Замятиной)
Навеску почвы массой 20,0 г помещают в сухую колбу или другую
емкость вместимостью 250 мл. К почве с помощью мерного цилиндра приливают 100
мл. 0,03 н. раствора K2SO4. Содержимое колбы взбалтывают 5 мин и фильтруют через складчатый
фильтр в сухую коническую колбу. Чтобы получить прозрачные фильтраты, на фильтр
переносят как можно больше почвы. Первые порции фильтрата могут опалесцировать,
их перефильтровывают. Вытяжка должна быть прозрачной.В полученной 0,03 н. K2SO4-вытяжке
определяют концентрацию фосфатов. Для этого в мерную колбу вместимостью 50 мл.
помещают 20-40 мл. вытяжки. В колбу добавляют 8 мл. реагента Б. Объем жидкости
в колбе доводят дистиллированной водой до метки, тщательно перемешивают и через
10 мин. Измеряют оптическую плотность раствора при длине волны 630-882 нм.
Перед окрашиванием анализируемого раствора необходимо приготовить
шкалу стандартных растворов для получения градуировочной кривой. С этой целью в
мерные колбы вместимостью 50 мл. приливают по 2 мл. 0,6 н. K2SO4,
что обеспечит концентрацию сульфата калия в находящемся в колбе растворе
приблизительно такую же, какую получают при анализе 40 мл K2SO4-вытяжки.
Затем в каждую из колб с помощью бюретки приливают стандартный раствор с
содержанием фосфора 0,005 мг P
в 1 мл. В колбы добавляют 0,5; 1,0; 3,0; 5,0; 7,0 и 10,0 мл стандартного
раствора. В колбы приливают дистиллированную воду приблизительно до объема 35 -
40 мл, реагент Б. Содержимое колб тщательно перемешивают, через 10 мин измеряют
оптическую плотность и строят градуировочную кривую в координатах: оптическая
плотность - количество фосфора в мерной колбе. По градуировочной кривой находят
концентрацию фосфора в анализируемых растворах. Результаты анализа выражают в
мг/л:
P,
мг/л = Cp1000/Vал,
где Vал
- объем аликвоты вытяжки, мл; Сp
- число миллиграммов фосфора в мерной колбе, мг/объем мерной колбы.
3
Экспериментальная часть
В экспериментальной части проводился анализ почвы. Почва была
отобрана в Усманском районе, Липецкой области. Проба отбиралась с глубины около
20 см, масса пробы составила 0,5 кг.
3.1 Определение гигроскопической влаги
1. Таблица полученных результатов:
|
Масса бюкса, г
|
Масса бюкса с почвой, г
|
Масса почвы m, г
|
Масса бюкса после сушки, г
|
Масса высушенной почвы m1, г
|
Гигроскопическая влага, %
|
|
27,54575
|
29,21100
|
1,66255
|
30,12541
|
1,21441
|
36,90
|
|
33,18410
|
35,38934
|
2,205240
|
36,54123
|
1,65181
|
33,50
|
|
41,38525
|
44,54641
|
3,16116
|
45,65941
|
2,29531
|
35,40
|
ωср, % = 35,30%
2. Статистическая обработка данных.
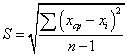 -
стандартное отклонение
-
стандартное отклонение
1.394
Sr = S/xср - относительное стандартное отклонение
Sr = 1.394/35.3
= 0.039
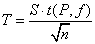
ω∆ω = (35.303.46) %.
3.2 Определение C и органических соединений по Тюрину
Vхол =40 мл
Vраб=10 мл
а=0,5 г
С%=(30*0,2*0,003*100)/0,5=3,6%
2. Определение фенола
Таблица полученных результатов
|
Сфенола мкг/мл
|
Аоптическая плотность
|
|
5
|
0.07
|
|
23
|
0.148
|
|
42.7
|
0.254
|
|
70
|
0.338
|
|
х
|
0.160
|
Градуировочный график
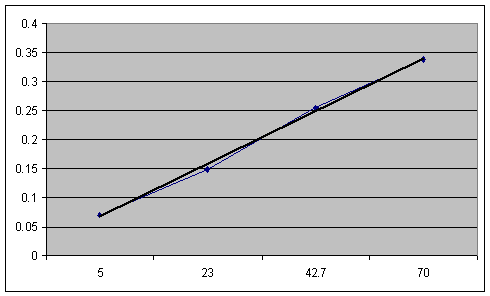
Из графика видно, что
|
№
|
Ах
|
Сх, мкг/мл
|
|
1
|
0,160
|
38
|
|
2
|
0,180
|
40
|
|
3
|
0,190
|
43
|
|
ср
|
0,176
|
40
|
Статистическая обработка данных.
S==2,08
Sr = 2,08/40 = 0,052
С∆С = (400,5)мкг/мл
Пересчитаем концентрацию: С=0,02г/20г почвы
3.3 Определение общей щелочности и щелочности, обусловленной
карбонат-ионами
1. Таблица полученных результатов:
|
№ п/п
|
Масса навески, г
|
Объем вытяжки, мл
|
Объем титранта 0,01 М H2SO4, мл
|
|
|
общий
|
аликвота
|
По ф/ф
|
По м/о
|
|
1
|
40
|
100
|
25
|
1,01
|
7,3
|
|
2
|
|
|
|
1,02
|
7,8
|
|
3
|
|
|
|
1,04
|
8,0
|
|
ср
|
|
|
|
1,03
|
7,9
|
2. Карбонатная щелочность.
;
0.404ммоль/100г, почвы
0,408ммоль/100 г почвы
0,416 ммоль/100г почвы
ммоль/100 г почвы
0,404*0,03*100=1,212%
0,408*0,03*100=1,44%
0,416*0,03*100=1,248%
=1,301
Статистическая обработка данных.
S==0,0031
Sr = 0,0031/0,409 = 0,006
С∆С = (0,4090,024)ммоль/100г почвы.
3.4 Общая щелочность
ОЩ1==1,662 ммоль/100г почвы
ОЩ2==1,764 ммоль/100г почвы
ОЩ3=1,808ммоль/100г почвы
ОЩср=1,745 ммоль/100г почвы
=1,662*0,061*100=10,14%
=1,764*0,061*100=10,76%;
=1,808*0,061*100=11,03%;
=1,745*0,061*100=10,65%.
Статистическая обработка данных.
S=0.06
Sr = 0,06/1,808 = 0,033
Т==0,14
С∆С = (1,8080,14) ммоль/100г почвы.
3.5 Валовое
содержание железа
1.
Таблица полученных результатов:
|
№п/п
|
Навеска почвы, г
|
Объем аликвоты, мл
|
Объем титранта, мл
|
|
1
|
20
|
25
|
12,0
|
|
2
|
|
|
11,5
|
|
3
|
|
|
12,0
|
|
ср
|
|
|
11,8
|
=0,0040н
=0,0038н
=0,0042н
=0,004н
С учетом разбавления:
С1 = 0,0080 моль/л
С2 = 0,0076 моль/л
С3= 0,0084 моль/л
Сср = 0,0080 моль/л.
mFe3+
= 0,0080·56·0,1 = 0,0448 г.
ω, %==0,224%
2. Статистическая обработка данных.
S==0,002
Sr = 0,002/0,0080 = 0,25
Т==0,004
С∆С = (0,00800,004)моль/л.
3.6 Определение кальция и магния при совместном присутствии
1. Определение суммы кальция и магния
СТ = 0,1 моль-экв/л
Vал
= 10 мл

|
№ опыта
|
Vт, мл
|
С∑ моль экв/л
|
|
1
|
2,05
|
0,0205
|
|
2
|
2,10
|
0,0210
|
|
3
|
1,95
|
0,0195
|
|
ср
|
2,03
|
0,0203
|
Статистическая обработка результатов
S==0,00026
Sr
= 0,00026/0,0203 = 0,0128
Т==0,00061
Ср ср±ΔC=(0,02030
± 0,00061)ммоль экв/мл
m∑
= 0,056 + 0,0128 = 0,069
ω%=0,203%
2. Определение кальция
Vал
= 10 мл
Ст = 0,1 моль экв/л
|
№ опыта
|
Vт, мл
|
СCa2+ моль экв/л
|
|
1
|
1,38
|
0,0138
|
|
2
|
1,36
|
0,0136
|
|
3
|
1,32
|
0,0132
|
|
ср
|
1,36
|
0,0136
|
Статистическая обработка результатов
S==0,0015
Sr
= 0,0015/0,0136 = 0,11
Т==0,0037
Ср ср ± ΔC
= (0,0136 ± 0,0037)ммоль экв/мл
ω%=mCa/ mн
mCa
= 0.0136·40·0.1 = 0,0544 г
ω%=0,19%
3.Определение магния
Vал = 10 мл
Ст = 0,1 моль экв/л
|
№ опытаVт, млСMg2+ моль экв/л
|
|
|
|
1
|
0,71
|
0,0071
|
|
2
|
0,73
|
|
3
|
0,74
|
0,0074
|
|
ср
|
0,72
|
0,0072
|
Статистическая обработка результатов
S==0.00024
Sr=0,00024/0,0072
= 0,033
Т==0.00054
Ср ср ± ΔC
= (0,0072 ± 0,00054)ммоль экв/мл
mMg
= 0,0072·24·0,1 = 0,01761 г
ω%=0,071%
3.7 Определение обменной кислотности
1. Таблица полученных данных
|
№ п/п
|
Vт
|
Vал
|
mнав
|
V0
|
Ноб,ммоль(+)/100г почвы
|
|
1
|
2,7
|
50
|
40
|
100
|
1,47
|
|
2
|
2,73
|
|
|
|
1,43
|
|
3
|
2,67
|
|
|
|
1,32
|
|
Cр
|
2,69
|
|
|
|
1,40
|
2. Статистическая обработка
результатов
S==0,03
Sr=0,03/1,40
= 0,028
Т==0.02
Ср ср±ΔC=(1,40±0,020)ммоль/100
г почвы
3.8 Определение концентрации фосфатов в 0,03 н. K2SO4-вытяжках
(по Карпинскому - Замятиной)
1. Построение градуировочного графика.
График: оптическая плотность - объем аликвоты.
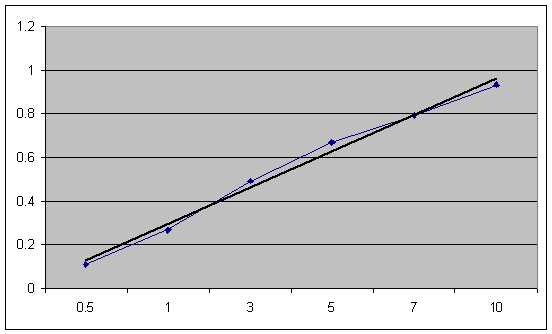
|
Vал
|
Оптическая плотность, Аср
|
|
0.5
|
0.11
|
|
1
|
0.27
|
|
3
|
0.49
|
|
5
|
0.67
|
|
7
|
0.79
|
|
10
|
0.93
|
|
х
|
0,53
|
С1 == 3,25 мг/100 г;
С2 = =3,27 мг/100 г;
С3 = =3,29 мг/100 г.
Сср = 3,27 мг/100 г = 3,27·10-3 г/100 г
ω%=(
Ср ср/10)·100% = 0,0327%
2. Статистическая обработка результатов
S==0,016
Sr=0,016/3,27
= 0,048
Т==0,039
Ср ср±ΔC=(3,27±0,039)мг/100
г
3.9
Определение гидролитической кислотности
1. Таблица полученных результатов
|
№ опыта
|
Vт
|
Vал
|
mнав
|
V0
|
Нгидрммоль(+)/100г почвы
|
|
1
|
1,17
|
50
|
40
|
100
|
0,61
|
|
2
|
1,22
|
|
|
|
0,56
|
|
3
|
1,19
|
|
|
|
0,51
|
|
Cр
|
1,19
|
|
|
|
0,51
|
2. Статистическая обработка
результатов
S==0,018
Sr=0,018/0,51
= 0,02
Т==0.059
Ср ср±ΔC=(0,51±0,059)ммоль/100
г почвы.
3.10 Определение нитрат ионов в почве с использованием нитрат селективного
электрода
Результаты определений занесены в таблицу:
|
С, моль/л
|
Е, В
|
-lg C
|
|
0,1
|
306.0
|
1
|
|
0,01
|
357.7
|
2
|
|
0,001
|
413.8
|
3
|
|
0,0001
|
462.6
|
4
|
По результатам построен график 1.
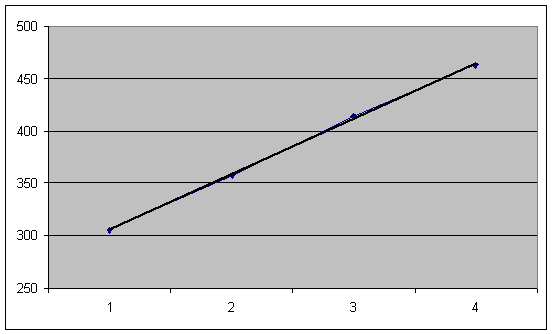
Концентрации найденные по
градуировочному графику приведены в таблице:
|
№ определения
|
Е, В
|
-lg C
|
С, моль/л
|
|
1
|
457,2
|
3,86
|
0,000138
|
|
2
|
457,5
|
3,88
|
0,000132
|
|
3
|
455,7
|
3,87
|
0,000135
|
|
ср
|
455,7
|
3,87
|
0,000135
|
Статистическая обработка результатов
S==0,00006
Sr=0,00006/0,000135
= 0,04
Т==0.009
Ср ср±ΔC=(0,000135±0,009)ммоль/100
г почвы.
Пересчитаем концентрацию:
с = сNO3 *14*105/1-(w/100)
С=0,000135*15/1-(35,3/100)=0,034мг/кг
Заключение
В ходе данной работы был
проанализирован образец почвы, отобранный в Усманском районе Липецкой области.
Полученные результаты представлены в таблице:
|
Определяемый показатель
|
Содержание в образце почвы
|
Определяемый показатель
|
Содержание в образце почвы
|
|
Гигроскопическая влага
|
35,3%
|
Содержание кальция и магния
|
0,203%
|
|
Содержание фенола
|
0,02г/20г почвы
|
Содержание кальция
|
0,19%
|
|
Карбонатная щелочность
|
0,409ммоль/100г почвы
|
Содержание магния
|
0,071%
|
|
Общая щелочность
|
1,808ммоль/100г почвы
|
Гидролитическая кислотность
|
1,40/100г почвы
|
|
Содержание железа
|
0,224%
|
Обменная кислотность
|
0,51 ммоль/100г почвы
|
|
Содержание фосфатов
|
0,0327%
|
Содержание углерода
|
3,6%
|
Библиографический список
1 Химический анализ
почв/ Воробьева Л.А. - М.: изд. МГУ, 1998. - 272с.: ил.
2 Эколого-аналитический
мониторинг стойких органических загрязнителей/ Майстренко В.Н., Клюев Н.А. -
М.: Мир: БИНОМ. Лаборатория знаний, 2004. -323с.: ил.
3 Основы аналитической
химии. Практическое руководство: уч. Пособие для ВУЗов/ Фадеева В.И., Шеховцова
Т.Н., Иванов В.М. и др.; под ред. Золотова Ю.А. - М.: Высшая школа, 2001. -
463с: ил.
4 Агрохимические
исследования почв/Под ред. А.В.Соколова. М.: Наука, 1975. 98 с.
5 Учебно-полевая
практика и лабораторные работы,методическое пособие/Дербенцева А.М.,Пилипушка
В.Н.-Владивосток,2005.-24с.
6 Практикум по
агрохимии/Под ред. МинееваВ.Г. М.:Изд-во МГУ,2001.-689 с.