Материальный баланс холодильника-конденсатора
1. Исходные данные для
расчета
1.
В
холодильник-конденсатор поступает 5000 нм³/ч нитрозных газов.
2.
Состав газа на
входе, %об.: NO – 2, NO2 – 8,35, O2 –
1,92, N2 – 70,80, Н2О – 16,93.
3.
Давление в
системе 7,5 атм.
4.
Степень
превращения окислов азота при абсорбции – 0,98.
5.
В расчете
теплового баланса определить количество охлаждающей воды.
6.
Температура
нитрозного газа на входе в холодильник – конденсатор – 160ºС.
7.
Температура
нитрозного газа на выходе из холодильника–конденсатора – 40ºС.
8.
Степень
конденсации водяных паров – 90 %.
2. Материальный баланс
холодильника-конденсатора
Цель материального
баланса: определение состава нитрозного газа после холодильника-конденсатора.
Таблица 1. Состав нитрозных
газов, поступающих в холодильник-конденсатор
|
Состав
|
м3/ч
|
кг/ч
|
кмоль/ч
|
% (об.)
|
|
NO
|
100
|
133,8
|
4,46
|
2
|
|
NO2
|
417,5
|
857,44
|
18,64
|
8,35
|
|
O2
|
96
|
137,152
|
4,286
|
1,92
|
|
N2
|
3540
|
4425,008
|
158,036
|
70,80
|
|
H2O
|
846,5
|
680,22
|
37,79
|
16,93
|
|
Всего
|
5000
|
6233,62
|
223,212
|
100
|
В холодильнике –
конденсаторе образуется конденсат, содержащий 40%-ную HNO3 , что соответствует степени превращения окислов азота
25 %.
Условно пересчитываем
окислы азота, содержащиеся в нитрозном газе, на NO2:
(NO+ NO2)=4,46+18,64=23,1 кмоль/ч
1. Количество конденсата.
Количество двуокиси
азота, превращенной в азотную кислоту, составит:
23,1*0,25=5,775 кмоль/ч
На образование азотной
кислоты по реакции
4 NO2 + O2 +2Н2О = 4HNO3 - 73600 кДж
расходуется воды: 5,775 /
2 = 2,887 кмоль/ч.
Количество
сконденсировавшейся воды x,
пошедшей на образование 40%-ной HNO3 , можно
вычислить по уравнению:
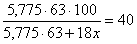
36382,5=14553+720x
x= 30,32 кмоль/ч
Всего сконденсировалось
воды:
2,887 + 30,32 = 33,21
кмоль/ч
В газе осталось водяных
паров:
37,79 – 33,21 =4,58 кмоль/ч
Количество образовавшейся
40%-ной HNO3 :
5,775 + 30,32 = 36,095
кмоль/ч
2. Количество и состав
газа после холодильника.
На образование HNO3 пошло кислорода:
5,775*0,25 = 1,444 кмоль/ч
В газе осталось:
4,286 - 1,444=2,842 кмоль/ч
окислов азота
23,1 – 5,775=17,325 кмоль/ч
Таблица 2. Состав
нитрозных газов, выходящих из холодильника-конденсатора
|
Состав
|
м3/ч
|
кг/ч
|
кмоль/ч
|
% (об.)
|
|
NO
|
99,904
|
133,8
|
4,46
|
2,44
|
|
NO2
|
288,176
|
591,79
|
12,865
|
7,04
|
|
O2
|
63,661
|
90,944
|
2,842
|
1,55
|
|
N2
|
3540,006
|
4425,008
|
158,036
|
86,46
|
|
H2O
|
102,592
|
82,44
|
4,58
|
2,51
|
|
Всего
|
4094,339
|
5323,982
|
182,783
|
100
|
Таблица 3. Состав
конденсата
|
Состав
|
м3/ч
|
кг/ч
|
кмоль/ч
|
%(об.)
|
|
HNO3
|
129,36
|
363,825
|
2,05
|
39,99
|
|
H2O
|
679,17
|
545,76
|
37,73
|
60,01
|
|
Всего
|
808,53
|
909,585
|
39,78
|
100
|
3. Сводный материальный баланс
холодильника–конденсатора
Таблица 4.
|
ПРИХОД
|
РАСХОД
|
|
В-во
|
м3/ч
|
кг/ч
|
кмоль/ч
|
%(об.)
|
В-во
|
кг/ч
|
кмоль/ч
|
%(об.)
|
|
NO
|
100
|
133,8
|
4,46
|
2
|
NO
|
99,904
|
133,8
|
4,46
|
2,01
|
|
NO2
|
417,5
|
857,44
|
18,64
|
8,35
|
NO2
|
288,176
|
591,79
|
12,865
|
5,78
|
|
O2
|
96
|
137,152
|
4,286
|
1,92
|
O2
|
63,661
|
90,944
|
2,842
|
1,28
|
|
N2
|
3540
|
4425,01
|
158,036
|
70,80
|
N2
|
3540,01
|
4425,01
|
158,04
|
71,06
|
|
H2O
|
846,5
|
680,22
|
37,79
|
16,93
|
H2O
|
102,592
|
82,44
|
4,58
|
2,06
|
|
|
|
|
|
H2O
конд-ат
|
679,17
|
545,76
|
37,73
|
16,96
|
|
|
|
|
|
HNO3
конд-ат
|
129,36
|
363,825
|
2,05
|
0,92
|
|
Всего
|
5000
|
6233,62
|
223,212
|
100
|
4902,873
|
6233,57
|
222,39
|
100
|
Неувязка материального баланса составляет:

Она не превышает 1 %,
соответственно материальный баланс рассчитан верно.
Тепловой баланс
холодильника – конденсатора
Цель теплового баланса:
расчёт тепловых потоков.
1.
Теплоту,
приносимую с нитрозным газом, находим по формуле,
 ,
,
где ni – количество вещества исходных
реагентов, кмоль/ч (материальный баланс);
ci – средняя удельная теплоемкость
компонентов, кДж / (кмоль К);
tвх,i – температура входного потока,
ºС.
Находим среднюю
теплоёмкость компонентов нитрозного газа по формулам:

 кДж / (кмоль К)
кДж / (кмоль К)

 кДж / (кмоль К)
кДж / (кмоль К)
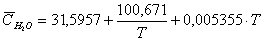
 кДж / (кмоль К)
кДж / (кмоль К)

 кДж / (кмоль К)
кДж / (кмоль К)

 кДж / (кмоль К)
кДж / (кмоль К)
Таблица 3. Средняя теплоёмкость нитрозного газа
|
Компоненты
|
Теплоёмкость, 
|
|
NО
|
30,53
|
|
N2
|
29,44
|
|
NO2
|
39,86
|
|
O2
|
29,78
|
|
H2O
|
34,15
|
Рассчитаем среднюю
теплоёмкость нитрозного газа по правилу аддитивности:
 ;
;

 .
.
Q1 =223,212*31,136*160 = 1111988,613 кДж/ч = 308,89 кВт.
2.
Теплоту,
поступающую за счет конденсации паров воды, определяем как:
Q2 = (2780 – 4,18*40) 33,21*18 = 1561879,584 кДж/ч =
433,85 кВт.
где 2780 кДж / кг –
теплота конденсации водяного пара.
3. Теплоту при образовании азотной
кислоты находим по формуле, кДж:
 ,
,
где q – теплота образования безводной HNO3 (по реакции), кДж; q=73600 кДж;
m – количество образовавшейся кислоты,
кмоль/ч.( материальный баланс)
Q3 =  кДж/ч = 29,52 кВт.
кДж/ч = 29,52 кВт.
Теплота, выделяющаяся при
разбавлении безводной кислоты до 40%-ной HNO3:
Q4 = 28400 * 5,775 = 164010 кДж/ч = 45,56 кВт.
где 28400 – теплота
разбавления азотной кислоты, кДж / моль.
Теплоту, отводимую
нитрозным газом из конденсатора, находим по формуле, кДж:

где nj – количество вещества продуктов
реакции, кг/ч, (материальный баланс); cj – средняя удельная теплоемкость компонентов, кДж / (кмоль
К);
tкон,j – температура выходного потока,
ºС.
 кДж / (кмоль К)
кДж / (кмоль К)
 кДж / (кмоль К)
кДж / (кмоль К)
 кДж / (кмоль К)
кДж / (кмоль К)
 кДж / (кмоль К)
кДж / (кмоль К)
 кДж / (кмоль К)
кДж / (кмоль К)
Таблица 3. Средняя теплоёмкость нитрозного газа
|
Компоненты
|
Теплоёмкость, 
|
|
NО
|
30,12
|
|
N2
|
29,18
|
37,09
|
|
O2
|
28,45
|
|
H2O
|
33,59
|

 .
.
Q5 =182,787*29,859*40 = 218313,481 кДж/ч = 60,64 кВт.
Теплоту, отводимую с
кислотой из холодильника – конденсатора находим как:
Q6 =  кДж/ч = 30,73 кВт.
кДж/ч = 30,73 кВт.
[3,041 – теплоемкость
40%-ной HNO3 при 40 ºС, кДж / (кг К)].
По разности между
количествами приходящей и расходуемой теплоты определяем теплоту, отводимую
охлаждающей водой:
Q7 = (308,89 + 433,85 + 29,52 + 45,56) – (60,64 + 30,73)
= 726,45 кВт.
Таблица 5. Тепловой баланс
холодильника–конденсатора
|
ПРИХОД
|
РАСХОД
|
|
Поток
|
кВт
|
%
|
Поток
|
кВт
|
%
|
|
Q1
|
308,89
|
37,77
|
Q5
|
60,64
|
7,41
|
|
Q2
|
433,85
|
53,05
|
Q6
|
30,73
|
3,76
|
|
Q3
|
29,52
|
3,61
|
Q7
|
726,45
|
88,83
|
|
Q4
|
45,56
|
5,57
|
|
|
|
|
Всего
|
817,82
|
100
|
Всего
|
817,82
|
100
|