Методические разработки урока по теме "Спирты"
ВВЕДЕНИЕ
Получение этанола — одно из крупнотоннажных промышленных
производств основного (тяжелого) органического синтеза. При его изучении можно
проследить основные тенденции технического прогресса в химической
промышленности. Большие масштабы производства этанола предъявляют определенные
требования к экономике производства, в первую очередь в решении проблемы выбора
сырья (в себестоимости химической продукции доля сырья достигает 70 %) и
рационального оформления технологического процесса. Кроме того, эти требования
направлены на сокращение числа стадий производства; укрупнение единичных
Мощностей аппаратов и установок в целом; повышение комплексности использования
сырья; создание малоотходных технологических процессов; обеспечение необходимых
мер по охране окружающей среды; максимальное внедрение на всех стадиях
производства АСУ.
ГЛАВА 1. ПРОИЗВОДСТВО
ЭТАНОЛА ФЕРМЕНТАЦИЕЙ БИОМАССЫ
Получение
этанола. Обычно
этанол получают отгонкой, и, по всей вероятности, этот способ будет применяться
и в ближайшем будущем. Отгонка производится в колоннах путем последовательного
отделения этанола от других компонентов жидкой фазы.
Отделение
барды. В первой колонне отделяются продукты ферментации (главным образом
этанол) и некоторое количество воды от неферменти-рующихся твердых веществ в
жидкой фазе (барде). Эта колонна обычно называется «пивным перегонным кубом».
Желательно, чтобы на этом этапе из жидкой среды был отогнан весь этанол. В
некоторых конструкциях колонн возможно увеличение концентрации этанола в
верхнем погоне путем ректификации. Для отделения твердых веществ из жидкой
фазы, движущейся вниз, предусмотрена отпарная секция.
Производство
безводного этанола. Последовательность перегонки после «пивного перегонного куба»
зависит от требований, предъявляемых к этанолу. При производстве пищевого
этанола последний должен быть очищен в соответствии с требованиями спецификаций
на этанол или продукт, в котором он будет использован. При производстве этанола
промышленного назначения необходимо удалить из него все загрязняющие вещества,
в том числе сивушные масла, которые являются побочными продуктами ферментации.
При получении безводного к очищенному продукту добавляют вещества, разрушающие
водно-этанольную азеотропную смесь. Этанол и азотообразующую компоненту
отделяют друг от друга в следующей колонне. В стандартных условиях для
производства безводного этанола требуется по крайней мере четырехкратная
перегонка.
Этанол,
предназначенный для использования в качестве топлива, не должен содержать воду
[8]. Вместе с тем предполагается, что из такого этанола нет необходимости
отделять сивушные масла. Поэтому перегонная система для получения этанола,
предназначенного для использования в качестве топлива, включает «пивной
перегонный куб» с ректификацией и колонны для азеотропной перегонки и отпарки.
Спецификации на готовый продукт. Количество энергии, расходуемой на очистку
этанола, определяет числа действующих колонн. В каждой колонне для поддержания
заданного равновесия паров и жидкости над тарелками расходуется значительное
количество тепловой энергии. Поэтому с энергетической точки зрения важное
значение имеет спецификация на готовый продукт. В зависимости от спецификации и
гибкости установки для производства более широкого ассортимента продуктов
эксплуатационные расходы могут возрасти больше или меньше.
Глава 2. ЭКОЛОГИЧЕСКИЕ И
ЭКОНОМИЧЕСКИЕ АСПЕКТЫ ПРОИЗВОДСТВА ЭТАНОЛА
Получение этанола — одно из крупнотоннажных промышленных
производств основного (тяжелого) органического синтеза. При его изучении можно
проследить основные тенденции технического прогресса в химической
промышленности. Большие масштабы производства этанола предъявляют определенные
требования к экономике производства, в первую очередь в решении проблемы выбора
сырья (в себестоимости химической продукции доля сырья достигает 70 %) и
рационального оформления технологического процесса. Кроме того, эти требования
направлены на сокращение числа стадий производства; укрупнение единичных
Мощностей аппаратов и установок в целом; повышение комплексности использования
сырья; создание малоотходных технологических процессов; обеспечение необходимых
мер по охране окружающей среды; максимальное внедрение на всех стадиях
производства АСУ.
Этанол (метилкарбинол, этиловый, винный спирт) известен человеку с
глубокой древности. Первые упоминания о нем относятся к VIII в. В арабских источниках
(950 г.) описано получение водного этанола. В 1050—1150 гг. этанол получали
ректификацией вина, в котором он образуется при брожении глюкозы, и
использовали под названиями «aqua ardens» («вода горючая»), «aqua vitae («вода жизни»), «spiritus vinb («дух вина»). Последний
термин удержался в фармакологии до настоящего времени,
С XIII в. этанол стали применять в медицине под названиями «мать»,
«государыня», «царица всех, лекарств». К 1440 г. относится исследование состава спирто-водных смесей (водки). С 1600 г. этанол используют в химических опытах для
экстракции органических веществ. В книге А. Либавия «Алхимия» (1597) приведен проект
химической лаборатории, в которой предусмотрен «винный погреб».
В 1682 г. И. Бехер впервые описал метод получения водного этанола
(водки) из картофеля, а в 1748 г. он опубликовал сообщение Шведской академии
наук о промышленном способе получения этанола из картофеля. Попытка получить в 1775 г. Т. Бергманом. Впервые безводный этанол получил Т. Е.Ловиц в 1796 г. В 1798 г. А. Арганд описал применение метода ректификации для перегонки этанола. Однако
только в 1820 г. для этой цели была сконструирована промышленная
ректификационная колонна.
В 1783 г. А. Лавуазье установил элементный состав этанола и
попытался объяснить природу спиртового брожения. Окончательно химизм этого
процесса был выяснен в XIX в. Исследование Д. И. Менделеевым в 1864 г. систем «этанол — вода» стало основой для разработки им гидратной (химической) теории
растворов.
До 1934 г. в стране этанол получали исключительно из пищевого
сырья. В 1934 г. было освоено производство этанола гидролизом древесины, а в 1935 г. построен первый гидролизный завод в Ленинграде. С 1930 г. в стране велись работы по получению этанола сернокислотной гидратацией этилене, ив 1936 г, вступил в строй опытный завод в Баку. Поиски технологического решения производства этанола
методом прямой f-идратации этилена были прерваны войной. В 1952 г. поэтому методу началось освоение производства этанола в г. Сумгаите, а в период с 1953 по 1958 г. вошли в строй заводы в Саратове, Уфе, Грозном, Самаре.
В результате этих работ к 1960 г. доля синтетического этанола достигла уже 25 % в общем объеме его производства. В 1988 г. на основе этилена было получено 26,5 дал. этанола, что эквивалентно 2,7 млн. тонн картофеля
или 0,86 млн. тонн зерна. Однако, несмотря на более низкую себестоимость
-синтетического этанола, его доля в общем балансе продукции возрастала
медленно. Так, в 1975 г. в СССР пищевой этанол составлял 60,0%, синтетический —
26,7%, гидролизный — 8,3%, в то время как в США уже в 1970 г. производство синтетического этанола достигло 83 %. С 1964 г. в стране было полностью прекращено использование для технических целей этанола, полученного из пищевого сырья,
что отвечало решению общей задачи по сокращению доли пищевого сырья в сырьевом
балансе химической промышленности.
Разработка промышленных методов производства этанола из этилена и
гидролизом древесины позволила в свое время решить в стране важнейшую
народнохозяйственную задачу по увеличению производства мономеров для
синтетических каучуков (бутадиен-1,3) и переводу производства на дешевое
непищевое сырье. В настоящее время перевод производства бутадиена на углеводородное
сырье (бутана и бутилен-дивинильная фракция продуктов пиролиза) высвобождает
значительное количество синтетического этанола. Его предполагается использовать
как сырье для производства кормовых дрожжей — белковых добавок к кормам, по
качеству значительно превосходящих кормовой белок из парафина, а само
производство не будет столь вредным в экологическом аспекте. В этой связи
экономически целесообразна схема производства, основывающаяся на этане
природного газа, который у нас в настоящее время не находит должного применения
и, как правило, его сжигают. Таким образом, значение технологического процесса
получения синтетического этанола не только сохраняется, но и возрастает, так
как потребность в этом продукте для указанной цели в 5—10 раз превышает уровень
его современного производства.
В связи с этим гидролизные заводы переводят на производство
кормовых дрожжей и производство гидролизного этанола прекращается.' Это в свою
очередь вызывает необходимость вновь использовать часть мощностей по
производству этанола из пищевого сырья для получения спирта высокой чистоты для
специальных технических целей.
Этанол образует с водой азеотропную смесь (95,67 % этанола),
кипящую при 78,15 °С, поэтому получение безводного (абсолютного) этанола
требует специальных методов обезвоживания! Он обладает наркотическим действием
(ПДК=1000 мг/м3).
Этанол относится к числу важнейших продуктов основного
органического синтеза. Это сырье для производства ацетальдегида, хлороформа,
диэтилового эфира, сложных эфиров органических кислот, пищевой уксусной
кислоты, бутадиена, лекарственных препаратов. Его используют в качестве растворителя,
антисептика, компонента моторных топлив, применяют в пищевой и парфюмерной
промышленности. На основе разбавленных растворов этанола разработано производство
кормовых дрожжей методы производства, этанола.
В основу классификации всех существующих промышленных методов производства
этанола могут быть положены виды используемого сырья (углеводородные газы,
древесина, пищевые продукты, отходы производства) и химизм превращений
(гидратация, брожение), лежащих в основе технологических процессов (схема 1).
В соответствии с этой классификацией различают производства
синтетического (I), гидролизного (II), ферментативного (пищевого) (III) и
сульфитного (IV) этанола.
Выход этанола существенно зависит от вида сырья и составляет (в л
на 1 т сырья): для этилена — 740, картофеля -г 93— 117, зерна — 185—361,
мелассы — 270—300, древесины — 160—200, сульфитных щелоков — 90—110 (в расчете
на 1 т древесины). При использовании в качестве сырья древесины и сульфитных щелоков
помимо этанола образуются дрожжи, фурфурол, лигнин и лигниносульфонаты, гипс.
Во всех вариантах биохимического метода производства этанола выделяется оксид углерода
(IV).
В настоящее время синтетический этанол получают исключительно
прямой гидратацией этилена. Метод сернокислотной гидратации сохранил значение
только для производства изопропанола и бутанолов вследствие низкой
экономичности процесса.
Производство
этанола прямой гидратацией этилена
Этилен как сырье в этом методе производства этанола может быть
выделен из пирогаза, полученного пиролизом низкооктанового бензина, из газов
нефтепереработки или попутного газа, из этиленовой фракции обратного коксового
газа (ОКГ), а также получен пиролизом этана (Схема 2).

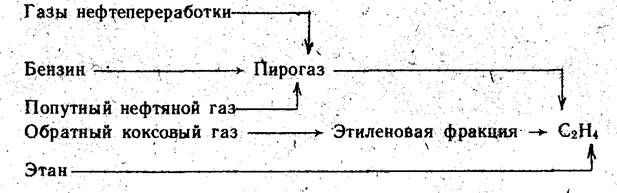
Основную массу этилена в настоящее время получают пиролизом
нефтяного сырья, преимущественно бензина.
Физико-химические основы прямой гидратации этилена;
Из уравнения реакции следует, что равновесный выход этанола
зависит от условий гидратации и растет с понижением температуры, повышением
давления и увеличением мольного отношения воды и этилена.
Процесс
гидратации катализируется кислыми и нейтральными катализаторами, среди которых
наибольшее применение получила фосфорная кислота на носителе в виде кизельгура
или силикагеля. В присутствии фосфорной Кислоты происходит электрофилыюе
присоединение воды к этилену по схеме:
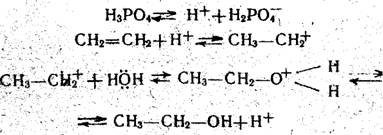
Катализ осуществляется свободной фосфорной кислотой, которая в
жидком состоянии находится на поверхности зерен носителя. Таким образом,
активность катализатора зависит от концентрации кислоты. При концентрации
кислоты ниже. 83% активность катализатора резко падает. В свою очередь,
концентрация кислоты зависит от парциального давления паров воды в системе и
температуры. Поэтому, вопреки, требованиям термодинамики данного процесса, его
нельзя вести при большом мольном отношении воды (пара) и, этилена, так как это
снижает концентрацию кислоты, а следовательно, и активность катализатора. На
практике это отношение' поддерживают в пределах (0,6-0,7):1.
Время работы катализатора — около 500 ч, после чего его активность
падает, так как часть кислоты уносится током продуктов. Это вызывает
необходимость непрерывного добавления фосфорной кислоты в процессе работы
установки. При соблюдении этого условия и применении в качестве сырья газа с
высоким содержанием этилена интенсивность катализатора составляет 180—200 кг
этанола с 1 м3 катализатора в час. В качестве побочных продуктов при
гидратации этилена образуются ацетальдегид, диэтиловый эфир и различные
олигомеры.
Технологическая схема прямой гидратации этилена. В промышленности процесс
гидратации может осуществляться- в двух вариантах: в жидкой и паровой фазах. На
практике реализован, преимущественно второй вариант. В этом случае процесс
ведут при температуре 290 °С и давлении 8 МПа, что позволяет обеспечить степень
конверсии этилена за один проход до 6% при выходе этанола по этилену около 95
%.
Технологический процесс получения этанола прямой гидратацией
этилена в паровой фазе строится по циклической схеме. В ней', предусмотрены
приготовление, парогазовой смеси (этилен и водяной пар), пополнение потерь
катализатора, нейтрализация уносимой с газовым потоком фосфорной кислоты,
периодическая отдувка циркуляционного газа для удаления из него примесей и
рациональный теплообмен с использованием теплоты реакции гидратации.
Парогазовую смесь готовят совместным нагреванием паров воды и
этилена в теплообменниках и трубчатой печи или смешением этилена с перегретым
паром высокого давления.
В промышленном масштабе реализованы обе схемы, однако вторая,
используемая в нашей' стране, экономически целесообразна при наличии ТЭЦ вблизи
производства этанола, В последнее время для приготовления парогазовой смеси
вместо пара высокого давления рекомендуют использовать рецикловую воду и
паровой конденсат.
На рис. 1 приведена схема гидратации этилена в паровой фазе.
Вводимый этилен сжимают в компрессоре 1до 8 МПа и смешивают с
циркуляционным газом. Так как давление циркуляционного газа ниже, чем этилена
(объем газа уменьшился за счет образования этанола), его дополнительно сжимают
в компрессоре 2. Смесь свежего этилена с циркуляционным, газом подогревают до
300 °С в теплообменнике 3 продуктами реакции и смешивают с перегретым да 450 °С
паром при давлении 8 МПа. Парогазовая смесь поступает в гидрататор 4. Гидрататор
выполнен в виде реактора идеального вытеснения ~ (РИВ-Н) представляет собой
стальной цилиндр диаметром 1,5 м и высотой 10 м; футерованный изнутри медью и наполненный катализатором, насыпанным на перфорированный конус
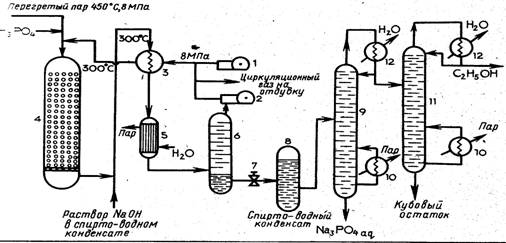
Рис. 1. Схема гидратации этилена в паровой фазе:
1
— компрессор этилена; 2 — компрессор циркуляционного; 3 — теплообменник; 4—гидрататор;
5—котел-утилизатор
На выходе из гидрататора смесь этанола, водяного пара и непрореагировавшего
этилена обрабатывают водным раствором гидроксида натрия для нейтрализации
унесенной потоком фосфорной кислоты, охлаждают в теплообменнике 3 и направляют в
котел-утилизатор 5, в котором вырабатывается пар низкого давления, поступающий
затем в пароперегреватель.
Из котла-утилизатора продукты поступают в сепаратор
(газоотделитель) высокого давления 6. Здесь отделяется циркуляционный газ,
направляемый в компрессор 2, а спирто-водный конденсат с содержанием этанола до
15 % дросселируют через редукционный вентиль 7 до давления 0,5—0,6 МПа и
направляют в сепаратор (сборник) низкого давления 8. В сборнике за счет
снижения давления выделяется растворенный в конденсате этилен, который
добавляют к циркуляционному газу.
Из сепаратора-сборника 8 спирто-водный конденсат поступает в
отпарную ректификационную колонну 9. Здесь за счет нагревания жидкости паром
через кипятильник 10 и ректификации смеси происходит отделение паров этанола,
загрязненных примесями, от водного раствора фосфата натрия. Из колонны 9 этанол
направляют в ректификационную колонну. После ректификации получают очищенный
этанол-ректификат, содержащий ацетальдегид (до 2 %) и диэтиловый эфир (не более
1 %).
Последующая очистка синтетического этанола и требования к нему
зависят от области использования этанола. Производительность современных
установок прямой гидратации этилена достигает 30 тыс. тонн этанола в год.
Производство
этанола гидролизом древесины
Гидролизное производство. Производство этанола из древесного сырья
представляет собой частный случай гидролизного производства, т. е.
производства, основанного на химической переработке растительных материалов
путем каталитического превращения содержащихся в них полисахаридов в
моносахариды. При этом непищевое растительное сырье (отходы древесины,
подсолнечная лузга, кукурузные кочерыжки и др.) может быть превращено в
пищевые, кормовые и технические продукты. Из образующихся в результате
гидролиза этих полисахаридов водных растворов моносахаридов (гидролизатов)
кристаллизацией получают пищевую глюкозу и техническую ксилозу; гидрированием —
ксилит и сорбит; дегидратацией — фурфурол; окислением — органические кислоты;
микробиологической переработкой — этанол, бутанол, ацетон, кормовые дрожжи,
антибиотики.
Из лигнина, остающегося после отделения гидролизата, термической
обработкой получают активированный уголь, уксусную кислоту и фенол; химической
переработкой — активированный лигнин и щавелевую кислоту; прессованием —
строительные материалы.
Процесс
гидролиза растительных материалов, как пример малоотходного производства,
представлен на схеме 3.
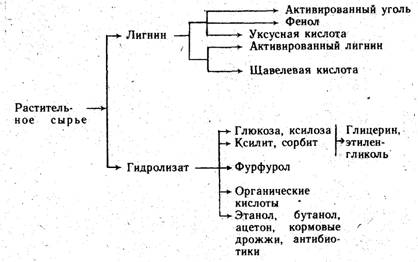
В зависимости от природы целевых продуктов гидролизное
производство строится по той или иной технологической схеме. При этом, если в
качестве сырья используют древесные отходы, то из 1 т абсолютно сухой древесины
может быть получено 220 кг кормовых дрожжей, или 35 кг дрожжей и 175 л этанола, или 110 кг дрожжей и 80 кг фурфурола.
Физико-химические основы производства гидролизного этанола. Наиболее распространенное
сырье для производства гидролизного этанола — древесина — представляет собой
сложную систему, состоящую из целлюлозы, гемицеллюлоз, лигнина, а также
небольших количеств смол, эфирных масел, дубильных и красящих веществ.
Элементный состав органической части древесины практически постоянен: углерод —
49—51 %, Водород — 6,1—6,9 %, кислород — 43—45 %, азот — 1 %. В то же время
содержание целлюлозы, лигнина и гемицеллюлоз зависит от природы древесины. В
среднем в сухой древесине хвойных пород, используемой для производства этанола,
содержится 52—58 % целлюлозы, 28—29 % лигнина и около 20 % гемицеллюлоз.
Гемицеллюлозы — это олигомеры различной степени нолимеризации, состоящие из
пентозанов и гексозанов (С6Н1005)п. Пентозаны построены
из остатков, моносахаридов ксилозы и арабинозы, гексозаны — из остатков
моносахаридов маннозы, галактозы, фруктозы и глюкозы.
Гидролиз
древесины —
каталитический процесс взаимодействия полисахаридов (целлюлозы, пентозанов и
гексозанов гемицеллюлоз) с водой. При этом они превращаются в соответствующие
моносахариды: ксилозу, a-D-глюкозу и т. д., например:

Катализаторы процесса гидролиза —концентрированные и разбавленные
кислоты или кислые соли. При этом скорость гидролиза возрастает с увеличением
константы диссоциации кислоты, ее концентрации и при повышении температуры
гидролизата существенно зависят от природы катализатора. Гидролиз в присутствии
разбавленной серной кислоты (0,4—0,7 %-ной) проводят при температуре 120—190
"С и давлении 0,6—1,2 МПа. В результате получают гидролизат, загрязненный
фурфуролом, органическими кислотами и другими веществами. Это объясняется тем,
что параллельно с гидролизом протекают реакции разложения образовавшихся
моносахаридов, скорость которых с повышением температуры также возрастает.
Поэтому, несмотря на то что константа скорости реакции гидролиза больше
константы скорости реакции разложения, выход гексоз в этом Случае не превышает
70 % от теоретически возможного при степени гидролиза около 90%. Гидролиз в
присутствии концентрированных кислот (70— 80 %-ной серной кислоты или 31—41
%-ной соляной кислоты) проводят при температуре не выше 60 "С и атмосферном
давлении. Он дает чистый гидролизат с выходом моносахаридов до 95% от
теоретически возможного.
Брожение (ферментация) процесс разложения углеводов под воздействием
микроорганизмов или выделенных из них ферментов. В производстве этанола
используют одну из разновидностей брожения — спиртовое брожение, вызываемое
ферментом зимазой, содержащимся в дрожжевых клетках. Из моносахаридов
спиртовому брожению подвергаются только гексозы. Процесс спиртового брожения, a-D-глюкозы, составляющей
структурную единицу целлюлозы, происходит без доступа кислорода (анаэробное
брожение) и включает ряд стадий с участием фосфорорганических соединений. В
результате сложных превращений из глюкозы образуется этанол.
Параметры
процесса брожения выбирают, исходя из оптимальных условий развития дрожжевых
клеток и подавления развития их спутников — кислотообразующих бактерий
молочнокислого и уксуснокислого брожения.
Так как оптимальные температуры размножения дрожжевых клеток
практически совпадают и равны 35— 50 °С, то подавить развитие бактерий
изменением температуры нельзя. Для этого повышают кислотность среды, вводя в
гидролизат серную или молочную кислоту. При рН 4,2 дрожжевые клетки интенсивно
растут, а бактерии не размножаются. Поэтому на практике процесс брожения
проводят при температуре 27 С, атмосферном давлении и в кислой среде (рН=
=3,8—4,0).
Технологическая схема производства этанола гидролизом древесины. Процесс производства
этанола складывается из двух последовательных стадий; объединенных в единую
технологическую схему: гидролиза древесины и сбраживания образующегося гидролизата.
В нашей стране распространен метод гидролиза древесины разбавленной серной
кислотой. В качестве сырья используют отходы хвойной древесины с высоким
содержанием гексозанов.
Производство этанола по этой схеме представляет собой
полунепрерывный перколяциоиный процесс, в основе которого лежит принцип:
непрерывной фильтрации раствора кислоты через периодически загружаемое в
реактор древесное сырье с непрерывным в течение нескольких часов отбором
гидролизата.. При этом раствор кислоты служит одновременно экстрагентом
образующихся при гидролизе моносахаридов. Схема производства этанола гидролизом
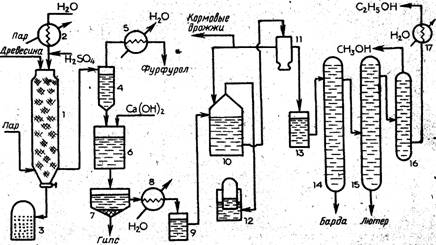
древесины приведена на рис. 2.
Древесное сырье в виде опилок или измельченной щепы загружают в
гидролиз-аппарат 1 — цилиндрический стальной сосуд, футерованный внутри
кислотоупорным материалом. После загрузки сырья в аппарат через специальное
оросительное устройство подают нагретый до 1$0—190 °С раствор серной кислоты
концентрацией около 0,5 %. Воду для получения раствора кислоты подогревают в
подогревателе 2. В гидролиз-аппарат вводят также пар и создают давление 1,0—1,2
МПа. Через фильтрующее устройство, расположенное в нижней части
гидролиз-аппарата и выполненное в виде перфорированных медных трубок, из
аппарата непрерывно отводят гидролизат и направляют его в испаритель 4. Вследствие
снижения давления гидролизат вскипает и пары, содержащие фурфурол (tKHn= 161,7 °С при атмосферном
давлении), поступают в конденсатор 5. Цикл непрерывной работы гидролиз-аппарата
от загрузки до выгрузки составляет несколько часов, затем оставшийся в нем
лигнин передавливают после открытия заслонки в сборник после этого в аппарат
загружают новую порцию древесного сырья.
После
отделения фурфурола гидролизат из испарителя поступает в нейтрализатор 6, куда
подают раствор гидроксида кальция, а оттуда —

Сульфитный щелок подают в колонну /, где из него паром выдувают
примеси. Очищенный щелок поступает в нейтрализатор 2, куда подают раствор
гидроксида кальция и вводят питательные соли. Из нейтрализатора щелок после
охлаждения до 30 °С в холодильнике 4 направляют сначала на первую ступень брожения
в дрожжанку 5, а затем на вторую ступень брожения в бродильный чан 6 и в.
сепаратор 7. В сепараторе дрожжи отделяются от образовавшейся бражки, и их
возвращают в дрожжанку. После сепаратора бражку, содержащую 1,0— 1,2 % спирта,
направляют на концентрирование и выделение этанола аналогично тому, как это
происходит в производстве гидролизного этанола (см. рис. 2).
Переработкой сульфитных щелоков можно получить (в расчете на 1 т
воздушно-сухой древесины) 90—110 л этанола, 40—50 кг белковых дрожжей, 600—700
кг сухих лигносульфонатов.
Комплексная
переработка сульфитных щелоков имеет и большое значение в экологическом плане.
Существующие промышленные способы производства целлюлозы не обеспечивают полной
утилизации и переработки его отходов — варочных сульфитных щелоков и отдувочных
газов. Вследствие этого целлюлозно-бумажная промышленность в настоящее время —
одна из основных источников загрязнения водоемов сточными водами.
этанол
урок одноатомный спирт
Глава
3. МЕТОДИЧЕСКИЕ РАЗРАБОТКИ ПО ТЕМЕ «СПИРТЫ»
Система уроков по теме: "Предельные одноатомные спирты"
Пояснительная
записка.
1.
урок-лекция,
2.
тренировочные
домашние упражнения,
3.
урок-коррекция.
Урок-лекция
(объяснение нового материала).
Цели:
-
ввести понятие предельных одноатомных спиртов, свойств;
-
развитие интереса, умения выделять главное, научить сравнивать и анализировать.
1.
Определение.
Органические
соединения, которые состоят из предельного углеводородного радикала и содержат
одну функциональную гидроксильную группу (-ОН), называются насыщенными
одноатомными спиртами.
Общая
формула СnН2n+1ОН ( где n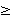 1) или R – ОН
1) или R – ОН
2.
Гомологический ряд и номенклатура
СН3
ОН – метиловый спирт (метанол),
СН3
СН2ОН – этиловый спирт (этанол)….
-
СН2 - гомологическая разница
Пример:
3-метилгексанол – 1
2.
Изомерия положения функциональной группы (-ОН)
Пример:
бутанол-1 -> бутанол-2
3.
Изомерия между классами (предельные одноатомные спирты изомерны простым эфирам)
4.
Физические свойства
1)
Спирты от С1 до С11 – жидкости, от С12 до С - твердые.
2)
Легче воды, бесцветны, жидкие имеют резкий запах, твердые запаха не имеют.
3)
Низшие спирты (до пропилового) смешиваются с водой в любых отношениях. Высшие
спирты практически нерастворимы в воде.
Межмолекулярная
водородная связь возможна между отдельными молекулами спирта и между молекулами
спирта и воды. Это влияет на физические свойства спиртов: повышает температуру
кипения, снижает летучесть, способствует хорошей растворимости в воде, не
позволяет перегонкой получить 100% спирт из его водного раствора.
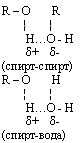
5.
Химические свойства (с примерами):
1)
горение,
2)
взаимодействие с активными металлами;
3)
взаимодействие с органическими кислотами, с неорганическими кислотами;
4)
с галогеноводородами;
5)
окисление
-
первичный спирт -> альдегид,
-
вторичный спирт -> кетон,
-
третичный спирт: тяжело окисляется с разрывом С-С связи;
6)
дегидратация:
-
внутримолекулярная,
-
межмолекулярная с образованием простых эфиров;
7)
дегидратация и дегидрирование (реакция Лебедева).
6.
Получение одноатомных спиртов (с примерами).
В
промышленности:
1) получение
СН3 ОН
- из
синтез-газа
- во время сухой
перегонки древесины (древесный спирт),
2) гидратация
алкенов,
3) брожение
сахаристых веществ.
В лаборатории:
1) из алканов
через галогенопроизводные,
2)
восстановление альдегидов.
Физиологическое
действие
спиртов на организм негативно.
СН3
ОН – сильный яд! В малых количествах вызывает слепоту, в больших – приводит к
смерти.
С2Н5ОН
– наркотик. Под влиянием этанола у человека ослабляется внимание,
затормаживается реакция, нарушается корреляция движений. При продолжительном
употреблении вызывает глубокие нарушения нервной системы, заболевания
сердечно-сосудистой системы, пищеварительного тракта, наступает тяжелая болезнь
– алкоголизм.
7.
Применение спиртов.
1)
Метанол:
- в
промышленном органическом синтезе (производство формальдегида),
- как
растворитель,
- как добавка
к бензину.
2) Этанол:
-
производство уксусной кислоты,
- как
растворитель,
- в
парфюмерии,
- в медицине,
- как
топливо,
- в пищевой
промышленности.
8.
Связь между ациклическими углеводородами и спиртами (показать на примерах).
Домашнее
задание: пар. 17 (учебник О.С. Габриелян), тренировочные упражнения.
Приложение
1.
Закрепление (если позволяет время)
1.
Назвать
по международной номенклатуре (2-4 примера).
2.
Написать
структурные формулы изомерных спиртов С4Н9 ОН и назвать
их.
Приложение
2. Тренировочные
домашние упражнения.
Тема:
“Одноатомные спирты”.
Сложность
1
(оценка “удовлетворительно”).
2.
Назвать
вещество и написать два его гомолога и два изомера
1.
Какой
объем водорода выделится при взаимодействии 19,5 г калия с этанолом.
Сложность
2
(оценка “хорошо”).
1.
Чем
объясняется изомерия спиртов? Пояснить это на примере спирта, в молекуле
которого четыре атома углерода. Назвать каждый изомер.
2.
Написать
реакции получения метанола.
3.
Осуществить
превращения:
Этан
-> бромэтан-> этен-> этанол-> метилэтиловый эфир. Где происходит
дегиратация?
4.
При
сжигании 4,8 г органического вещества образовалось 3,36 л оксида углерода (IV) и 5,4 г воды. Плотность паров этого вещества по метану 2. Определить
формулу вещества.
Сложность
3
(оценка “отлично”).
1.
Чем
отличаются первичные, вторичные и третичные спирты? (Привести примеры каждого и
назвать их)
2.
Предложить
схему получения из пропана пропанол-1.
3.
Осуществить
превращения (предложить две цепочки).
4.
При
межмолекулярной дегидратации 100г одноатомного предельного спирта неизвестного
строения выделилось 21,09 г воды и выход продукта реакции составил 75% от
теоретического. Определить строение спирта.
Урок-коррекция.
1
этап.
10-15 минут. Учащиеся задают вопросы по тренировочным упражнениям.
2
этап.
20-30 минут. Самостоятельная работа. Работа разноуровневая. Учащиеся выбирают
любой вариант.
Самостоятельная
работа
(тема: “Одноатомные спирты”).
Оценка
“удовлетворительно”
|
Вариант 1
|
Вариант 2
|
|
1.
Какие
вещества называют спиртами? (привести примеры).
2.
Какие
спирты образуются в результате гидратации следующих веществ: этена, бутена-2.
3.
Осуществить
превращения:
1)С2Н 5
ОН->С2Н 4 ->С2Н 5 Cl->С2Н5
ОН
2)ацетилен- >А->
этанол
4. При взаимодействии 12,8 г спирта с натрием образовалось 4,48 л водорода. Какой это спирт?
|
1.
Написать
общую формулу спиртов. Что такое функциональная группа?
2.
Написать
уравнение гидролиза водным раствором щелочи следующих соединений: хлорэтана,
2-хлорбутана.
3.
Осуществить
превращения:
1)СН 4 ->
С2Н 2 -> С2Н 4 -> С2Н
5 ОН
2)этанол -> А->
этан
4. При дегидратации 12 г спирта образовался алкен и 3,6 г воды. Какой это спирт?
|
Оценка
“хорошо”
|
Вариант 3
|
Вариант 4
|
|
1.
Объяснить
образование водородных связей между молекулами спирта и влияние на физические
свойства.
2.
Как
получить спирты из алкенов (привести два примера).
3.
Осуществить
превращение: оксид углерода (IV) – метанол – хлорметан – этан – углекислый
газ.
4.
Найти
молекулярную массу вещества А: пропанол-1 – А - пропанол-2
5.
0,5
моль метанола нагрели с KBr и H2SO4 и получили 38 г бромметана. Найти выход бромметана
|
1.
Как
доказать, что спирты отравляюще и пагубно действуют на организм человека.
2.
Дописать
уравнения и назвать вещества.
1.
СН 3
– CHCl - СН 2 - СН 3 + КОН(водн)
2.
СН 3
– CHCl - СН 2 - СН 3 + КОН(спирт)
1.
Осуществить
превращения: метан – этан – этен – этанол – углекислый газ
2.
Определить
молекулярную массу вещества А: этанол – А – 1,2-дихлорэтан.
3.
Какая
масса этилата натрия получится при взаимодействии этанола массой 11,5 г с натрием массой 9,2 г?
|
Оценка
“отлично”
|
Вариант 5
|
Вариант 6
|
|
1.
Почему
температура кипения спиртов намного выше, чем соответствующих углеводородов?
2.
Сколько изомерных бутиловых спиртов может образоваться из
изомерных алкенов С4Н 8 при их гидратации?
3.
Написать
уравнения реакций, в результате которых можно получить из метана
бутадиен-1,3.
4.
Метанол
массой 2,04 кг получили взаимодействием оксида углерода (11) объемом 2 м3 с водородом объемом 5 м3 (ну). Найти выход продукта реакции.
5.
Определить
массу пропанола-2, взятого для реакции, если во время дегидратации
пропанола-2 получили пропен, который обесцветил бромную воду массой 200 г. Массовая доля брома в бромной воде равна 3,2%.
|
1.
Почему
нельзя физическими методами получить 100%-ный этанол из его водного раствора?
2.
Сколько изомерных третичных спиртов имеют состав .С6Н13
ОН ? Написать формулы и назвать .
3.
Написать
уравнения реакций, в результате которых можно получить из метана диэтиловый
эфир.
4.
Какую
массу бутадиена-1,3 можно получить из спирта объемом 230 л и плотностью 0,8 кг/л, если массовая доля этанола в спирте 95%? Выход продукта реакции
составляет 60%.
5.
Вычислить
массу добытого продукта, если выход на обеих стадиях синтеза составляет по
60%, если известно, что из пропанола-2 массой 24 г добыт 2-бромпропан, из которого синтезировали 2,3-диметилбутан.
|
Химические
свойства спиртов
Одноатомные
спирты не обладают ни щелочными, ни кислотными свойствами. Водные растворы
спиртов на индикаторы не действуют.
Рассмотрим
химические свойства спиртов на примере этанола. В молекуле этилового спирта СН3–СН2–ОН
имеется четыре типа химических связей, различающихся полярностью: 1) Н–О;
2)
С–О; 3) С–Н; 4) С–С. В результате химических превращений разрываются наиболее
полярные связи Н–О, С–О и С–Н. Неполярная связь С–С в реакциях спиртов не
разрывается.
1. Разрыв связи Н–О в реакции с натрием:

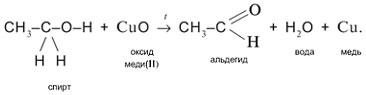
2. Одновременный разрыв связей Н–О и С–Н, находящихся
при спиртовом атоме углерода, под действием окислителя (CuO) с отщеплением
молекулы Н2О и образованием альдегида (СН3СНО):
2.
Разрыв
связи 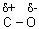 под действием нуклеофильных
реагентов (ионов В– или молекул с неравномерным распределением
заряда в молекуле
под действием нуклеофильных
реагентов (ионов В– или молекул с неравномерным распределением
заряда в молекуле  ) в
кислой среде.
) в
кислой среде.
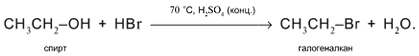
б)
Действие кислородсодержащих кислот – неорганических и органических – с
образованием сложных эфиров (подробнее см. урок 29):


Модель
нуклеофильного и электрофильного процессов
4. Внутримолекулярное отщепление Н и ОН от соседних
атомов С в присутствии концентрированной серной кислоты при нагревании с
образованием алкена:
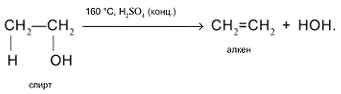
5. Межмолекулярное отщепление Н и ОН от двух разных
молекул спирта при умеренном нагревании в присутствии дегидратирующих агентов.
Продукт реакции – простой эфир:
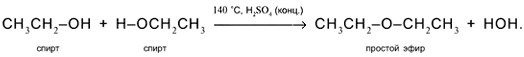
6. Спирты горят на воздухе с расщеплением всех
связей и образованием углекислого газа и воды:
С2Н5ОН
+ 3О2 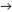 2СО2
+ 3Н2О.
2СО2
+ 3Н2О.
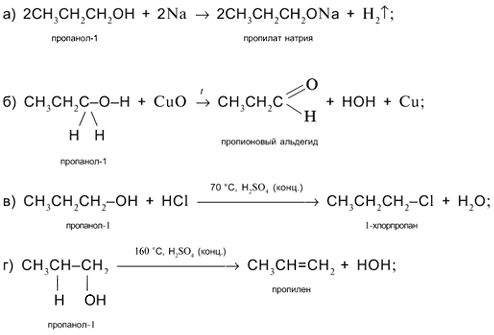
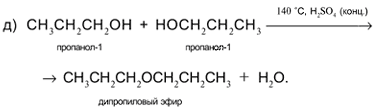
Задача. Составьте уравнения реакций пропанола-1
СН3СН2СН2ОН со следующими реагентами: а) Na;
б) CuO; в) HCl в присутствии H2SO4 (конц.) при
нагревании; г) H2SO4 (конц.) при 160 °С (продукт – алкен);
д) H2SO4 (конц.) при 140 °С (продукт – простой
эфир).
Решение
1. Составьте уравнения реакций пропанола-2 СН3СН(ОН)СН3
со следующими реагентами:
а) Na; б) CuO; в) HCl в
присутствии H2SO4 (конц.) при нагревании; г) H2SO4
(конц.) при 160 °С (продукт – алкен); д) H2SO4 (конц.)
при 140 °С (продукт – простой эфир).
2. Алюминий реагирует со спиртами подобно натрию.
При этом происходит замещение гидроксильного водорода на металл и выделение
свободного водорода Н2. Реакция протекает при нагревании около температуры
кипения спирта. Составьте уравнения реакций металлического алюминия со
спиртами: а) метанолом; б) этанолом.
3. Почему температуры
кипения спиртов выше, чем у соответствующих по молекулярной массе углеводородов
(С2Н5ОН, Мr = 46, tкип =
78 °С; С3Н8, Мr = 44, tкип =
–42 °С)?
4. Напишите схему реакций, с
помощью которых пропанол-1 можно превратить в пропанол-2.
Из
спиртов ROH получают соединения многих других классов: алкилгалогениды RHal,
алкены R'СН=СН2, простые эфиры RОR', сложные эфиры R'СООR, альдегиды
R'СНО, карбоновые кислоты R'СООН и т.д. Спирты используют в качестве
растворителей при синтезе новых соединений, производстве лаков и красок,
фармацевтических препаратов, душистых веществ, парфюмерно-косметической
продукции. Этанол используют как дезинфицирующее средство, горючее в
двигателях. Он идет также на изготовление алкогольных напитков.
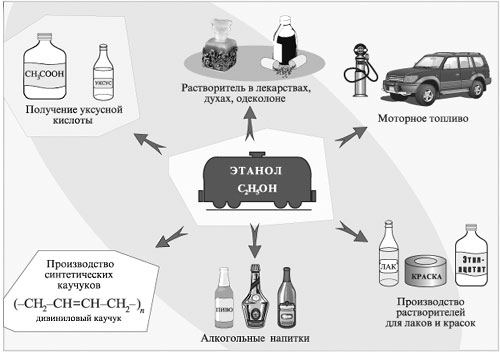
Применение
этилового спирта
Для
прочного усвоения знаний по химии надо овладеть умением составлять и решать
цепочки химических превращений. Решить цепочку – это значит записать уравнения
реакций, соответствующие каждой стрелке схемы. В результате удается из
имеющихся в наличии веществ получать новые необходимые вещества. Для решения
цепочек необходимо знать:
а)
способы получения веществ и б) химические свойства веществ различных классов.
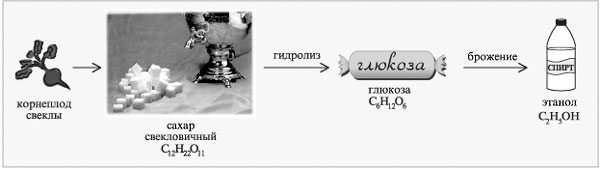
Пример
цепочки химических превращений в производстве этанола
Задача. Составьте уравнения реакций для цепочки превращений:
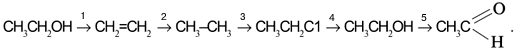
Решение
Воспользуемся
удобным способом, помогающим определять реагенты, требуемые для превращения
одного вещества в другое: будем находить отличие в составе двух веществ,
стоящих по разные стороны от стрелки, и из химической формулы с большим числом
атомов вычитать формулу с меньшим числом атомов. Так, для первой стрелки схемы:
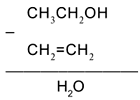
Следовательно,
чтобы превратить спирт СН3СН2ОН в алкен СН2=СН2,
надо отщепить молекулу воды от молекулы спирта:
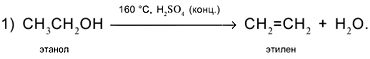
Вторая
реакция схемы состоит в присоединении водорода к алкену:

Третья
стрелка схемы представляет реакцию замещения водорода в алкане СН3–СН3
на хлор. Это достигается действием молекулярного хлора на алкан:

Четвертое
превращение – замещение атома хлора в хлорэтане С2Н5Сl на
гидроксильную группу ОН:
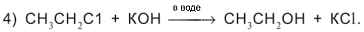
Пятая
реакция заключается в отщеплении двух атомов водорода от молекулы спирта. На
практике это означает окисление спирта кислородом [O] окислителя, т.е.
связывание избыточных атомов Н в форме Н2О:

ЛИТЕРАТУРА
1.
О.В.
Байдалина. О прикладном аспекте химических знании // Химия в школе, 2005, № 5,
с. 45-47.
2.
Ахметов
Н.С. Методика преподавания темы «Закономерности протекания химических реакций»
// Химия в школе. 2002, № 3, с. 15 – 18.
3.
Ахметов
Н.С. Учебник для 8 класса общеобразовательных учреждений. М.: Просвещение, 1998 г.
4.
Рудзитис
Г.Е., Фельдман Р.Г. Учебник для 8 класса средней школы. М.: Просвещение, 1992.
5.
Материалы
сайта www.1september.ru
6.
О.С. Габриелян,
Н.П. Воскобойникова, А. В. Ящукова. Настольная книга учителя. Химия. 8 класс.
М.: Дрофа, 2003 г.
7.
Малинин
К.М. Технология серной кислоты и серы. М., Л., 1994.
8.
Васильев
Б.Г., Отвагина М.И. Технология серной кислоты. М., 1985.
9.
Отвагина
М.И., Явор В.И., Сретенская Н.С., Шарифов М.Ю. Промышленность минеральных
удобрений и серной кислоты. М., НИИТЭХИМ. 1972. Выпуск № 4.
10. Резницкий И.Г.
Возможности использования нитрозного способа для переработки газов автогенных
процессов на серную кислоту / Цветные металлы. 1991. № 4.
11. Березина Л.Т., Борисова
С.И. Утилизация фосфогипсов - важнейшая экологическая проблема // Химическая
промышленность. 1999 г. № 12.
12. Громов А.П. Экологические
аспекты производства серной кислоты // Экология и промышленность России. 2001,
№ 12.
13. Лидин Р.А. Химия:
Руководство к экзаменам / Р. А. Лидин, В. Б. Маргулис. – М.: ООО Издательство
«АСТ»: ООО «Издательство Астрель», 2003. с. 64 – 70.
14. Единый государственный
экзамен 2002: Контрольные измерительные материалы: Химия / А.А. Каверина, Д.Ю.
Добротин, М.Г. Снастина и др.; М.: Просвещение, 2002. – с. 39 – 51.
15. Химия: Большой справочник
для школьников и поступающих в вузы / Е.А. Алферова, Н.С. Ахметов, Н.В.
Богомолова и др. М.: Дрофа, 1999. с. 430-438
16. Р.П. Суровцева, С.В.
Сафронов. Задания для самостоятельной работы по химии. М.: Просвещение, 1993 г.