Значимость острого воспаления в инициировании атеросклероза у детей
Министерство
Здравоохранения Республики Узбекистан
Ташкентский
Педиатрический Медицинский Институт
Кафедра
биологической химии
ДОКЛАД
«Значимость
острого воспаления в инициировании атеросклероза у детей»
Сидикова Н.Т., 218 Б группа,
педиатрический факультет
Научный руководитель: к. м. н. доц.
Хайбуллина З. Р.
Ташкент – 2009г.
План
1.
Характеристика
ЛПНП.
2.
Воспаления
– существенная роль в развитии атеросклероза.
3.
Белки
Острой Фазы способны модифицировать ЛПНП.
4.
Действие
вирусов, токсинов.
Вывод.
Взаимоотношение
воспаления и атеросклероза является темой научной дискуссии более 150 лет. В.Н.Титов
(2000) выдвигает гипотезу о ключевой роли в патогенезе атеросклероза дефицита в
клетках полиненасыщенных жирных кислот. По мнению Титова, атеросклероз –
специфический синдром воспаления, пусковым моментом патогенеза которого является
блокада рецепторного поглощения клетками ЛПНП и внутриклеточный дефицит эссенциальных
полиненасыщенных жирных кислот (поли ЖК).
Биохимическую основу
патогенеза атеросклероза составляет блокада Апо-В100 рецепторного эндоцитоза
липопротеинов низкой плотности (ЛПНП). У человека ЛПНП являются основной
транспортной формой эссенциальных поли-ЖК в форме эфиров холестерина ( поли –
ЭХ), точнее, этерифицированных холестеринов (Хс) эссенциальных поли-ЖК. ЛНП
апоВ-рецептор
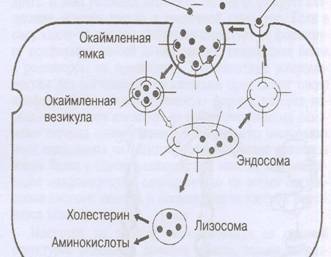
Различие
физико-химических свойств и функциональных особенностей ЛПНП является основой
разделения ЛПНП в норме на два субкласса:
ЛПНП-1-большие по
размерам, малой плотности липидтранспортные молекулы с еще высоким содержанием
ТГ, наличием н-ЭХ, отсутствием поли-ЭХ и пока неактивным положением
апоВ-100-лиганда; с ЛПНП-1 ассоциирован апоС-III.
ЛПНП-2 – средние по
размерам, более плотные ЛП, с более низким, чем в ЛПНП-1, содержанием ТГ и
существенно более высоким уровнем поли-ЭХ, оптимальной конформацией апоВ-100 и
активным положением лиганда, который взаимодействует с апоВ-100-рецепторами.


1
2 3
1-ЛПНП транспортная
форма ЭХ поли-ЖК 2- БОФ- блокатор апоВ-100 рецепторного комплекса 3-
клетка,которой эссенциальные поли-ЖК жизненно необходимы.
В
условиях блокады апо-В -100 эндоцитоза ЛПНП,
циркулурищие
в крови, становятся антигенами. Длительная циркуляция ЛПНП и ЛППП, как всех иных
белковых макромолекул ( креатинкиназа ЛДГ,АЛТ, АСТ ) вызывает активацию нейтрофилов,
которые денатурируют ( модифицируют) макромолекулы ЛПНП и ЛППП путем прикрепления
к апо-В 100 сиаловых кислот, усиления перекисного окисления апоВ-100 и поли жк
в сложных липидах. В результате денатурации в ЛП формирируются патологические эпитопы,
которые позволяют другим иммунокомпетентным клеткам распознавать “ чужеродные.
” макромолекулы ЛПНП и ЛППП и удалять их из кровотока.
Клетки РЭС, моноциты и макрофаги
интимы сосудов удаляют ЛПНП и ЛППП из крови путем неспецифического фагоцитоза.
На клеточной мембране макрофагов модифицированные ЛПНП и ЛППП взаимодействуют со
скважендер - рецепторами ( рецепторами - мусорщиками). При этом атеросклеротическое
поражение сосуда формируют макрофаги. Чем выше иммунный статус организма, тем активнее
макрофаги поглощают денатурированные ЛП, накапливают их в стенке сосудов, тем активнее
развивается атеросклероз.
Моноциты захватывают денатурированные
ЛП, проникают в стенку сосуда и дают начало липидным пятнам, а позже - атеросклеротическим
бляшкам.
Поглощение макрофагами ЛПНП,
ЛППП и формирование пенистых клеток происходит там, где локализованы клетки рыхлой
соединительной ткани.
Внутренняя
пограничная пластина интимы является преградой для диффузии ЛП и миграции макрофагальных
клеток.
В
силу этого формирование пенистых клеток и последующие деструктивные изменения захватывают
медию и более глубокие слои стенки сосуда.
Фагоцитированные
макрофагами модифицированные ЛПНП и ЛППП воспринимаются ими как чужые молекулы белка
и попадают в лизосомы. В лизосомах кислые протеазы осуществляют протеолиз апо- В
100, но гидролизовать поли -ЭХ на свободную ЖК и свободный ХС ни моноциты ни макрофаги
не могут.
Этерифицированные ХС поли
- ЖК накапливаются в лизосомах в форме кристаллов поли - ЭХ и превращаются во внутриклеточные
инородные тела, которые вначале провоцируют гипертрофию лизосом, а позже кристаллы
поли -ЭХ занимают весь цитозоль, формируя пенистые клетки (лаброциты). Далее кристаллы
поли- ЭХ механически разрушают лизосомы, вызвая аутолиз и гибель пенистых клеток
по типу некроза.
Деструкция клеточных мембран
и выход содержимого клеток в межклеточное пространство вызывают реактивные изменения
окружающих клеток, гиперпродукцию ими межклеточного матрикса (
коллагена и эластина ) и запускают неспецифичный синдром воспаления.
Ситуация усугубляется тем, что в условиях внутриклеточного дефицита поли –ЖК фибробласты
и гладкомышечные клетки синтезируют W-9-лейкотриены,
которые активируют синдром воспаления и синтез белковых молекул, активирующих миграцию
нейтрофилов. При этом вокруг каждой некротизированной
клетки формируется очаг активированного асептического воспаления.
Лизис прилежащих клеток,
синтез ими интерлейкинов приводят к усилению синтеза гепатоцитами позитивных белков
острой фазы : С- реактивного белка, фибриногена, протромбина, апо(а).
С позиций физиологии фагоцитоз
клетками денатурированных ЛП и элиминация их из кровотока считается нормальным процессом
компенсации. Однако невозможность для макрофагов гидролизовать поли- ЭХ приводит
к тому, что процесс компенсации заканчиваются гибелью клеток.
Также, многочисленные
микробные токсины способны ингибировать активность ферментов транспорта в крови
ЖК. Ингибирование гидролиза Тг в ЛПОНП изменяет поглощение клетками ЛПОНП и ЖК,
а ингибирование липолиза в ЛППП и ЛПНП-а нарушает поглощение клетками ЛПНП-б и
эссенциальных поли-ЖК. Кроме того, липополисахариды микроорганизмов
ассоциируются в крови с ЛПНП и нарушая конформацию апоВ-100, блокируют
рецепторное поглощение клетками поли-ЖК. Гепатотоксичное действие
микроорганизмов способно ингибировать в гепатоцитах синтез ЛХАТ и блокировать
транспорт в клетки поли-ЖК на этапе формирования поли-ЭХ. Действие микробных
цитотоксинов способно ингибировать способность гепатоцитами апоА-1 и
формирование тех ЛПВП, которые осуществляют отток от клеток свободного Хс.
Кроме того, наличие у больного иного хронического заболевания может
способствовать развитию атеросклероза, особенно когда заболевание поражает
рыхлую соединительную ткань (ревматизм и системная красная волчанка), тем более
когда патологический процесс локализован в стенке артерий (болезнь Такаясу).
Внедрение в клетки
вирусов существенно действует на процессы клеточной адаптации, изменяет функцию
генов, которые кодируют синтез ферментов метаболизма липидов в клетке. Это в
большей степени относится к вирусу герпеса и цитомегаловирусам, которые находят
в стенке сосуда, особенно в очагах атеросклеротического поражения. В острой
фазе восплаения цитомегаловирусы ингибируют активность нейтральной гидролазы
моноеновых ЭХ и инициируют накопление их в клетках.
Вирусы способны
блокировать в клетках синтез нейтральной гидролазы моно-ЭХ, вызывая накопление
в микросомах холестерололеата с формированием пенистых клеток, липидных пятен и
полос. Ингибирование гидролиза моно-ЭХ приводит к накоплению их в цитозоле
ретикулоэндотелиальных клеток. Возможно, поэтому вирусная инфекция является
одним из факторов, который провоцирует формирование рестенозов в коронарных
артериях после баллонной дилатации. Аденовирусы индицируют синтез гепатоцитами
БОФ, в частности САА, с последующим нарушением как рецепторного поглощения
клетками ЛПНП, так и функции апоА-1 ЛПВП. В условиях высокожировой диеты
аденовирусы индуцируют гены воспаления и активируют формирование липидной
инфильтрации стенки сосудов. При этом формирование липидных пятен и полос из
моноеновых эфиров Хс является типичным проявлением острой фазы воспаления.
Вывод
Инфекционные агенты
запускают синдром воспаления, БОФ блокируют рецепторный эндоцитоз ЛПНП, что
способствует дефициту в клетках ПНЖК, избытку в крови ЛПНП, что трансформирует
синдром воспаления в синдром атеросклероза.
БОФ – СРБ, САА, апо(а)
– при атеросклерозе как синдроме воспаления блокируют физиологические лиганды в
ЛПОНП и ЛПНП, становятся их патофизиологичными лигандами и переадрисуют поток
насыщенных и эссенциальных поли-ЖК от высокодифференцированных клеток к клеткам
в очаге воспаления.