|
Лекарственное вещество
|
Химическая структура
|
Описание
|
|
Chloramphenicol – хлорамфеникол (Левомицетин)
|
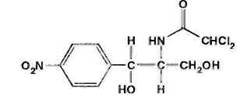
D-(-)-трео-1-n-нитрофенил-2-дихлорацетиламинопропандиол-1,3
|
Белый или белый со слабым
желтовато-зеленым оттенком кристаллический порошок без запаха. Температура
плавления 149-1530С. Удельное вращение от +18 до +210
(5%-ный раствор в этаноле)
|
|
Chloramphenicol Stearate – хлорамфеникола стеарат
|
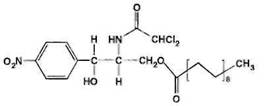
D-(-)-трео-1-n-нитрофенил-2-дихлорацетиламинопропандиол-1,3
3-стеарат
|
Белый с желтоватым оттенком
порошок, практически без запаха и вкуса. Температура плавления 88-900С.
Удельное вращение от +15 до +200 (5%-ный раствор в этаноле)
|
|
Chloramphenicol Sodium Succinate – хлорамфеникола натрия
сукцинат
|
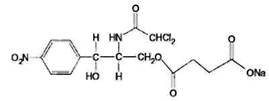
D-(-)-трео-1-n-нитрофенил-2-дихлорацетиламинопропандиол-1,3
3-сукцинат натрия
|
Порошок белого или с желтоватым
оттенком цвета, со слабым специфическим запахом. Гигроскопичен. Удельное
вращение от +5 до +80 (5%-ный раствор в этаноле)
|
Хлорамфеникол
малорастворим в воде, эфире, хлороформе, растворим в этилацетате. В отличие от
хлорамфеникола и его эфира стеарата, хлорамфеникола натрия сукцинат очень легко
растворим в воде. В этаноле хлорамфеникол легко растворим, стеарат трудно
растворим, натрия сукцинат — растворим. Хлорамфеникола натрия сукцинат
практически нерастворим в эфире и хлороформе, а хлорамфеникола стеарат легко
растворим в хлороформе. Во всех указанных растворителях хлорамфеникола стеарат
образует мутные растворы. Хлорамфеникола натрия сукцинат, являясь натриевой
солью, дает положительную реакцию на ион натрия.
Подлинность
хлорамфеникола подтверждают по УФ-спектру 0,002%-ного водного раствора, который
в области 220-400 нм имеет максимум поглощения при 278 нм и минимум при 237 нм.
ФС рекомендует устанавливать величину удельного показателя поглощения при длине
волны 278 нм (от 290 до 305). Водный 0,04%-ный раствор хлорамфеникола натрия
сукцината в области 230-350 нм имеет один максимум поглощения при длине волны
276 нм. Для идентификации хлорамфеникола и хлорамфеникола натрия сукцината
использованы вторые производные УФ-спектров поглощения, а также значения
отношений оптических плотностей в максимумах и минимумах поглощения
(растворители вода, этанол).
Реакция
гидролиза в щелочной среде лежит в основе испытания подлинности хлорамфеникола
и его производных. При нагревании в течение 1-2 мин с 15%-ным раствором
гидроксида натрия хлорамфеникол и хлорамфеникола стеарат приобретают желтое
окрашивание, переходящее и красно-оранжевое. В отличие от хлорамфеникола
стеарата хлорамфеникол при дальнейшем нагревании в щелочной среде образует
кирпично-красный осадок аци-формы n-нитрофенилпропандиола-1,3.
Одновременно ощущается запах аммиака. Фильтрат после подкисления азотной
кислотой дает характерную реакцию на хлориды. Это позволяет подтвердить наличие
в молекуле хлорамфеникола нитрофенильного радикала, аминогруппы и ковалентно
связанного атома хлора, поскольку при щелочном гидролизе образуется "основание"
хлорамфеникола, переходящее в аци-форму, выделяются аммиак и натриевая соль
глиоксиловой кислоты:
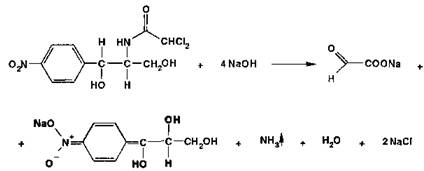
Хлорамфеникол,
подобно эфедрину, за счет наличия в молекуле спиртового гидроксида и вторичной
алифатической аминогруппы может образовывать окрашенные комплексные соединения
с солями тяжелых металлов. С раствором сульфата меди образуется синий осадок,
который растворяется в н-бутаноле, окрашивая его слой в фиолетовый цвет.
Хлорамфеникола
натрия сукцинат идентифицируют также по остатку янтарной кислоты, в частности
при нагревании с резорцином и концентрированной серной кислотой. Образуется
желтый раствор, имеющий в УФ-свете желтовато-зеленую флуоресценцию. Сели вместо
резорцина взять гидрохинон, после охлаждения разбавить водой и смешать с
бензолом, то его слой приобретает красную окраску.
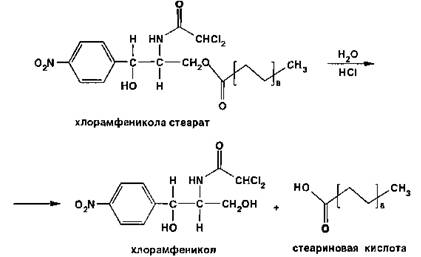
Хлорамфеникола
стеарат, являясь сложным эфиром, гидролизуется в присутствии концентрированной
хлороводородной кислоты (при нагревании) с образованием стеариновой кислоты,
которая всплывает на поверхность в виде масляных капель, затвердевающих при
охлаждении:
Известны
многочисленные способы идентификации и количественного определения, основанные
на предварительном гидрировании (цинковой пылью в кислой среде) нитрогруппы и
молекуле хлорамфеникола до аминогруппы. Одновременно отщепляются атомы хлора:

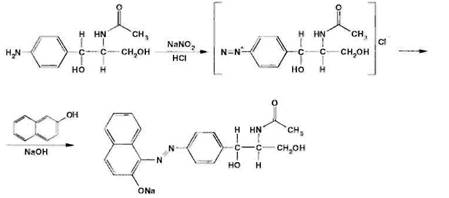
Образовавшийся
1-n-аминофенил-2-ацетиламинопропандиол-1,3
диазотируют и превращают в азокраситель, сочетая с β-нафтолом,
α-нафтиламином или другим амином или фенолом. Например, в результате
азосочетания с β-нафтолом образуется азокраситель красного цвета:
Для
идентификации лекарственных веществ, содержащих в молекуле нитрогруппу,
используют также испытание, основанное на последовательном гидрировании (цинком
в хлороводородной кислоте) до ароматического амина с последующей его
конденсацией с n-диметиламинобензальдегидом
до образования окрашенной соли основания Шиффа. Хлорамфеникол в этих условиях
приобретает ярко-оранжевое окрашивание.
Наличие
исходных и промежуточных продуктов синтеза в хлорамфениколе устанавливают
методом ТСХ на пластинках Силуфол УФ-254 в системе хлороформ-метанол-вода
(90:10:1). На хроматограмме допускается наличие не более трех посторонних
пятен, каждое из которых не должно превышать пятно свидетеля по величине и
интенсивности (не более 0,5% каждой примеси).
В
хлорамфеникола натрия сукцинате определяют содержание примеси свободного
хлорамфеникола (не более 5%) методом диффузии в агар (ГФ XI,
в. 2. с. 210), устанавливая антимикробную активность. В хлорамфеникола стеарате
количественно определяют примесь свободной стеариновой кислоты (не более 3%)
методом нейтрализации по фенолфталеину.
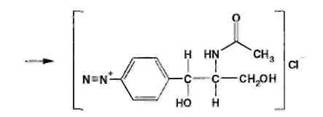
Количественное
определение хлорамфеникола по ФС выполняют нитритометрическим методом после
предварительного гидрирования в кислой среде цинковой пылью:

Содержание
хлорамфеникола определяют и обратным бромид-броматометрическим методом. Однако этому,
как и в случае нитритометрии, должна предшествовать стадия гидрирования
нитрогруппы в аминогруппу с помощью цинковой пыли и хлороводородной кислоты при
нагревании на кипящей водяной бане. Остаток цинка удаляют фильтрованием и к
фильтрату добавляют избыток 0,1 M
раствора бромата калия в присутствии бромидов. Количество непрореагировавшего
титранта устанавливают с помощью йодида калия. Выделившийся йод оттитровывают
0,1 М раствором тиосульфата натрия.
Количественное
определение хлорамфеникола стеарата выполняют спектрофотометрическим методом в
спиртовых растворах при длине волны 272 нм; он должен содержать 51-55%
хлорамфеникола. Хлорамфеникола натрия сукцинат также определяют
спектрофотометрическим методом, измеряя оптическую плотность 0,002%-ного
водного раствора при длине волны 276 нм. Расчет количественного содержания
выполняют относительно 0,002%-ного стандартного раствора, приготовленного из
отвечающего требованиям ФС хлорамфеникола. оптическую плотность которого
измеряют при той же длине волны. Содержание в нем хлорамфеникола должно быть
65,0-76,5%.
Реакция
образования комплексного соединения хлорамфеникола с ионом меди (II)
использована для прямого титрования хлорамфеникола 0,01 М раствором сульфата
меди (индикатор мурексид). Известны также аргентометрическое и меркуриметрическое
определение хлорамфеникола по хлорид-иону, образующемуся после его окисления
пероксидом водорода в щелочной среде. В результате этой реакции образуются две
молекулы хлорида натрия. Хлорид-ион можно получить и при озолении
хлорамфеникола в присутствии карбонатов натрия и калия.
Хлорамфеникол
и его сложные эфиры хранят по списку Б, в хорошо укупоренной таре
(хлорамфеникол в склянках оранжевого стекла), а хлорамфеникола натрия сукцинат
- в сухом, защищенном от света месте при комнатной температуре.
Хлорамфеникол
– антибиотик широкого спектра действия. Его применяют для лечения
брюшного тифа, паратифов, дизентерии, бруцеллеза, коклюша, пневмонии, различных
инфекционных заболеваний. Он легко всасывается из желудочно-кишечного тракта,
сохраняя при этом свою активность. Это позволяет использовать хлорамфеникол для
назначения внутрь обычно в дозах 0,5 г 3-4 раза в сутки. В детской практике
применяют менее горький хлорамфеникола стеарат, который в желудочно-кишечном
тракте постепенно гидролизуется с образованием хлорамфеникола. Показания для
применения хлорамфеникола стеарата те же, но, поскольку он всасывается
медленнее и содержит 51-55% хлорамфеникола, то дозы соответственно увеличивают
в 2 раза. Хлорамфеникола натрия сукцинат (растворимый) применяют аналогично, но
внутривенно, внутримышечно и подкожно 2-3 раза в сутки по 0,5-1,0 г в виде
растворов для инъекций.
Список
литературы
1. Анализ лекарственных
смесей. / А.П. Арзамасцев, В.М. Печенников, Г.М. Родионова и др. — М.:
Компания Спутник+, 2000. - 275с.
2. Арзамасцев AM.
Стандартные
образцы лекарственных веществ. / А.П. Арзамасцев, П.Л. Сенов. – М.: Медицина.
1978. – 248с.
3. Бабилев Ф.В. Полиморфизм
лекарственных веществ./Ф. В. Бабилев, И.Я. Андроник. – Кишинев: Штиница, 1981. –
239с.
4. Бабилев Ф.В. Применение
люминесценции в фармацевтическом анализе./Ф.В. Бабилев. – Кишинев: Штиница,
1977. – 120с.
5. Бычков В.Г. Дифференциальная
фотометрия. /В.Г. Беликов. — Ставрополь: Кн. изд-во, 1970. – 136с.
6. Беликов В.Г. Современные
синтетические и природные лекарственные средства: Кр. справочник. Изд. 2-е,
перераб. и доп. /В.Г. Беликов. - Пятигорск: Пятигорск, гос. фармац. акад..
2002. - 335с.
7. Белоусов Ю.Б. Клиническая
фармакология и фармакотерапия. /Ю.Б. Белоусов, B.C.
Моисеев, В.К. Лепахин. – М.: Универсум Паблишинг, 1997. – 531с.
8. Березовский В.М. Химия
витаминов. / В.М. Березовский. – М.: Пищевая промышленность, 1973. – 632с.
9. Берштейн И.Я. Спектрофотометрический
анализ в органической химии. / И.Я. Берштейн. Ю.Л. Каминский. – Л.: Химия.
1975. – 230с.
10. Булатов М.И. Практическое
руководство по фотоколориметрическим и спектрофотометрическим методам анализа.
/М.И. Булатов, И.П. Калинкин. – Л.: Химия, 1976. – 376с
11. Гауптман З. Органическая
химия. /3. Гауптман, Ю. Грефе, X.
Ремане. Пер. с нем. – М.: Химия, 1979. – 832с.
12. Государственная
фармакопея СССР. /М-во здравоохранения СССР. – 10-е изд. – М.: Медицина, 1968. –
1080с.
14. Государственный
реестр лекарственных средств. – М., 2001. – 1277с.
15. Джилкрист Т. Химия
гетероциклических соединений. /Т. Джилкрист. Пер. с англ. – М.: Мир, 1996. –
464с.
16. Дорохова Е.Н.
Аналитическая химия. Физико-химические методы анализа: Учеб. /Н.И. Дорохова,
Г.В. Прохорова. – М.: Высш. шк, 1991. – 256с.
17. Евстигнеева Р.П.
Тонкий
органический синтез: Учеб. пос. /Р.П. Евстигнеева. – М.: Химия, 1991. – 183с.
18. Егоров Н.С. Основы
учения об антибиотиках: Учеб. /Н.С. Егоров. – М.: Высш. шк.. 1986. – 448с.
19. Иванский В.И. Химия
гетероциклических соединений. /В.И. Иванский. – М.: Высш. шк.. 1978. – 559с.
20. Идентификация
органических соединений. /Р. Шрайнер, Р. Фьюзон, Д. Кертин, Т. Морил. Пер.
с англ. – М.: Мир, 1983. – 703с.
21. Кнорре Д.Г. Биологическая
химия: Учеб. /Д.Г Кнорре, С.Д. Мызина. – М.: Высш. шк., 1998. – 479с.
22. Крамаренко В.Ф. Химико-токсикологический
анализ: Практикум. /В.Ф. Крамаренко. – Киев: Вища шк., 1982. – 272с.
23. Кулешова М.И. Анализ
лекарственных форм, изготовляемых н аптеках. /М.И. Кулешова, Л.П. Гусева, O.K.
Сивицкая. 2-е изд. – М.: Медицина. 1989. – 287с.
24. Кулешова М.И. Пособие
по качественному анализу лекарств. /М.И. Кулешова, Л.Н. Гусева, O.K.
Сивицкая. – М.: Медицина, 1980. – 208с.
25. Лабораторные работы
по фармацевтической химии: Учеб. пос. для фармац. инт-ов и фармац. фак. мед.
ин-тов. /В.Г. Беликов, Е.И. Вергейчик, В.Е. Годяцкий и др. / Под ред.
В.Г. Беликова. – М.: Высш. шк., 1989. – 375с.
26. Лакин К.М. Биотрансформация
лекарственных веществ. /К.М.Лакин, Ю.Ф. Крылов. – М.: Медицина. 1981. – 344с.
27. Ланчини Д. Антибиотики.
/Д. Ланчини, Ф. Паренти. – М.: Мир, 1985. – 272с.
28. Машковский М.Д. Лекарства
XX века. /М.Д. Машковский. – М.:
Новая Волна, 1998. – 320с.
29. Машковский М.Д. Лекарственные
вещества. В 2-х тт. 14 изд. / М.Д. Машковский. – М.: Новая Волна, 2000. – Т.
1-2.
30. Международная
фармакопея. /ВОЗ. – 3-е изд. – М.: Медицина, 1981-1995. – Т. 1-4.
31. Мелентьева Г.А. Анализ
фармакопейных препаратов по функциональным группам. /Г.А. Мелентьева, А.А.
Цуркан, Т.Е. Гулимова. /Под ред. А.П. Арзамасцева. – Рязань, 1990.
32. Мелентьева Г.А. Фармацевтическая
химия. В 2-х т. /Г.А. Мелентьева. – М.: Медицина, 1976. – Т. 1-2.
33. Методы анализа
лекарств. /Н.П. Максютина, Ф.Е. Каган, Л.А. Кириченко, Ф.А. Митченко. – Киев:
Здоров'я. 1984. – 224с.
34. Методы
идентификации фармацевтических препаратов. /И.М. Максютина, Ф.Е. Каган, Ф.А.
Митченко и др. — Киев: Здоров'я, 1978. – 240с.
35. Некрасов Б.В. Основы
обшей химии. В 2-х т. / Б.В. Некрасов, — М.: Химия, 1974. – Т 1-2.
36. Общая химия.
Биофизическая химия. Химия биогенных элементов: Учеб. /Ю.А. Ершов, В.А.
Попков, А.С. Берлянд и др. – М.: Высш. шк., 1993. – 559с.
37. Орехов AM.
Химия
алкалоидов растений СССР. /А.П. Орехов. – М.: Наука, 1965. – 391с.
38. Основы
аналитической химии: В 2-х кн. /Под ред. Ю.А. Золотова. – М: Высш. шк.,
2000. – Кн. 1-2.
39. Пиккеринг У.Ф. Современная
аналитическая химия. /У.Ф. Пиккеринг. Пер. с англ. – М.: Химия, 1977. – 559с.
40. Погодина Л.И. Анализ
многокомпонентных лекарственных форм. /Л.И. Погодина. – Мн.: Вышейшая школа,
1985. – 240с.
41. Полюдек-Фабини
Р. Органический
анализ. /Р. Полюдек-Фабини, Т. Бейрих. Пер. с нем. – Л.: Химия, 1981. – 624с.
42. Пономарев В.Л. Математические
методы в фармации. /В.Д. Пономарев, ВТ. Беликов, Н.И. Коковкин-Щербак. – М.:
Медицина, 1983. –232с.
43. Райлс А. Основы
органической химии для студентов биологических и медицинских специальностей.
/А. Райлс, К. Смит, Р. Уорд. Пер. с англ. – М.: Мир, 1983. – 352с.
44. Регистр
лекарственных средств России: Энциклопедия лекарств: Ежегод. сб. – М.: РЛС,
2002. – Вып. 9. – 1504с.
45. Розенблит А.Б. Логико-комбинационные
методы в конструировании лекарств. /А.Б. Розенблит, B.E.
Голендер. – Рига: Зинатне, 1983. – 351с.
46. Рубцов М.В. Синтетические
химико-фармацевтические препараты: Справочник. /М.В. Рубцов, А.Г. Байчиков. –
М.: Медицина, 1971. – 328с.
47. Руководство к лабораторным
занятиям по фармацевтической химии: Учеб. пособие. /ЭМ. Аксенова, ОМ.
Адрианова, A.M.
Арзамасцев и др. – М: Медицина, 2001. – 384с.
48. Синев Д.М. Технология
и анализ лекарств. /Д.Н. Синев, И.Я. Гуревич. – Л.: Медицина, 1989. – 366с.
49. Слесарев В.И. Химия.
Основы химии живого: Учеб. /В.И. Слесарев. – СПб.: Химиздат, 2000. – 768с.
50. Солдатенков А.Т.
Основы органической химии лекарственных веществ. /А.Т. Солдатенков, Н.М.
Колядина, И.В. Шендрик. – М.: Химия, 2001. – 192с.
51. Справочник провизора-аналитика.
/Д.С. Волох, Н.М. Максютина, Л.А.Кириченко и др. – Киев: Здоровья, 1989.
– 200с.
52. Технология и
стандартизация лекарственных средств. /Под ред. В.П. Георгиевского, Ф.А.
Конева. – Харьков; ООО "Рирег", 1996. – 784с.
53. Тюкавкина Н.А. Биоорганическая
химия. /Н.А. Тюкавкина, Ю.И. Бауков. – М.: Медицина, 1985. – 480с.
54. Файгль Ф. Капельный
анализ органических веществ./Ф. Файгль. – М.: Госхимиздат, 1962. – 836с.
55. Харитонов Ю.Я. Аналитическая
химия (аналитика). В 2-х кн. /Ю.Я Харитонов. – М.: Высш. шк., 2001. – Кн. 1-2.
56. Харкевич Д.А. Фармакология:
Учеб. /Д.А. Харкевич. – М.: Издательский дом ГЭОТАР-МЕД, 2001. – 664с.
57. Холодов Л.Е. Клиническая
фармакокинетика. /Л.Е. Холодов, В.П. Яковлев. – М.: Медицина, 1985. – 464с.
58. Шаршунова М. Тонкослойная
хроматография в фармации и клинической биохимии. В 2-х ч. / М. Шаршунова, В.
Шварц, Ч. Михалец. Пер. со словац. – М.: Мир, 1980. – Ч. 1-2.
59. Шашкова Г.В, Справочник
синонимов лекарственных средств. /Г.В. Шашкова, В.К. Лепахин, Г.Н. Колесникова.
– М.: РЦ "Фармединфо", 2001. – 480с.
60. Энциклопедический
словарь лекарственных растений и продуктов животного происхождения. /Под ред. Г.М.
Яковлева, К.Ф. Блиновой. – СПб.: Спец. лит., 1999. – 407с.
61. Юинг Г. Инструментальные
методы химического анализа. /Г. Юинг. Пер. с англ. – М.: Мир, 1989. – 608с.
62. Яхонтов Л.М. Синтетические
лекарственные средства. /Л. Н. Яхонтов, Р.Г. Пашков. – М.: Медицина, 1983. –
272с.