Экологические проблемы бытовой химии
Министерство образования Российской Федерации
Государственное образовательное учреждение
высшего профессионального образования
Дальневосточный Государственный Гуманитарный
Университет
биолого-химический факультет
кафедра химии
кафедра
Выпускная квалификационная работа
На тему
«Экологические проблемы бытовой
химии»
Работу выполнила студентка
5 курса ОЗО БХФ
Русакова В.Г.
Научные руководители:
Доцент к.х.н.: Крупина Т.С.
Хабаровск - 2006
Содержание
Введение
……………………………………………………………………..3
Глава1. Меры безопасности при
использовании химических веществ…..
1.1.Хранение и правила
применения……………………………………
1.2.Опасность при
использовании………………………………………
Глава2.Классификация предметов
бытовой химии и их краткая характеристика……………………………………………………………………..
Глава3.Мыла и моющие средства………………………………………………..
Глава4.Синтетические моющие средства………………………………………..
4.1.Вспомогательные
средства для стирки:
4.1.1.Оптические
отбеливатели……………………………………………….
4.1.2.Химические
отбеливатели……………………………………………….
4.1.3.Отбеливающие
ферменты……………………………………………….
4.1.4. Смягчители
……………………………………………………………..
4.1.5.Пенообразователи……………………………………………………….
4.1.6.Подкрахмаливающие и
аппретирующие средства……………………
4.1.7.Антистатики…………………………………………………………….
Глава5.Химические средства гигиены и
косметики……………………………
5.1.Средства ухода за
зубами………………………………………………..
5.2.Косметические
средства………………………………………………….
5.3.Дезодоранты и озоновый
«щит планеты»……………………………….
Заключение…………………………………………………………………….
Приложения……………………………………………………………………
Список литературы…………………………………………………………….
Введение
Везде и всегда – на работе и дома, в
огороде и в деревне – повсюду нас окружает всемогущая химия и рожденные ею
вещества и материалы. В этом огромном количестве химических продуктов можно
выделить особую категорию – препараты бытовой химии.
Быстрое развитие химической
промышленности вызвало к жизни появление огромного количества разнообразных
товаров бытовой химии, которые получили широкое признание. С помощью этих
препаратов мы куда легче, чем когда-то, стираем, подсиниваем и подкрахмаливаем
белье, чистим ковры и одежду, красим, клеим, ухаживаем за растениями в комнате
и на приусадебном участке и т.д.
Популярность товаров бытовой химии
неуклонно растет, расширяются их применения, и увеличивается выпуск.
Использование химических веществ в
быту – отнюдь не изобретение нашего времени, детищем которого является
промышленность бытовой химии. Есть немало сведений о том, что еще задолго до
нашей эры люди применяли хотя и несовершенные, но все же достаточно эффективные
химические вещества.
Так, в древних рукописях можно найти
упоминания о маслах и составах для полирования дерева и камня, средствах для
дезинфекции и о средствах для консервирования пищи и др. С незапамятных времен
известно и составление рисовых красок. В гробнице египетского фараона
Тутанхамона археологи обнаружили благовония, сохранившие аромат в течение
тридцати веков. Вообще в далеком прошлом химические вещества особенно часто
применялись в культовых обрядах и в косметике. Во время религиозных церемоний в
курильницах зажигали благовонные смеси. Восточные поэты воспевали насурьмленных
красавиц. Мумии египетских фараонов сохранились до наших дней, так как тела их
были хорошо забальзамированы.
Начиная с I века до н.э. в культурных центрах Средиземноморья широкое
распространение получило мыло. Немало рецептов бытовых химических препаратов
существовало в то время в Индии, Китае, в государствах Средней Азии и
Закавказья. Широко использовались химические средства в повседневной жизни в
средние века. Развитие городов, ремесел, торговых связей в немалой степени
этому способствовало. Химические средства с древних времен применялись и на
Руси. Особенно развито было солеварение, обработка и выделка кож, переработка
пчелиного воска.
С развитием письменности появляются и
советы по бытовой химии. Так, в одном из старинных русских лечебников дается
такой совет: «если хочешь, чтоб тебя не ели комары, то возьми платок, смочи его
дегтем и положи на голову, на шапку». С древних времен применялся для стирки
щелок, который готовили из древесной золы; широко был распространен и
сохранился до наших дней способ отбеливания путем попеременного замачивания и
выстеливания их на солнце.
Издавна люди научились применять для
чистки изделий из цветных металлов подручные средства, причем некоторые из них
не потеряли своего назначения до сих пор. Конечно большинство таких рецептов,
удачно и обычно случайно найденных, передавались от отца к сыну. Многие
открытия держались в строгом секрете, особенно это относится к работам
алхимиков. Любопытно отметить, один из первых патентов в мире имел прямое
отношение к бытовой химии. Речь идет об английском патенте №4 от 1617г., в котором
предлагается новый способ защиты доспехов от ржавчины с помощью покрытия их
специальным маслом.
Более поздние достижения бытовой
химии хорошо известны и многие из них сохранили свое значение до наших дней.
Безусловно, они были связаны с успехами химии, с появлением возможности
применять более или менее чистые химические вещества или смеси таких веществ,
использовать химические продукты, которые стала выпускать промышленность в
конце XVIII - в начале XIX века.
Как известно, несмотря на выдающиеся
открытия русских ученых-химиков, химическая промышленность в царской России
была развита слабо; многие химические препараты ввозили из-за рубежа. Только в
годы первых пятилеток была заложена основная база химической промышленности.
Однако потребность народного хозяйства в многочисленных химических продуктах, в
том числе предназначенных для быта, удовлетворялась далеко не полностью. Хотя
объем производства товаров бытовой химии все же неуклонно возрастал,
ассортимент их оставался бедным, высоко качественных препаратов выпускалось
мало.
Необыкновенно бурное развитие
химической промышленности в последние десятилетия и в месте с тем рост
потребностей и запросов современного человек привели к резкому увеличению
выпуска продукции бытовой химии. Что надо знать о товарах бытовой химии?
Товар и препарат – это не одно и
тоже. Препарат – это химическое вещество или смесь веществ, применяемые для
определенных целей в индивидуальном виде или как составная часть. Он расфасован
в соответствующую упаковку, предназначен для розничной (или оптовой) продажи.
Товаром бытовой химии он становится, как попадает в торговую сеть.
Актуальность этой темы состоит в том,
что ассортимент бытовой химии постоянно обновляется и расширяется как
отечественными, так и зарубежными видами препаратов. Менее эффективные уступают
дорогу более эффективным, более опасные – менее опасным для здоровья и
окружающей среды. При этом меняется не только внешний вид, название, но и
химический состав.
Цель данной работы - расширить знания
о применении бытовой химии в повседневной жизни.
Задачи:
1. Рассмотреть классификацию препаратов
бытовой химии.
2. Рассмотреть краткую характеристику
предметов бытовой химии.
3. Изучить меры безопасности при
использовании химических веществ.
4. Изучить правила хранения и правила
применения химических веществ.
5. Познакомиться с некоторыми предметами
бытовой химии, такими как мыла и моющие средства, синтетические моющие средства,
средства гигиены и косметики.
6. Выявить некоторые экологические
проблемы, связанные с использованием предметов бытовой химии.
Чтобы легче ориентироваться в
огромном разнообразии товаров бытовой химии, необходимо их классифицировать.
Разумеется, все товары различаются по
своему химическому составу, а следовательно, по степени опасности, которую они
могут представить для людей и окружающей среды при неумелом использовании.
Глава 1. Меры безопасности при
использовании химических веществ.
1.1.
Хранение и
правила применения
Все средства бытовой химии, даже если
это обычный стиральный порошок или сода, должны храниться так, чтобы до них не
могли добраться маленькие дети. Эти средства следует обязательно хранить
отдельно от любых пищевых продуктов.
Средства, опасные в пожарном
отношении, должны стоять в закрытых склянках, далеко от источников тепла или
огня, желательно – в прохладном месте. Если с бутылки или банки с таким
средством слетела этикетка, надо немедленно наклеить ее или изготовить заново.
Вообще этикетками с четкой, разборчивой надписью должны быть снабжены все
упаковки с химическими веществами.
При работе с пожароопасными
средствами нельзя зажигать газовые горелки, спички, нельзя курить, пользоваться
электронагревательными приборами. Надо помнить, что особо взрывоопасны пары
горючих жидкостей. Поэтому лучше всего работать с подобными средствами на
воздухе.
Средства, содержащие в больших
количествах агрессивные химические вещества (соляную кислоту, щелочи и др.),
должны обязательно храниться закрытыми и иметь этикетку. При работе сними надо
надеть резиновые перчатки, очки, после завершения работы надо хорошо вымыть
руки водой с мылом и перчатки, и руки.
Жидкие вещества следует переливать,
обязательно пользуясь воронкой, а сыпучие перекладывать ложкой. При этом надо
беречь глаза от попадания в них брызг или мелкого порошка. Воронку и ложку
после употребления следует вымыть и высушить; хранить лучше в том же месте, где
хранятся химические препараты.
Следует помнить, что при разбавлении
серной кислоты ее надо лить в воду, а не наоборот.
Нельзя низко наклоняться над сосудами
с химикатами (а тем более нюхать их, сильно втягивая воздух) и над кипящей
жидкостью, особенно при вливании в нее новой порции или всыпании порошка.
Горячие жидкости нельзя вливать в обычную толстостенную стеклянную посуду.
Особые правила предосторожности надо
соблюдать при работе с аэрозольными баллонами. Хранить аэрозольные баллоны
следует в вертикальном положении в прохладном месте, удаленном от источников
тепла. На баллоны не должны попадать прямые солнечные лучи. При распылении из
баллона нельзя курить, зажигать газовые горелки. Баллоны нельзя вскрывать и не
рекомендуется выбрасывать до полного удаления содержимого.
Все работы с ядохимикатами надо
производить в специальной одежде – халате, фартуке и в резиновых перчатках.
Рекомендуется также пользоваться защитными очками (особенно при работе с
ядовитыми веществами на открытом воздухе). После всего рабочую одежду надо
выстирать.
Некоторые вещества при смешивании
реагируют друг с другом, выделяя иногда большое количество тепла, поэтому
возможны вспышки или воспламенения; другие вещества после смешивания превращаются
в новые, с иными свойствами и становятся не пригодными к употреблению. Такие
вещества называются несовместимыми, их ни в коем случае нельзя смешивать.
·
Нашатырный спирт
(аммиак) и нашатырь (хлористый аммоний) несовместимы с формалином и йодом.
·
Бура несовместима
с нашатырем, серной и соляной кислотами.
·
Йод несовместим с
нашатырным спиртом.
·
Серная и соляные
кислоты несовместимы с кальцинированной и питьевой содой, известью, молом,
щелочами.
·
Сера несовместима
с марганцовокислым калием, хлорной известью.
·
Хлорная известь
несовместима с жирами, маслами, глицерином, нашатырным спиртом, нашатырем,
органическими растворителями.
Итак, соблюдение всех перечисленных
выше простых правил, а также инструкций, имеющихся на упаковке каждого
химического препарата, гарантирует полную безопасность при работе с такими
препаратами.
1.2. Опасность при
использовании
Препараты бытовой химии при
неправильном их использовании, могут служить причиной отравлений, ожогов и т.д.
Хранение их в неположенном месте, в посуде без этикеток, использование без
соблюдения мер техники безопасности могут способствовать попаданию их в пищевые
продукты.
При сильном разбрызгивании жидких
химических веществ или распылении порошков мелкие частицы могут попасть на
слизистые оболочки глаз и дыхательных путей и вызвать их воспаление, а также
стать причиной общего отравления. Очень опасно, когда бытовые средства,
содержащие ядовитые вещества, случайно попадая в желудочно-кишечный тракт,
всасываются в кровь.
Отравление химическими веществами
случается и в результате их небрежного хранения (негерметичность тары,
доступность для маленьких детей и т.д.).
Некоторые вещества при смешивании
выделяют много тепла, что нередко грозит воспламенением. Жидкие вещества
бытовой химии нельзя переливать в бутылки из-под напитков, уксуса,
растительного масла, лекарственных препаратов и в другую посуду, откуда они по
ошибке могут быть использованы внутрь.
Каждый из препаратов бытовой химии
имеет свои особенности. Ядовитость вещества зависит от химического состава,
летучести, стойкости во внешней среде, растворимости в воде и органических
растворителях. Определенное значение имеет и то, находится препарат в жидком,
твердом состоянии или в виде аэрозоля. Имеет значение способ применения и
количество расходуемого вещества. Все эти особенности необходимо учитывать и
принимать в каждом случае меры предосторожности.
Через дыхательные пути внутрь чаще
попадают ядовитые вещества, которые находятся в парообразном состоянии: в виде
туманов, газов, аэрозолей.
Даже при одних и тех же условиях
разные люди неодинаково чувствительны к ядам. У одних симптомы отравления
появляются очень скоро, у других – позднее, а некоторые вообще могут не
предъявлять жалоб.
Влияние химических веществ на
организм человека усиливается под воздействием факторов окружающей среды
(влажность, температура, скорость ветра и т.п.).
В торговую сеть поступают препараты
только средней и малой токсичности, но если и их неправильно применять, то тоже
может произойти отравление.
Дозы яда могут быть смертельными,
действующими – и минимально действующими. Первые вызывают гибель, а последние
действуют на организм, вызывая ту или иную степень отравления. Недействующие
дозы и концентрации ядов не влияют на функции организма. Это те минимальные
количества, с которыми можно работать, не боясь отравления. Однако и эти малые
дозы могут концентрироваться в печени, почках, сердце, в крови, в нервной
системе, оказывать влияние на их функции.
Глава 2. Классификация препаратов
бытовой химии.
1. По назначению
·
Моющие средства
·
Чистящие
·
Дезинфицирующие
средства
·
Уход за мебелью
·
Уход за полом
·
Борьба с бытовыми
насекомыми
·
Средства защиты
растений
·
Универсальные
средства
·
Средства гигиены
и косметики
2. По агрегатному состоянию
·
Жидкие (также
суспензии и эмульсии)
·
Твердые
(порошкообразные, гранулированные и таблетированные)
3. По концентрации
·
Готовые к
употреблению
·
Концентрированные
4. По использованию
·
Одноразовые
·
Многоразовые
5. По степени потенциальной опасности
·
Безопасные
·
Огнеопасные
·
ядовитые
Товары бытовой химии выпускают также
в виде паст и памадообразных препаратов (дезодорирующие и клеящие карандаши и
ид.).
Препараты одного и того же назначения
могут различаться по способу применения.
Так, синтетические моющие средства
могут предназначаться как для машинной, так и для ручной стирки. Как для
белого, так и для черного белья. Необходимо помнить, что любой химический
препарат действует эффективно только в определенных условиях, которые всегда
указаны в прилагаемой инструкции или на упаковке.
Существуют препараты узкого целевого
назначения, например, отбеливатели, предназначенные для отбеливания льняных и
хлопчатобумажных тканей. Бывают также препараты нескольких целевых назначений.
Так, некоторые отбеливатели можно применять и как дезинфицирующие средства.
Необходимо сказать и об упаковках, в
которых выпускают товары бытовой химии. Наиболее удобны товары в аэрозольных
баллонах. Также удобны многие виды упаковок в виде пластмассовых флаконов,
банок и фляг, многие товары выпускают в стеклянных или металлических банках, в
пакетах из полимерных пленок и из дублированных материалов, в картонной
упаковке. Конечно, во всех случаях учитывается специфика препарата – его
химический состав, агрегатное состояние, срок хранения – соответственно
подбирают тару, т.е. упаковку. Принимаются во внимание и удобства хранения и использования.
С формой упаковки связано и наличие
или отсутствие функциональных приспособлений. Некоторые из них очень просты, но
создают дополните6льные удобства – например, мерные колпачки для жидких моющих
средств и других концентрированных препаратов, мерные стаканы для дозирования
СМС, поролоновая подушечка для нанесения пасты, распылитель и др.
Глава
3. Мыла и моющие средства.
Мыло было известно человеку до новой эры летоисчисления.
Ученые не располагают информацией о начале приготовления мыла в арабских
странах и Китае. Самое раннее письменное упоминание о мыле в европейских
странах встречается у римского писателя и ученого Плиния Старшего
(23...79 гг.). В трактате «Естественная история» (в 37 томах), который, по
существу, был энциклопедией естественнонаучных знаний античности, Плиний писал
о способах приготовления мыла омылением жиров. Мало того, он писал о твердом и
мягком мыле, получаемом с использованием соды и поташа соответственно. Раньше
для стирки одежды использовали щелок, получающийся от обработки золы водой.
Скорее всего, это было до того, как стало известно, что зола от сжигания
топлива растительного происхождения содержит поташ.
Развитию мыловарения способствовало наличие сырьевых
источников. Например, марсельская мыловаренная промышленность, известная с
эпохи раннего средневековья, располагала оливковым маслом и содой. Оливковое
масло получают простым холодным прессованием плодов масличных деревьев. Масло,
получаемое после первых двух прессовок, употребляли для пищевых целей, а после
третьей – использовали для переработки на мыло. Марсельское мыло было важным
товаром торговли уже в IX в. оно уступило свое место международной
торговле венецианскому мылу лишь с конца средних веков (XIV в.) кроме
Франции, мыловарение в Европе развивалось в Италии, Греции, Испании, на Кипре,
т.е. в районах, культивирующих оливковые деревья. Первые германские мыловарни
были основаны в XIV столетии.
Несмотря на то, что в конце эпохи средневековья в разных
странах существовала довольно развитая мыловаренная промышленность, химическая
сущность процессов, конечно, была не ясна. Лишь на рубеже XVIII и XIX вв.
была выяснена химическая природа жиров и внесена ясность в реакцию их омыления.
В 1779 г. шведский химик Шееле показал, что при взаимодействии оливкового
масла с оксидом свинца и водой образуется сладкое и растворимое в воде
вещество. Решающий шаг на пути изучения химической природы жиров был сделан
французским химиком Шеврелем. Он открыл стеариновую, пальмитиновую и олеиновую
кислоты, как продукты разложения жиров при их омылении водой и щелочами.
Сладкое вещество, полученное Шееле, было Шеврелем названо глицерином. Сорок лет
спустя Бертло установил природу глицерина и объяснил химическое строение жиров.
Глицерин – трехатомный спирт. Жиры – сложные эфиры глицерина (глицериды)
тяжелых одноосновных карбоновых кислот, преимущественно пальмитиновой CH3(CH2)14COOH,
стеариновой CH3(CH2)16COOH и олеиновой CH3(CH2)7CH = CH(CH2)7COOH.
Их формулу и реакцию гидролиза можно описать следующим образом:
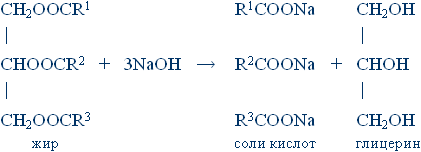
В состав различных жиров входят в различных соотношениях
пальмитиновая, стеариновая, олеиновая и другие кислоты. В растительных (жидких)
жирах преобладают непредельные кислоты (содержащие этиленовые связи). В
животных (твердых) – предельные кислоты, т.е. не содержащие двойных связей.
Потребности в твердых животных жирах большие, чем в растительных. Поэтому
жидкие растительные жиры переводят в твердые каталитической гидрогенизацией. В
этом процессе остатки непредельных кислот в глицеридах превращаются
(присоединением водорода) в остатки предельных кислот. Например:
CH3(CH2)7CH = CH(CH2)7COOH
|
[катализатор 190...240°C]
↓
CH3(CH2)7CH2 – CH2(CH2)7COOH
Именно так получают кулинарные жиры, масло для обжаривания,
салатное масло, а также жиры, идущие на производство маргарина. Гидрированные
жиры называют саломаслами (сало из масла).
Важно
то, что среди остатков различных кислот в глицеридах (жирах) присутствует
остаток линолевой кислоты CH3(CH2)4CH = CHCH2CH2CH = CH(CH2)7COOH.
В отличие от других эта кислота не синтезируется в организме
человека, а вводится только с пищей. В настоящее время существует утвердившееся
мнение, что линолевая кислота необходима для предотвращения атеросклероза –
распространенной болезни, служащей одной из главных причин потери
трудоспособности и преждевременной смерти. Необходимо отметить, что линолевая
кислота непредельная, а значит, она входит в состав главным образом
растительных жиров.
В быту, не говоря о промышленности, мойке подвергают разные
предметы и объекты. Загрязняющие вещества бывают самые разнообразные, но чаще
всего они малорастворимы или нерастворимы в воде. Такие вещества, как правило,
являются гидрофобными, поскольку водой не смачиваются и с водой не
взаимодействуют. Поэтому нужны и различные моющие средства.
Если попытаться дать определение, то мытьем можно назвать
очистку загрязненной поверхности жидкостью, содержащей моющее вещество или
систему моющих веществ. В качестве жидкости в быту используют главным образом
воду. Хорошая моющая система должна выполнять двойную функцию: удалять
загрязнение с очищаемой поверхности и переводить его в водный раствор. Значит,
моющее средство также должно обладать двойной функцией: способностью
взаимодействовать с загрязняющим веществом и переводить его в воду или водный
раствор. Следовательно, молекула моющего вещества должна иметь гидрофобную и
гидрофильную части. Фобос – по-гречески означает страх, боязнь. Значит,
гидрофобность означает боящийся, избегающий воду. Филео – по-гречески – люблю,
а гидрофильность – любящий, удерживающий воду. Гидрофобная часть молекулы
моющего вещества обладает способностью взаимодействовать с поверхностью
гидрофобного загрязняющего вещества. Гидрофильная часть моющего вещества
взаимодействует с водой, проникает в воду и увлекает с собой частицу
загрязняющего вещества, присоединенную к гидрофобному концу.
Таким образом, моющие вещества должны обладать способностью,
адсорбироваться на пограничной поверхности, т.е. обладать поверхностной
активностью. Их называют поверхностно-активными веществами (ПАВ).
Соли тяжелых карбоновых кислот, например CH3(CH2)14COONa,
являются типичными поверхностно-активными веществами. Они содержат гидрофильную
часть (в данном случае – карбоксильную группу) и гидрофобную часть (углеводородный
радикал).
Животные жиры – древнее и весьма ценное сырье мыловаренной
промышленности. Они содержат до 40% (насыщенных) жирных кислот. Искусственные,
т.е. синтетические, жирные кислоты получают из парафина нефти каталитическим
окислением кислородом воздуха. В упрощенном виде реакцию можно описать
следующим уравнением:
CH3(CH2)mCH2 – CH2(CH2)nCH3 + 2,5O2
↓
CH3(CH2)mCOOH + CH3(CH2)nCOOH + H2О
Молекула парафина при окислении разрывается в разных местах и
потому получается смесь кислот, которые разделяются на фракции. При
производстве мыла используют две фракции: C10–C16 и C17–C20.
В хозяйственное мыло синтетические кислоты вводят в количестве 35...40%. Для
производства мыла также применяют нафтеновые кислоты, выделяемые при очистке
нефтепродуктов (бензина, керосина и др.). С этой целью нефтепродукты
обрабатывают раствором гидроксида натрия и получают водный раствор натриевых
солей нафтеновых кислот (монокарбоновые кислоты ряда циклопентана и
циклогексана). Этот раствор упаривают и обрабатывают поваренной солью, в
результате чего на поверхность раствора всплывает мазеобразная масса темного
цвета – мылонафт. Для очистки мылонафт обрабатывают серной кислотой, т.е.
вытесняют из солей сами нафтеновые кислоты. Этот нерастворимый в воде продукт
называют асидолом или асидол-мылонафтом. Непосредственно из асидола можно
изготавливать только жидкое или, в крайнем случае, мягкое мыло. Оно имеет
нефтяной запах, но зато обладает бактерицидными свойствами.
Процесс производства мыла состоит из химической и
механической стадий:
·
На первой стадии
(варка мыла) получают водный раствор солей натрия (реже калия) жирных кислот
или их заменителей (нафтеновых, смоляных).
·
На второй стадии
проводят механическую обработку этих солей – охлаждение, сушку, смешивание с
различными добавками, отделку и упаковку.
Варку мыла заканчивают обработкой мыльного раствора (мыльного
клея) избытком щелочи (NaOH) или раствором NaCl. В результате этого на
поверхность раствора всплывает концентрированный слой мыла, называемый ядром.
Полученное таким образом мыло называют ядровым, а процесс его выделения из
раствора – отсолкой или высаливанием. При высаливании происходит повышение
концентрации мыла и его очистка от белковых, красящих и механических примесей –
так получают хозяйственное мыло.
Если мыло варилось из животных или растительных жиров, то из
раствора после отделения ядра выделяют образующийся в результате омыления
глицерин. Он находит широкое и разнообразное применение: в производстве
взрывчатых веществ (тринитроглицерина) и полимерных смол; в качестве умягчителя
тканей и кожи; для парфюмерных, косметических и медицинских препаратов; при
производстве кондитерских изделий и ликеров. Последним он придает вязкую
консистенцию.
Для получения особо чистого и светлого мыла его очищают
(шлифуют) переведением снова в раствор кипячением с горячей водой и повторным
высаливанием. В результате шлифования мыло приобретает большую однородность,
низкую вязкость и надлежащую пластичность. Для изготовления туалетного мыла в
очищенном ядровом мыле снижают содержание воды от 30 до 12%. Затем в него
вводят парфюмерные отдушки, отбеливатели типа TiO2, красители и др.
Хорошие сорта туалетного мыла содержат до 50% мыла, полученного из импортного
кокосового или пальмового масла. Кокосовое масло хорошо растворяется в холодной
воде и характеризуется высоким пенообразованием. Иногда туалетное мыло содержит
до 10% свободных жирных кислот. Самое дорогое туалетное мыло целиком
изготавливают из кокосового масла.
Для улучшения некоторых характеристик хозяйственного мыла
(иногда и туалетного), а также для удешевления в него вводят наполнители. К ним
относятся некоторые натриевые соли (Na2CO3, Na2B4O7,
Na5P3O10, жидкое стекло), которые при
растворении в воде приводят к подщелачиванию, клеи (казеин, казеиновый
студень), углеводы (крахмал). Клеи и крахмал способствуют пенообразованию
мыльного раствора и стойкости пены, однако моющей способностью не обладают. Для
получения паст в жидкое хозяйственное мыло вводят тонкоизмельченный песок,
толченый кирпич, жирные глины. Они способствуют механической очистке. Такие
мыла применяют для чистки кухонной посуды, некрашеной мебели, полов и т.д.
Особое место среди наполнителей занимает сапонин, получаемый
выщелачиванием некоторых растений и, прежде всего мыльного корня. Он хорошо
растворяется в воде, и его растворы сильно пенятся. Поэтому сапонин используют
для улучшения пенообразования и применяют для дорогих сортов мыл.
Следует отметить, что замена натрия на калий приводит к
изменению консистенции мыла. Из твердого оно становится мягким или
мазеобразным.
Ионы кальция и магния образуют с анионами тяжелых карбоновых
кислот малорастворимые соли. Этот процесс можно выразить уравнениями:
2RCOONa + Ca(HCO3)2 = Ca(RCOO)2 + 2NaHCO3
2RCOONa + MgCl2 = Mg(RCOO)2 + 2NaCl
Поэтому при стирке белья в жесткой воде, содержащей эти ионы,
расход мыла повышается на 25...30%. Малорастворимые соли кальция и магния
оседают на ткани, забивают поры и потому делают ткань грубой, менее эластичной,
с плохой воздухо- и влагопроницаемостью. Такие ткани приобретают сероватый
оттенок, а окраска становится блеклой. Кроме того, осевшие на ткани известковые
мыла приводят к снижению ее прочности. Это происходит потому, что анионы
ненасыщенных карбоновых кислот при сушке тканей окисляются кислородом воздуха с
образованием веществ пероксидного характера. Они же окисляют целлюлозу, из
которой состоят ткани. Для устранения вредных последствий жесткой воды в мыла
вводят натрийтрифосфат Na5P3O10. Анион P3O510–
связывает ионы Ca2+ и Mg2+ в прочные, но растворимые в
воде соединения. По существу они играют роль умягчителя воды. С этой же целью
натрийтрифосфат и другие полифосфатные анионы добавляют и в стиральные порошки.
Кроме использования мыла в качестве моющего средства оно
широко применяется при отделке тканей, в производстве косметических средств,
для изготовления полировочных составов и водоэмульсионных красок. Имеется и не
столь безобидное его применение. Алюминиевое мыло (алюминиевые соли смеси
жирных и нафтеновых кислот) применяют в США для получения некоторых видов
напалма – самовоспламеняющегося состава, используемого в огнеметах и
зажигательных авиабомбах. Само слово напалм происходит от начальных слогов нафтеновой
и пальмитиновой кислот. Состав напалма довольно простой – это бензин,
загущенный алюминиевым мылом.
Глава 4. Синтетические моющие средства
В настоящее время химическая промышленность выпускает большое
количество различных синтетических моющих средств. Наибольшее практическое
значение имеют соединения, содержащие насыщенную углеводородную цепь из 10...15
атомов углерода, так или иначе связанную с сульфатной или сульфонатной группой,
например

Производство синтетических моющих средств основано на дешевой
сырьевой базе, а точнее на продуктах переработки нефти и газа. Они, как
правило, не образуют малорастворимых в воде солей кальция и магния.
Следовательно, многие из синтетических моющих средств
одинаково хорошо моют как в мягкой, так и в жесткой воде. Некоторые средства
пригодны даже для стирки в морской воде. Синтетические моющие средства
действуют не только в горячей воде, как это характерно для хозяйственного мыла,
но и в воде при сравнительно низких температурах, что важно при стирке тканей
из искусственных волокон. Наконец, концентрация синтетических моющих веществ
даже в мягкой воде может быть гораздо ниже, чем мыла, полученного из жиров.
Стиральные порошки можно условно разделить на следующие
группы:
1.
Собственно
стиральные средства: универсальные (для всех видов ткани): для стирки
шерстяных, шелковых и синтетических тканей; для предварительного замачивания
белья.
2.
Средства
комплексного действия, с помощью которых можно одновременно со стиркой
дополнительно обработать ткань, например, подкрасить и продезинфицировать ее.
Это чаще используется при ручной стирке.
3.
Отбеливатели. Они
способствуют удалению с тканей окрашенных пятен, оставшихся после стирки, а
также придают белью дополнительную белизну.
4.
Подсинивающие
средства.
5.
Средства
антистатической обработки. Применяются при последнем полоскании выстиранных
изделий из капрона, нейлона, ацетатного волокна и шерсти.
6.
Смягчители. Используются
при последнем полоскании изделий и придают тканям из хлопка, льна и вискозных
волокон приятное ощущение бархатистости.
7.
Аппретирующие
средства. Ими пропитывают ткани после стирки для возвращения прежних свойств,
ослабленных стиркой. Например, в связи с удалением части крахмала, а также веществ,
способствующих водоотталкиванию, используют подкрахмаливающие и гидрофобирующие
средства. К этой группе относятся также препараты, обладающие
грязеотталкивающими свойствами и делающие ткани несминаемыми.
Более подробно эти группы рассмотрим далее.
Для удаления жирных загрязнений в моющее средство включают
щелочные добавки, например, соду или жидкое стекло (соль кремниевой кислоты). Многие
загрязнения, особенно белкового происхождения, отстирываются очень плохо. Для
облегчения процесса в стиральные порошки добавляют энзимы (ферменты) – вещества
биологического происхождения. И к названию порошка добавляется приставка «био».
В отличие от мыла СМС обладают большой моющей способностью,
гигиеничностью, экономичностью и целым рядом других преимуществ. Они способны
при растворении в воде лучше, чем мыло, смачивать обрабатываемые поверхности,
другими словами, увеличивать поверхностную активность воды, являясь более
сильными поверхностно-активными веществами, и, кроме того, измельчать
загрязнение на такие частички, которые удерживаются в водном растворе во
взвешенном состоянии и не оседают на предмет, подлежащий обработке.
Необходимо помнить, что у некоторых людей синтетические
моющие средства вызывают раздражение кожи, зуд, покраснение и отек. Поэтому
лицам с повышенной чувствительностью к химическим веществам, страдающим
аллергией, бронхиальной астмой, крапивницей, экземой, пользоваться СМС нужно
особенно осторожно, тщательно соблюдая правила указанные на упаковке.
С добрым старым мылом наши женщины еще и сегодня стояли бы у
корыта. Поэтому химики своевременно обратили свое внимание на новые моющие
вещества. Ими оказались сульфаты жирных спиртов (фева,1930г.) и
алкилбензолсульфонаты, которые начали употребляться в Германии во время второй
мировой войны. Сегодняшние моющие средства – это смесь веществ. Их компонентами
являются поверхностно-активные вещества, комплексообразователи, оптические
осветители, отбеливатели и различные вспомогательные вещества. Мыло содержится
в них в очень небольшом количестве и то не как моющий агент, а как
обеспениватель. Поверхностно-активные вещества, хотя они и не составляют
количественно основную массу смеси, имеют решающее значение для качества
стирки. Их назначение – уменьшить поверхностное натяжение воды, улучшить
смачиваемость ткани и повысить эмульгатируемость пенообразователей.
Все молекулы поверхностно-активных веществ гидрофильные и
гидрофобные части. По заряду активной части молекулы различают анионные
(например, карбоксилаты, сульфаты и сульфонаты), катионные (большей частью высокомолекулярные
азотосодержащие соединения) и неионогенные поверхностно-активные вещества.
Варьирование составных частей, длины цепи и расположения полярных групп в
молекулах поверхностно-активных веществ приводит к многообразованию товарной
продукции.
Таблица №1 Состав современных моющих средств.
|
Компонент
|
Содержание в %
|
Назначение
|
|
Поверхностно-активные
вещества
|
10-15
|
Смачивание
волокон, вскрытие слоя грязи
|
|
Мыло
|
0-10
|
Регулирование
пенообразования
|
|
Полифосфаты
|
20-50
|
Связывание накипеобразователей(т.е. солей,
обуславливающих жесткость воды), усиление действия поверхностно-активных
веществ
|
|
Перборат натрия
|
10-30
|
Отбеливание при температуре выше 80
градусов
|
|
Карбонат и
силикат натрия
|
5-10
|
Щелочной буфер
|
|
Карбоксиметилцеллюлоза
|
0,5-2
|
Предотвращение повторного осаждения
эмульгированной грязи на волокна ткани
|
|
Нейтральные соли
|
5-20
|
Придание порошку сыпучести
|
|
Отдушки
|
0-0,5
|
Дезодорация
|
|
Производные
стильбена и пиразолена
|
0,1-0,3
|
Оптическое осветление
|
|
Вода
|
3-12
|
|
|
Ферменты,
красители, антимикробные средства
|
В некоторых случаях, очень малые количества
|
Различное
|
Катионные поверхностно-активные вещества пока еще имеют
второстепенное значение. В основном они используются как пластификаторы в
моющих средствах.
Современные моющие средства содержат 30-50% пентанатрий-ди
(или три) фосфата (например, Na5 P3O10*6H2O) и некоторое
количество полифосфатов. Они так прочно связывают двух- и трехзарядные ионы
металлов, что устраняют серый налет на белье и полосы грязи в ванных, связанные
с образованием известкового мыла и других труднорастворимых соединений. При их
использовании белье можно стирать даже без предварительного замачивания. Кроме
того, полифосфаты усиливают действие поверхностно-активных веществ.
Адсорбируясь на волокнах, молекулы полифосфатов отталкивают частицы грязи с
поверхности ткани и вследствие электростатического отталкивания способствуют их
распределению в моющем растворе. Однако они имеют и существенный недостаток –
загрязняют окружающую среду. Продукты гидролиза полифосфатов накапливаются в
сточных водах, а поскольку фосфор - необходимый компонент питания растений, то
создается нежелательная концентрация этих питательных веществ.
Обычные моющие средства эмульгируют только жиры, а,
следовательно, и присутствующие на них частицы грязи. Другие загрязнения, такие
как белковые вещества остатков пищи и крови, при этом не удаляются. Более того,
в горячей воде они вообще не растворяются. Для устранения подобных загрязнений
разработаны биологически активные моющие средства. Эти препараты содержат
ферменты, растворяющие белки, - так называемые протеазы. Но, к сожалению,
большинство известных протеаз разлагаются в щелочной среде моющего раствора и
не выдерживают высокой температуры при стирке.
Чтобы у стираного белья был приятных запах, во все моющие
средства вводят парфюмерные отдушки.
Из-за незнания действия моющего средства и правильной
технологии стирки потреблялось в среднем на 10-15% больше моющего средства, чем
нужно. Да и как разодраться в обилии грубых, быстродействующих, универсальных,
легких и тонких стиральных порошков и паст?
Итак, стирка – физико-химический процесс, факторами для
которого являются химия (в форме моющих средств), механика (стиральные машины),
температура и время. Целью научных исследований и разработок служит увеличение
в этом процессе доли химии и уменьшение других, более трудоемких факторов –
температуры и времени.
Стирка и химическая чистка изделий из тканей являются
химическими процессами. Химик должен знать их условные обозначения, а также
допустимые температуры глажки и условия сушки. (Приложение №3)
Универсальными моющими средствами можно стирать изделия из
тканей всех видов, но изделия из синтетических, шелковых и шерстяных тканей
все-таки лучше стирать жидкими моющими средствами.
В продаже имеются следующие универсальные моющие средства:
порошки «Лотос», «Лотос-А», «Лотос-автомат», «Биолан», «Лоск», «Тайд»,
«Ариэль», «ОМО», «Миф», «Пемос», «Апрель», «Аист», «Мix», «Дося», и др.; пасты «Аэлита», «Ландыш», «Сюрприз»,
«Эридан», «Фея»,; жидкости «Аста», «Сепераль», «Экс».
Среди СМС универсального действия имеют порошки, содержащие
энзимы (ферменты) – «Биолан», «Био-эст», «Биомакс». Ими нельзя стирать изделия
из натурального шелка и шерсти.
Разработана технология получения нового синтетического
кускового моющего средства (СКМС). Она состоит в основном из синтетических
моющих средств, но с обязательной добавкой обычного мыла. Новое СКМС обладает
высокой эффективностью при удалении загрязнения, не вызывает раздражения кожи,
что предупреждает возникновение различных кожных заболеваний. Организация
производства СКМС расширит ассортимент СМС. Это позволит создать препараты для
стирки различных видов ткани, для личной гигиены, для мытья рук, для мытья
посуды, полов, ванн, кафельных стен, санузлов и др
Вспомогательные средства для стирки
4.1.1. Оптические отбеливатели
После нескольких стирок изделия из белых тканей желтеют или
сереют. Для устранения появляющихся оттенков и вводят в синтетические моющие
средства оптические отбеливатели. Их действие заключается в том, что они
поглощают ультрафиолетовый свет (с длиной волны ~360 нм) и вновь испускают
поглощенную энергию путем флуоресценции в синей области видимого спектра (при
430…440 нм). Возникающее при этом «посинение» изделия компенсирует
пожелтение и делает изделие визуально более белым. Действие оптических
отбеливателей напоминает действие синьки, с давних пор использовавшейся при
полоскании белья после стирки. Бытовая синька или ультрамарин – природный
минерал лазурит, называемый также ляпис-лазурью. В монолитном виде он
используется как поделочный камень, а его очень тонкий порошок в далеком
прошлом применялся в качестве синьки. В 1828 г. ультрамарин был получен
искусственно в лабораторных условиях. Для этого смесь каолина, соды и серы
прокаливалась в сильной струе воздуха. Состав ультрамарина выражают формулой Na6Al4Si6S4O24,
однако его строение до сих пор не выяснено. Заменителем ультрамарина в быту
является порошок белой глины (каолина) или мела с предварительно нанесенным на
их поверхность органическими красителями синего цвета (органические синьки).
4.1.2. Химические отбеливатели
При стирке тканей необходимо не только удалить загрязнения,
но и разрушить окрашенные соединения. Часто ими являются природные красители от
ягод или вин. Эту функцию выполняют химические отбеливатели. Наиболее
распространенным отбеливателем является перборат натрия. Его химическую формулу
условно записывают в виде NaBO2·H2O2·3H2О.
Из формулы видно, что отбеливающим началом служит пероксид водорода, который
образуется в результате гидролиза пербората. Этот химический отбеливатель
эффективно действует при 70°C и выше.
4.1.3. Отбеливающие ферменты
Пятна белковых веществ и крови трудно отстирываются и плохо
обесцвечиваются химическими отбеливателями. Для их устранения применяют
специальные ферменты, которые вводят в качестве добавки к моющим системам.
Ферменты действуют при замачивании изделий в холодной воде перед стиркой
горячей водой. Однако они могут быть эффективны и непосредственно в процессе
стирки.
·
4.1.4. Смягчители.
При стирке синтетическими моющими средствами и последующей
сушке изделия из тканей (полотенца, пеленки и др.) могут стать жесткими на
ощупь. Для ее устранения применяют смягчители. Это достигается полосканием в
воде с добавкой специальных составов. Наиболее известными смягчителями являются
соединения четвертичных аммониевых оснований.
Formula p.101
В состав смягчителей, которые выпускаются в виде раствора или
пасты, входят также оптические отбеливатели и отдушка. Кроме того, средства,
предназначенные для смягчения, обладают также антистатическим действием. Отечественные
средства «Полиэн», «Утюжок», «Маг», и «Амелия», а к импортным средствам
относятся «Ваниш», «Ленор».
4.1.5. Пенообразователи.
Среди домохозяек бытует устаревшее мнение, что для успешного
отстирывания тканей необходима обильная пена. Однако это представление
справедливо лишь для порошков на основе мыла. В случае синтетических моющих
средств прямой связи между отстирывающей и пенообразующей способностью нет.
Существуют составы, которые обладают хорошими отстирывающими свойствами, но
пены почти не дают. При использовании стиральных машин обильная пена иногда и
нежелательна. Поэтому существуют пенообразователи на любой вкус. К усилителям
пенообразования относят аминоспирт C11H23CONHCH2CH2OH
и оксид амина
Formula p.101
4.1.6. Подкрахмаливающие и
аппретирующие средства.
Кроме известного и широко применяемого крахмала, для
подкрахмаливания постельного белья и других изделий в быту активно используются
современные препараты на основе крахмала и поливинилацетатной эмульсии. Цель
подкрахмаливания заключается в придании тканям большей жесткости, несминаемости,
грязе- и водоотталкивающих свойств; то есть подкрахмаливание можно назвать
одним из компонентов аппретирования – окончательной отделки тканей. В процессе
аппретирования ткань обрабатывают соответствующим препаратом и дают возможность
образоваться на ее поверхности довольно твердой пленке.
К препаратам на основе крахмала относятся «Нежный» (порошок)
и «Паланга» (таблетки). В торговую сеть поступают препараты – «Альба»,
«Амелия», «Апперт», «Белая эмульсия» и др. Аэрозольные препараты на основе
поливинилацетатной эмульсии с добавкой карбомола «Элегант», «Элегант с
отбеливанием», «Кросс», «Вельте», «Бланка-эффект», «Дана» применяются для
придания тканям несминаемости.
4.1.7. Антистатики
Вспомним недалекое прошлое. Мы восторгались одеждой из
капрона. Потом стали замечать, что в ней не особенно уютно, появляются какие-то
покалывания, иногда становится душно. Ткань прилипает к телу, выступающие
волокна скатываются, изделие теряет форму, к нему притягивается пыль. Иногда
наблюдается треск и искрение. По способности электризоваться синтетические
волокна модно расположить следующим образом: из волокон, накапливающих «+»
заряд – капрон, нейлон, шерсть, шелк. Среди волокон, способных накапливать «-«
заряд – нитрон, лавсан и ацетатные волокна.
Способность электризоваться может быть снижена или вовсе
устранена, если повысить влажность волокна. Некоторые синтетические материалы
плохо удерживают влагу, поэтому изделия из таких волокон надо подвергнуть специальной
обработке препаратами, образующими на их поверхности тончайшую пленку. Такая
пленка удерживает влагу и вместе с поглощенной ею водой снижает электрическое
сопротивление тканей, в результате чего электризация уменьшается или исчезает
вовсе.
Химики создали препараты – антистатики (химические вещества),
вводимые в синтетические ткани для предотвращения аккумулирования ими зарядов
статического электричества.
Эффективными антистатиками являются «Анэль» (жидкость), пасты
«Антистатик», аэрозоли «Лана», «Полилана»,
Глава 5. Химические средства гигиены и косметики.
Слово гигиена происходит от греч. Гигиенос, что означает
целебный, приносящий здоровье, а косметика – от греч., означающее искусство
украшать. В настоящее время термин «косметика» употребляют прежде всего в связи
с уходом за кожей лица и тела. Гигиена – это раздел профилактической медицины,
изучающей влияние внешней среды на здоровье человека.
К важнейшим гигиеническим средствам следует, прежде всего,
отнести мыла и моющие средства. О них была речь ранее. Конечно, охватить все
химические средства гигиены и косметики невозможно. Поэтому здесь внимание
будет обращено лишь на некоторые.
5.1. Средства
ухода за зубами
Зуб состоит из трех частей: коронки (часть, выступающая над
десной), корня (часть, погруженная в альвеолу челюсти) и шейки – место перехода
коронки в корень. Коронка покрыта эмалью, а под ней находится дентин. Корень
покрыт слоем ткани, называемой цементом. Эмаль, дентин и цемент – это твердые
ткани. Внутри зуба имеется полость, которая содержит пульпу, состоящую из
рыхлой соединительной ткани, в которой проходят нервы и сосуды, питающие ткани
зуба. (Приложение №1)
Зубы подвержены ряду заболеваний и одним из наиболее
распространенных является кариес. К сожалению, никому не удается избежать этого
заболевания, но ограничить его распространение на многие зубы можно, принимая
профилактические меры. Сущность кариеса состоит в том, что под влиянием
микроорганизмов и вырабатываемых ими кислот происходит разрушение тканей зуба.
Самой прочной тканью является эмаль. Ее состав близок к минералу
гидроксидапатиту Ca5OH(PO4)3. При разрушении
эмали микроорганизмы попадают в дентин, а затем в пульпу и вызывают ее
воспаление (пульпит). (Приложение №1)
Закреплению микроорганизмов на эмали способствует зубной
камень – твердые пористые отложения на зубах. Микроорганизмы поселяются в порах
этого камня. Первая стадия образования зубного камня связана с отложением на
зубах мягкого налета из остатков пищи, отживших клеток, слизи. На второй стадии
происходит минерализация мягкого налета, т.е. его пропитывание минеральными
компонентами слюны. Слюна содержит ионы Ca2+ и HPO24–.
Они препятствуют растворению эмали зуба, но, откладываясь в мягком налете в
виде малорастворимой соли, приводят к его минерализации.
Слюна здорового человека имеет нейтральную реакцию (рН
7,0...7,5). В результате расщепления бактериями (Streptococcys mytanis) остатков пищи, содержащей углеводы (в частности,
сахар), образуются органические кислоты – в основном молочная. Эти кислоты
снижают рН до 4,5...5,0. В данных условиях разрушение эмали ускоряется, что и
приводит к весьма неприятным результатам. Давно замечено, что любители сладкого
часто не могут похвастаться хорошим состоянием зубов.
Таким образом, одним из путей профилактики кариеса является
очистка зубов, и полоскание ротовой полости после приема пищи. Это приводит к
предотвращению образования мягкого налета и зубного камня.
Трудно сказать, когда люди начали чистить зубы, но имеются
сведения, что одним из древнейших препаратов для чистки зубов была табачная
зола. Еще сравнительно недавно для чистки зубов широко применяли зубные
порошки. Они состоят из абразивного материала: чаще всего это мел CaCO3,
реже CaHPO4, а иногда их смеси. Эти абразивы получают химическим
осаждением, например, в соответствии с уравнением
Ca(NO3)2 + Na2CO3 = CaCO3↓ + 2NaNO3
Природный мел использовать нельзя, так как в нем содержатся
твердые частицы от панцирей морских организмов, которые обладают высокой
прочностью и могут привести к сильному истиранию и повреждению эмали зуба. К
абразивным материалам добавляют MgO, полученный прокаливанием MgCO3.
Оксид магния придает порошкам легкость и рыхлость. В некоторые сорта порошков
вводят пероксид магния MgO2, который обладает отбеливающими
свойствами. В небольших количествах в порошки включают поверхностно-активные
вещества, например лаурилсульфат натрия C12H25OSO3Na,
а также отдушки – чаще всего ментол или экстракт мяты. В настоящее время
сокращено производство зубных порошков, поскольку они стали менее популярными,
чем пасты.
Важнейшим средством ухода за зубами являются зубные пасты.
Они имеют меньшую истирающую способность по сравнению с порошками, более удобны
в применении и характеризуются более высокой эффективностью.
Зубные пасты – это многокомпонентные составы. Они подразделяются
на гигиенические и лечебно-профилактические. Первые оказывают только очищающее
и освежающее действие, а вторые, кроме того, служат для профилактики
заболеваний и способствуют лечению зубов и полости рта.
Основные компоненты зубной пасты следующие: абразивные,
связующие, загустители, пенообразующие. Абразивные вещества обеспечивают
механическую очистку зуба от налетов и его полировку. В качестве абразивов чаще
всего применяют химически осажденный мел CaCO3. Установлено, что
компоненты зубной пасты способны влиять на минеральную составляющую зуба и, в
частности, на эмаль. Поэтому в качестве абразивов стали применять фосфаты
кальция: CaHPO4, Ca3(PO4)2, Ca2P2O7,
а также малорастворимый полимерный мета-фосфат натрия (NaPO3)x.
Кроме того, в качестве абразивов в различных сортах паст применяют оксид и
гидроксид алюминия, диоксид кремния, силикат циркония, а также некоторые
органические полимерные вещества, например метилметакрилат натрия. На практике
часто используют не одно абразивное вещество, а их смесь. Для превращения смеси
абразивных порошков в стойкую пасту применяют желатинирующие компоненты. Их
часто получают в промышленном масштабе из растений; например, из морских
водорослей извлекают природные полисахариды: натриевые соли альгиновых кислот и
каррагинаты. Для этой цели реже применяют растительные камеди – трагакант и
пектины. Из синтетических веществ широкое применение нашли производные
клетчатки (хлопковой и древесной) – натрийкарбоксиметилцеллюлоза,
оксиэтилированные этиловый и метиловый эфиры целлюлозы или просто этиловый и
метиловый эфиры целлюлозы. Для получения пластичной, тиксотропной массы, легко
выдавливающейся из тюбика, применяют полиатомные спирты: глицерин, сорбит,
полиэтиленгликоль. Они способствуют сохранению в пасте влаги при хранении,
повышают температуру замерзания и улучшают вкусовые свойства пасты.
Растительные экстракты и камеди чувствительны к действию микробов. Поэтому для
устранения их разрушительного действия в состав паст вводят антисептические
вещества: формальдегид, хлорированные фенолы и алкильные эфиры оксибензойных
кислот.
В качестве пенообразующих веществ в зубных пастах в прошлом
использовали мыла. Однако их низкая пенообразующая способность в жесткой воде и
неприятный мыльный привкус снижали качество паст. Вместо мыла стали
использовать ализариновое масло (сульфированное касторовое масло)
Formula p.105
Оно не связывается в малорастворимое вещество ионами кальция
и магния и обладает смачивающими и бактерицидными свойствами. Кроме него в
качестве пенообразователей используют натрийлаурилсульфат C12H25OSO3Na
и натрийлаурилсаркозинат
Formula p.101
Считают, что последний обладает антикариесным действием. Уже
в концентрации 0,3% он подавляет действие бактерий, образующих в полости рта
молочную кислоту, которая разрушает эмаль зуба. Действие лаурилсаркозината
сохраняется в полости рта после чистки зубов в течение примерно 12 ч.
Хорошими пенообразующими, очищающими и смачивающими свойствами обладает
натриевая соль таурида жирной кислоты RCONHCH2SO3Na.
Борьбу с кариесом при помощи лечебно-профилактических зубных
паст ведут по двум направлениям:
1) укрепление минеральной ткани зуба;
2) предупреждение образования зубного налета.
Первое достигается введением в пасты соединений фтора:
монофторфосфата натрия, формулу которого условно можно записать в виде двойной
соли NaF·NaPO3, а также фторида натрия NaF и фторида олова (II)
SnF2.
Существуют две точки зрения на влияние фторидных ионов на
укрепление эмали зуба:
1. Ионы F– переводят гидроксидапатит эмали
CaOH(PO4)3 в менее растворимый в кислотах фторапатит Ca5F(PO4)3.
2. В результате обменной реакции в пасте образуется CaF2,
который адсорбируется на гидроксидапатите и предохраняет его от воздействия
кислот. Известно также, что фторидные соединения способствуют подавлению жизнедеятельности
бактерий, вызывающих образование в полости рта органических кислот.
В настоящее время в антикариесных пастах стали широко
использовать ферменты, а иногда в них вводят антибиотики.
В зубные пасты обязательно вводят отдушки и вкусовые
компоненты. Наиболее распространены отдушки мятного и коричного характера.
Мятная отдушка обеспечивается применением ментола, мятных масел – перечной или
кудрявой мяты, а также различных модификаторов. В отдушках применяют
метилсалицилат, гвоздичное масло, эвкалиптол, коричный альдегид. В качестве
подслащивающего компонента чаще всего используют сахарин и некоторые его
производные. За рубежом для этой цели рекомендуют сахарат натрия и дульцин
вместе с небольшим количеством хлорида натрия или лимонной кислоты. Недавно
стали применять натриевую соль цикламеновой кислоты, которая по вкусу
напоминает сахар.
Некоторые зарубежные фирмы приступили к производству
безабразивных гелеобразных прозрачных зубных паст. В них используют гели SiO2,
а также сополимеры акриловой кислоты и аллилового спирта. Эти пасты обладают
высокой пенообразующей способностью, имеют приятный вкус и красивый внешний
вид. Они легко окрашиваются в различные яркие цвета – красный, синий, зеленый,
желтый. Однако их очищающая способность намного ниже, чем паст с использованием
абразивов.
Хотя зубные протезы, естественно, не подвергаются кариесу и
другим заболеваниям, но от них может зависеть состояние микрофлоры полости рта.
Имеет существенное значение и их внешний вид. Поэтому зубные протезы требуют
периодической чистки от остатков пищи, пятен и образующегося зубного камня. Для
этой цели протезы погружают на ночь или на более короткий срок в растворы
кислот: соляной, сульфаминовой или лимонной, а также в растворы, содержащие
активный хлор, – гипохлориты или активный кислород – перборат натрия.
5.2. Косметические
средства
В мире считается, что среди наиболее прибыльных отраслей
промышленности на одном из первых мест стоит косметическая. Наблюдения
показывают, что если нужно, то женщины могут отказать себе во многом, только не
в том, что сделает их хотя бы чуточку красивее.
Искусство косметики уходит в далекое прошлое. Так, при
раскопках найдены египетские мумии, ногти которых раскрашены. В усыпальницах
египетских пирамид обнаружены натуральные краски и косметические инструменты,
различные плитки для приготовления смеси красок и румян, сосуды для хранения
мазей и масел. Найден письменный документ – папирус Эберса, в котором изложены
косметические правила и рецепты. Его написание относят к пятому тысячелетию до новой
эры.
Письменные источники далекого прошлого и наблюдения
современных путешественников свидетельствуют о том, что на ранней стадии
развития к раскрашиванию тела красками были неравнодушны и мужчины. Как атавизм
этого можно рассматривать склонность некоторых мужчин к накожной татуировке. По
мере развития культуры мужчины теряют этот интерес. Стремление женщин к
подкрашиванию кожи (особенно лица) наоборот усиливается. Судя по всему, для
женщин нет простой связи между культурой и количеством используемой косметики.
Связь скорее можно уловить между количеством косметики и прирожденным вкусом.
Древние рукописи свидетельствуют, что уже тысячи лет назад
женщины Востока подкрашивали веки в голубой цвет тончайшей пыльцой из толченой
бирюзы. Бирюза – это природный минерал, имеющий состав СuАl6(PO4)4(OH)8·4H2О.
С незапамятных времен для подкрашивания бровей использовался
мягкий природный минерал – сурьмяный блеск Sb2S3. В
русском языке было выражение «сурьмить брови». Сурьмяный блеск поставлялся в
различные страны арабами, которые называли его стиби. От этого названия и пошло
латинское стибиум, означавшее в древности не химический элемент, а его сульфид
Sb2S3. Природный сурьмяный блеск имеет цвет от серого до
черного с синей или радужной побежалостью.
Достоверно известно, что в России косметические краски
применялись в конце XVI и особенно широко в XVII в. историк
П.М. Лукьянов в одной из своих книг цитирует саксонского путешественника
Олеария, который посетил Россию в первой половине XVII в. и позднее описал
свои впечатления: «Женщины в России среднего роста, вообще стройны, нежны лицом
и сложением, но в городах все румянятся и так грубо и заметно, что, глядя на них,
подумаешь, будто кто вымазал их рукою полною муки и потом кисточкой намазывал
им на щеки красной краской. Брови и ресницы они также подкрашивали черной, а
иногда и коричневой краской»{5}. Впечатления того же времени другого
путешественника по России голландца Стрюйса на этот счет записаны следующими
словами: «Хотя женщины обыкновенно белы, и кожа на лице их очень гладкая,
все-таки они почти все румянятся или вернее натираются ляповато белилами и
приглашают для этого белильшиц»{5}. Румянами в то время красили не только щеки,
но и губы.
Естественно, что в далеком прошлом в качестве косметических
препаратов использовались лишь природные минеральные и органические вещества. С
развитием химии для этой цели все чаще стали применять синтетические продукты.
Так, например, в качестве пигмента для губных помад применяют малиново-красный
бис-ди-метилглиоксимат никеля. Органический реагент ди-метилглиоксим
химики-аналитики используют для качественного обнаружения и количественного
определения ионов никеля (II), а реакция образования этого соединения
носит имя нашего соотечественника Л.А. Чугаева.
Промышленность выпускает перламутровые губные помады и кремы,
а также шампуни с перламутровыми блесками. Перламутровый эффект в косметических
средствах создается солями висмутила BiOCl и ВiO(NO3) или
титанированной слюдой – перламутровым порошком, содержащим около 40% TiO2.
Давно известны жемчужные или испанские белила. Их основным компонентом является
ВiO(NO3)2, образующийся при растворении нитрата висмута
Вi(NO3)3 в воде. В косметике эти белила используют для
приготовления белого грима.
Для создания специальных косметических средств (гримов)
применяют оксид цинка ZnO, получаемый прокаливанием основного карбоната (ZnOH)2CO3.
В медицине его используют в присыпках (в качестве вяжущего, подсушивающего,
дезинфицирующего средства) и для изготовления мазей.
Косметические декоративные пудры – многокомпонентные смеси. В
них входят: тальк, каолин, ZnO, TiO2, MgCO3, крахмал,
цинковые и магниевые соли стеариновой кислоты, а также органические и
неорганические пигменты, в частности Fe2O3. Тальк придает
пудре сыпучесть и скользящий эффект. Его недостатком является способность
впитываться в кожу и придавать жирный блеск. Тем не менее, в состав пудр он
входит в количестве до 50...80%. Каолин обладает высокой укрывистостью и
способностью впитывать избыток жировых выделений кожи. Его повышенная гигроскопичность
способствует слеживаемости и неравномерному распределению пудры на коже,
поэтому каолин вводят не более 25%. Оксиды цинка и титана обладают хорошей
укрывистостью. Кроме того, оксид цинка обладает антисептическими свойствами и
потому одновременно выполняет роль дезинфицирующей добавки. Эти оксиды вводят в
пудры до 15%. В больших количествах они приводят к сухости кожи. Крахмал
придает коже бархатистость, а благодаря стеаратам цинка и магния пудра хорошо
удерживается на коже и делает ее гладкой.
Компактная пудра в отличие от рассыпной содержит связующие
добавки: натрийкарбоксиметилцеллюлозу, высшие жирные кислоты, воски,
многоатомные спирты и их эфиры, минеральные и растительные масла. Они позволяют
получать при прессовании брикеты определенной формы, которые сохраняют
прочность при длительном употреблении.
2H2O2 = 2H2О + O2
В момент образования кислород находится в атомарном состоянии
и лишь, затем переходит в молекулярный:
2О = O2
Атомарный кислород обладает особенно сильным окислительным
свойством. Благодаря ему, растворы пероксида водорода разрушают красящие
вещества и отбеливают ткани из хлопчатобумажных и шерстяных тканей, шелк,
перья, волосы. Способность пероксида водорода обесцвечивать волосы используют в
косметике. Она основана на взаимодействии атомарного кислорода с красящим
веществом волос меланином – смесью сложных органических веществ. При окислении
меланин переходит в бесцветное соединение. Следует помнить, что пергидроль вызывает
ожоги кожи и слизистых оболочек.
В настоящее время для окраски волос имеется большой
ассортимент различных органических красителей.
Иногда же для этой цели применяют соли серебра, меди, никеля,
кобальта, железа. В таком случае крашение волос осуществляют при помощи двух
растворов. Один из них содержит соли данных металлов: нитраты, цитраты,
сульфаты или хлориды, а второй – восстановители: пирогаллол, танин и др. При
смешении этих растворов ионы металлов восстанавливаются до атомов, которые и
осаждаются на поверхности волос.
Наиболее распространенный лак для ногтей представляет раствор
нитроцеллюлозы в органических растворителях. Нитроцеллюлозу получают
нитрованием целлюлозы (хлопковой или древесной) смесью азотной и серной кислот.
Она является сложным эфиром азотной кислоты и характеризуется общей формулой
[C6H7O2(OH)3–x(ONO2)x]n.
В качестве растворителей используют амиловый эфир уксусной
кислоты, ацетон, различные спирты, этиловый эфир, а также их смеси. В лак
добавляют пластификаторы – касторовое масло или другие экстракты, которые
препятствуют обезжириванию ногтей и предотвращают их ломкость.
Следует отметить, что косметика тесно соприкасается с
гигиеной, так как имеется много косметических средств (лосьоны, кремы, шампуни
и др.), которые выполняют и гигиеническую функцию.
5.3. Дезодоранты и озоновый «щит»
планеты
Каждый знает, что дезодоранты – это средства, устраняющие
неприятный запах пота. На чем основано их действие? Пот выделяется особыми
железами, расположенными в коже на глубине 1...3 мм. (Приложение №2) У
здоровых людей на 98...99% он состоит из воды. С потом из организма выводятся
продукты метаболизма: мочевина, мочевая кислота, аммиак, некоторые
аминокислоты, жирные кислоты, холестерин, в следовых количествах белки,
стероидные гормоны и др. Из минеральных компонентов в состав пота входят ионы
натрия, кальция, магния, меди, марганца, железа, а также хлоридные и иодидные
анионы. Неприятный запах пота связан с бактериальным расщеплением его
составляющих или с окислением их кислородом воздуха. Дезодоранты (косметические
средства от пота) бывают двух типов.
1.
Тормозят
разложение выводимых с потом продуктов метаболизма путем инактивации
микроорганизмов или предотвращением окисления продуктов потовыделения.
2.
Действие второй
группы дезодорантов основано на частичном подавлении процессов потовыделения.
Такие средства называют антиперспиранами. Этими свойствами
обладают соли алюминия, цинка, циркония, свинца, хрома, железа, висмута, а
также формальдегид, таннины, этиловый спирт. На практике из солей в качестве
антиперспирантов чаще всего используют соединения алюминия. Перечисленные
вещества взаимодействуют с компонентами пота, образуя нерастворимые соединения,
которые закрывают каналы потовых желез и тем самым уменьшают потовыделение. В
оба типа дезодорантов вводят отдушки.
Чем же создается давление в аэрозольных баллонах? Это не
праздный вопрос, так как с ним, можно сказать, связана судьба человечества.
Рабочее давление в баллонах создается парами сжиженного газа, либо за счет
сжатого газа, например, N2, CO2 или N2O. До
сих пор баллоны со сжатыми газами применялись редко, поскольку их рабочее
давление падает по мере расходования содержимого баллона, т.е. по мере
увеличения объема парового пространства. Давление над сжиженным газом
постоянно, так как оно поддерживается испарением жидкости и заполнением
увеличивающегося пространства. В качестве веществ, создающих давление в
аэрозольных баллонах, оказались удобными фторхлоруглероды. 
Так, при 21°C давление паров над жидким CF2Cl2
составляет 5 атм, а над смесью (50%:50%) CF2Cl2 и CF2Cl2
2,5 атм. Эти вещества, кроме того, обладают важным свойством – малой
химической активностью по отношению ко многим веществам. Легкокипящие и
химически инертные вещества, используемые для создания повышенного давления в
аэрозольных баллонах, называют пропеллентами. Таким образом, в аэрозольных
баллонах в жидком веществе (основе), ради которого и создается устройство,
содержится жидкий пропеллент. Довольно часто растворы аэрозольного баллона
(одеколоны, кремы для бритья и др.) содержат воду. Пропелленты CF2Cl2
и CFCl3 со временем частично гидролизуются (взаимодействуют с водой)
и поэтому нежелательны. В таких случаях в качестве пропеллента используют CF2Cl – CF2Cl
(1,2-дихлортетрафторэтан). В настоящее время принято международное соглашение
по сокращению производства аэрозольных баллонов, содержащих в качестве
пропеллентов фторхлоруглероды, поскольку установлено, что они плохо влияют на
озоновый слой Земли.
 В атмосфере на определенной высоте от Земли имеется
повышенная концентрация озона. Он получается в результате фотодиссоциации
молекулярного кислорода и взаимодействия атомарного кислорода
В атмосфере на определенной высоте от Земли имеется
повышенная концентрация озона. Он получается в результате фотодиссоциации
молекулярного кислорода и взаимодействия атомарного кислорода
O2 ← [hν (свет)] → 2O
с молекулярным в соответствии с уравнением
O + O2 ↔ O3*
Образующиеся молекулы озона содержат избыточную энергию, т.е.
они возбуждены. Если не отвести от молекулы озона эту избыточную энергию, то
она долго не просуществует, а распадется на исходные атомарный и молекулярный
кислород. Чтобы молекула озона стала стабильной, она должна отдать избыток
энергии какой-то другой молекуле, например молекуле азота:
O3* + N2 → O3 + N2*
Концентрация озона в атмосфере зависит от двух причин:
1. Для диссоциации молекул O2 на атомы нужно
интенсивное коротковолновое солнечное излучение, которое поглощается по мере
приближения к Земле. Следовательно, диссоциация O2 на атомы
преимущественно протекает в верхних слоях.
2. Для стабилизации образующихся молекул озона необходимо
столкновение с другими частицами, т.е. разрежение воздуха не должно быть
слишком большим, а, следовательно, высота должна быть также не очень большая. В
результате этих двух факторов, действующих в противоположных направлениях, озон
накапливается в определенных слоях атмосферы. Опыт показывает, что наибольшая
его концентрация наблюдается на высоте около 50 км. Этот слой атмосферы и
называют озоновым «щитом» планеты. Он играет чрезвычайно важную роль в
сохранении жизни на Земле. Оказалось, что молекулы озона, как никакие другие,
находящиеся в атмосфере, сильно поглощают фотоны с длиной волны от 200 до
310 нм, т.е. ультрафиолетовое излучение Солнца. Известно, что растения и
животные гибнут при интенсивном облучении этим светом. Таким образом, можно
сказать, что от концентрации озона зависит судьба нашей планеты.
Концентрация озона в атмосфере зависит от содержания оксидов
азота и фторхлорметанов. Оксиды азота постоянно присутствуют в низких
концентрациях в результате фотохимического взаимодействия азота и кислорода.
Оксид азота (II) разрушает озон, а оксид азота (IV) связывает
атомарный кислород в соответствии с уравнениями
Formula p.109
Таким образом, оксиды азота играют роль катализаторов в
разложении озона.
За 4,6 млрд лет существования нашей планеты установилось
равновесие, и жизнь на Земле возникла и развилась при определенном равновесном
составе атмосферы. Однако интенсивное развитие сверхзвуковой авиации начинает
оказывать влияние на создавшееся в атмосфере равновесие. Поскольку
сверхзвуковые самолеты предназначены для полетов в стратосфере, верхний предел
которой подходит к «озоновому» слою, то появляется опасность влияния
сверхзвуковой техники на этот слой. При сгорании топлива в двигателях самолетов
в довольно больших количествах образуются оксиды азота.
Другим источником опасности озоновому слою являются
фторхлорметаны (главным образом CF2Cl2 и CFCl3).
Эти вещества широко используют в баллонах в аэрозольной упаковке, а также в
качестве хладоагентов в промышленных и бытовых холодильниках. Фторхлорметаны –
чрезвычайно инертные химические вещества. В атмосфере они разрушаются лишь в
верхних слоях под действием ультрафиолетового излучения в диапазоне длин волн
190...225 нм. Одним из продуктов разложения фторхлорметанов является
атомарный хлор:
CCl4–xFx – [hν
(свет)] → CCl3–xFx + Cl
Скорость разрушения фторхлорметанов максимальна на высоте
около 30 км, т.е. в слое, примыкающем к озоновому. Атомарный хлор так же,
как и оксиды азота, способен катализировать разложение озона в соответствии с
уравнениями
Formula p.110
Научная общественность высказывает озабоченность разрушением
озонового слоя Земли и требует сокращения использования фторхлорметанов в
качестве распылителей аэрозолей.
Ожоги солнечным светом вызываются ультрафиолетовыми лучами в
области длин волн 280...315 нм (эритемная область). Ультрафиолетовые лучи
с длинами волн 315...400 нм способствуют образованию на коже человека
пигмента меланина, который служит защитой от эритермы (от ожога). В некоторых
странах налажен выпуск фотозащитных кремов, которые поглощают или отражают
солнечные лучи эритемной области, но пропускают лучи, стимулирующие появление
на коже загара. В качестве примеров фотозащитных соединений можно указать на
этиловый эфир циннамилиденуксусной кислоты (I) и
2-фенилбен-зоксазол (II):
Formula p.110
Заключение
Химия – это наука, важная часть естествознания. Строго
говоря, наука не может окружать человека. Его могут окружать результаты
практического приложения науки. Это уточнение весьма существенное. В настоящее
время часто можно слышать слова: «химия испортила природу», «химия загрязнила
водоем и сделала его непригодным для использования» и т.д. На самом же деле
наука химия здесь вовсе непричем. Люди, используя результаты науки, плохо
оформили их в технологический процесс, безответственно отнеслись к требованиям
правил безопасности и к экологически допустимым нормам промышленных сбросов,
неумело и не в меру использовали удобрения на сельскохозяйственных угодьях и
средства защиты растений от сорняков и вредителей растений. Любая наука,
особенно естествознание, не может быть хорошей или плохой. Наука – накопление и
систематизация знаний. Другое дело, как и в каких целях используются эти
знания. Однако это уже зависит от культуры, квалификации, моральной
ответственности и нравственности людей, не добывающих, а использующих знания.
Без продуктов химической промышленности современному человеку
не обойтись, так же как нельзя обойтись без электричества. Такая же ситуация и
с продуктами химической промышленности. Нужно протестовать не против некоторых
химических производств, а против их низкой культуры.
Культура человека – сложное и разноплановое понятие, при
котором возникают такие категории, как умение человека вести себя в обществе,
правильно владеть родным языком, следить за опрятностью своей одежды и внешним
видом и т.д. Однако мы часто говорим и слышим о культуре строительства,
культуре производства, культуре ведения сельского хозяйства и т.д.
Действительно, когда речь заходит о культуре Древней Греции или еще более
ранних цивилизациях, то, прежде всего вспоминают о ремеслах, которыми владели
люди той эпохи, какие орудия труда они использовали, что умели строить, как
умели украшать строения и отдельные предметы.
Многие важные для человека химические процессы были открыты
задолго до того, как химия оформилась в науку. Значительное количество
химических открытий было сделано наблюдательными и любознательными ремесленниками.
Эти открытия переходили в семейные или клановые секреты и далеко не все дошли
до нас. Часть из них была утеряна для человечества. Приходилось и приходится
затрачивать огромный труд, создавать лаборатории, а иногда и институты для
раскрытия секретов древних мастеров и их научного толкования.
Многие не знают, как устроен телевизор, но успешно пользуются
им. Однако знание устройства телевизора никогда и никому не помешает в
правильной его эксплуатации. Так и с химией. Понимание сущности химических процессов,
с которыми мы встречаемся в повседневной жизни, может принести человеку только
пользу.
В жизни приходится выполнять много функций, не связанных с
основной специальностью: строить дом, обрабатывать садовый участок, окрашивать
ткань и выводить с нее пятна и т.д. Как уже было сказано, культура – понятие
многоплановое, но любая ее составляющая основана на знаниях, на
информированности, на грамотности.
Список литературы
1.
Краткая
химическая энциклопедия. – М.: Советская энциклопедия, 1961...1967. Т. I...V.
2.
Советский
энциклопедический словарь. – М.: Сов. энциклопедия, 1983.
3.
Войцеховская А.Л.,
Вольфензон И.И. Косметика сегодня. – М.: Химия, 1988.
4.
Кукушкин Ю.Н.
Соединения высшего порядка. – Л.: Химия, 1991.
5.
Кукушкин Ю.Н.Химия
вокруг нас. – Л.: Химия, 1993.
6.
Лепешков И.Н.,
Розен Б.Я. Минеральные дары моря. – М.: Наука, 1972.
7.
Лукьянов П.М.
Краткая история химической промышленности СССР. – М.: Изд-во АН СССР, 1959.
8.
Теддер Дж.,
Нехватал А., Джубб А. Промышленная органическая химия. – М.: Мир,
1977.
9.
Чалмерс Л.
Химические средства в быту и промышленности. – Л.: Химия, 1969.
10.
Рудзитис Г.Е., Фельдман Ф.Г. Химия-10. М.: Просвещение, 1991
11.
Перельман Я.И. Знаете ли вы
физику? М.: Просвещение, 1971;
Грин Н., Стаут У., Тейлор Д. Биология.
М.: Мир, 1993.
12.
Химия в быту. –
Смоленск: «Русич», 1996, 56 стр. (Азбука быта).
13.
Юдин А.М., Сучков
В.Н., Коробелин Ю.А. «Химия для Вас» - 3 изд., стереотипн. – М.: Химия, 1986г.
– 192 с. С ил.
14.
Коноплева Н.П.
Домашнее хозяйство 1000 полезных советов – М.: Изд-во Эксмо-Пресс, 2001 г. -352
с.
15.
Поллер .З.К.
Химия на пути в 3-е тысячелетие: Пер. с немецкого (перевод и предисловие
Васиной Н.А. – М.: Мир, 1982 г. 401 с.
16.
Справочник
зубного врача /Под ред. А.И.Воробьева – М.: Медицина, 1981, 656 с.
17.
Федюкович Н.И.
«Анатомия и физиология»: Учеб.пособ. Ростов на Дону – Изд-во «Феникс», 2000г.
18.
Овчинников Ю.А.
Биоорганическая химия – М.: Просвещение 1987г. – 825 с.
|

Схема
развития кариеса
|
Приложение №1
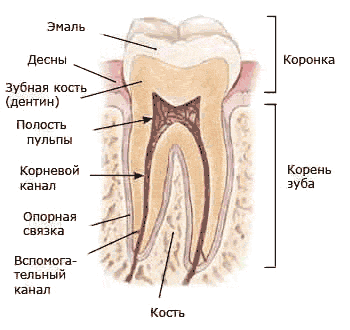
Схема строения здорового зуба
Приложение
№2
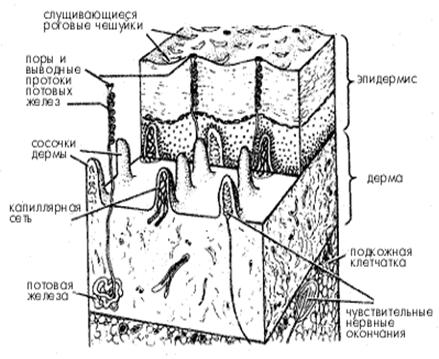
Схема
строения кожи
Приложение №3
Расшифровка
условных обозначений
|

|
|

|
Стирка
запрещена
|
|

|
Только ручная
стирка при температуре максимум 40°, не тереть, не отжимать
|
|

|
Ручная или
машинная стирка при температуре не выше указанной
|
|

|
Ручная или
машинная стирка. Внимательно придерживаться указанной температуры, не
подвергать сильной механической обработке. Умеренный отжим.
|
|

|
Очень
деликатная стирка в большом количестве воды, минимальная механическая
обработка, быстрое полоскание при низких оборотах
|
|

|
Запрещено
отжимать и высушивать в стиральной машине
|
|

|
Разрешено
отжимать и высушивать в стиральной машине
|
|

|
После отжима
разрешена вертикальная сушка
|
|

|
Сушить без
отжима в подвешенном состоянии
|
|

|
Высушивать
при нормальной температуре
|
|

|
Высушивать
при горячей температуре
|
|

|
Сушить на
горизонтальной поверхности
|
|

|
Гладить
запрещено
|
|

|
Разрешено
гладить при максимальной температуре 200°, допустимо для льна и хлопка; можно
слегка увлажнять изделие
|
|

|
Разрешено
гладить при максимальной температуре 150°, допустимо для шерсти и смешанных
волокон с полиэстером и вискозой; использовать влажную ткань
|
|

|
Разрешено гладить
при максимальной температуре 110°, допустимо для синтетики, нейлона, акрила,
полиэстера, ацетата; использовать тканевую прокладку, не пользоваться паром
|
|

|
Разрешено
гладить
|
|

|
При стирке не
использовать средства, содержащие отбеливатели (хлор)
|
|
|
Разрешена
стирка с отбеливателями, содержащими хлор; использовать только холодную воду,
следить за полным растворением порошка
|
|

|
Только сухая
чистка
|
|

|
Сухая чистка
с любым растворителем
|
|

|
Чистка только
с углеводородом, бензином, хлорным этиленом и монофтортрихлорметаном
|
|

|
Чистка с
использованием только углеводорода, бензина и трифтортрихорметана
|
|

|
Чистка только
с углеводородом, хлорным этиленом и монофтортрихлорметаном при ограниченном
добавлении воды, контроле за механическим воздействием и температуре сушки
|
|

|
Чистка только
с углеводородом и монофтортрихлорметаном при ограниченном добавлении воды,
контроле за механическим воздействием и температуре сушки
|
|
|
Химическая
чистка запрещена
|




